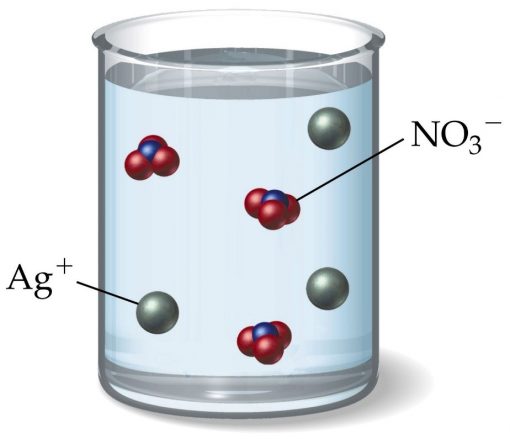
نیترات-نقره یک ترکیب شیمیایی با فرمول شیمیایی AgNO3 است. این ترکیب از یک پیوند یونی بین کاتیون نقره یعنی Ag+ و آنیون نیترات NO+3 تشکیل شده است. ماهیت یونی نیترات-نقره سبب انحلال آسان در آب و تجزیه به یونهای تشکیل دهنده آن میگردد. نیترات نقره پیش ساز بسیاری از مواد دیگر حاوی نقره از جمله ترکیبات نقره در عکاسی است. با مقایسه نیترات نقره و هالیدهای نقره که به دلیل حساسیت آنها به نور در عکاسی استفاده میشود درمییابیم که AgNO3 هنگام قرار گرفتن در معرض نور، پایدار است.
مقدمه ای بر
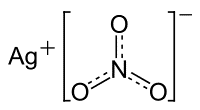
یون نیترات در در این ماده از یک اتم نیتروژن تشکیل شده که توسط سه اتم اکسیژن احاطه گشته است. پیوندهای نیتروژن و اکسیژن در این یون مشابه یکدیگر هستند. بار اتمی نیتروژن ۱- است، در حالی که هر اتم اکسیژن دارای بار ۳/۲- است. بار خالص یون نیترات ۱- است، با بار ۱+ که توسط یون Ag+ از طریق پیوند یونی در AgNO3 وجود دارد خنثی میشود. پایداری ساختار یون نیترات به دلیل وجود پدیده رزونانس است.
خواص فیزیکی
- جرم مولی نیترات نقره ۱۶۹.۸۷۲ گرم بر مول است.
- نیترات نقره بی رنگ و بی بو است.
- در حالت جامد، چگالی نیترات-نقره ۴.۳۵ گرم بر سانتی متر مکعب و در حالت مایع در دمای ۲۱۰ درجه سانتی گراد ۳.۹۷ گرم بر سانتی متر مکعب است.
- نقطه ذوب و جوش نیترات-نقره به ترتیب K ۴۸۲.۸ و K ۷۱۳ است.
- نیترات نقره مانند سایر ترکیبات یونی به آسانی در آب انحلال مییابد. حلالیت نیترات نقره در آب معادل ۱۲۲ گرم در ۱۰۰ میلی لیتر در دمای ۰ درجه سانتی گراد و ۲۵۶ گرم در ۱۰۰ میلی لیتر در دمای ۲۵ درجه سانتی گراد است.
- ساختار کریستالی نیترات-نقره متعامد است.
خواص شیمیایی
- خطرات نیترات-نقره شامل ماهیت سمی و خورنده بودن آن است.
- واکنش نیترات-نقره و اتانول بسیار انفجاری است.نقره موجود در این ماده توسط مس قابلیت جانشینی دارد که درنتیجه نیترات مس را تشکیل میدهد. معادله شیمیایی این واکنش به صورت بالا است:
- هنگامی که نیترا-نقره تا دمای ۴۴۰ درجه سانتیگراد حرارت داده شود، به طور کامل به اکسیژن، دی اکسید نیتروژن و نقره تجزیه میگردد.
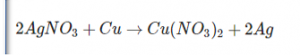
موارد استفاده
نیترات نقره در بسیاری از زمینهها مانند زیست شناسی، سنتز شیمیایی و پزشکی و دارویی کاربردهای فراوانی دارد. برخی موارد استفاده از این ماده به شرح زیر است:
- نیترات-نقره یک ترکیب همه کاره است. یون نیترات را میتوان به راحتی با لیگاندهای دیگری که به یون نقره متصل میشوند جایگزین نمود.
- توانایی نیترات-نقره برای تشکیل رسوبی از هالیدهای نقره هنگام کار با یونهای هالید در ساخت فیلمهای عکاسی مورد استفاده قرار میگیرد.
- بسیاری از مواد منفجره مبتنی بر نقره با واکنش رسوب نیترات-نقره تهیه میشوند.
- در زمینه شیمی معدنی، هالیدها با کمک نیترات نقره استخراج میشوند.
- شاخههایی از شیمی مثل شیمی تجزیه از این واکنش برای بررسی وجود آنیونهای هالید مانند یونهای یدید، برمید یا کلرید استفاده میکند.
- مخلوط آلکنها با کمک نیترات-نقره جدا میشوند زیرا کاتیون نقره به شکل برگشت پذیر با آلکنها پیوند برقرار میکند.
- نیترات-نقره به عنوان یک ضد عفونی کننده در بسیاری از مجموعههای پزشکی کارایی دارد.
- نیترات-نقره میتواند برای درمان و از بین بردن زگیلهای ناخواسته در انسان استفاده گردد.
سوالات متداول
سوال ۱: آیا این ماده خطرناک است؟
پاسخ: نیترات-نقره یک ماده اکسیدکننده است و به همین دلیل دور از ترکیبات آلی نگه داشته میشود. علیرغم استفاده گسترده از آن برای پیشگیری از سوزاک و جلوگیری از خونریزی از بینی، نیترات-نقره Thou بسیار سمی و خورنده است. قرار گرفتن کوتاه مدت در معرض نیترات-نقره هیچ عارضهای ایجاد نمیکند. اما با این وجود، قرار گرفتن طولانی مدت در معرض نیترات-نقره میتواند به چشم آسیب برساند.
سوال ۲: این ماده چگونه تهیه میشود-
پاسخ: نیترات نقره از ترکیب نقره با اسید نیتریک تهیه میگردد. اشیاء نقرهای معمولی که در این واکنشها استفاده میشوند، شمشهای نقره و ورقهای نقره هستند. محصولات تشکیل شده نیترات-نقره، آب و اکسیدهای نیتروژن هستند. محصولات جانبی این واکنش شیمیایی به غلظت اسید نیتریک بستگی دارد. توجه به این نکته حائز اهمیت است که چنین واکنشی به دلیل تکامل اکسیدهای سمی نیتروژن در طول واکنش، باید زیر یک هود بخار انجام شود. واکنش تولید نقره-نیترات به شرح زیر است:

تهیه و استاندارد سازی نقره-نیترات ۰.۱ مولار
آماده سازی محلول
- حدود ۱۰۰ میلی لیتر آب را در یک فلاسک حجمی ۱۰۰۰ میلی لیتری تمیز و خشک بریزید.
- طی هم زدن مداوم، حدود ۱۷ گرم ترکیب نیترات-نقره را اضافه کنید.
- حدود ۷۰۰ میلی لیتر آب مقطر بیشتر بیفزایید و مخلوط کنید.
- آن را با آب به حجم ۱۰۰۰ میلی لیتر برسانید. محلول را کاملاً مخلوط نمایید.
- محلول حاصل را حداقل یک ساعت نگه دارید و سپس استانداردسازی را انجام دهید.
استاندارد سازی این ماده
- حدود ۵۰ میلی گرم، وزن دقیق از کلرید سدیم معرف را که قبلاً در دمای ۱۱۰ درجه سانتی گراد به مدت ۲ ساعت خشک شده بود، به یک فلاسک مخروطی ۱۵۰ میلی لیتری منتقل کنید.
- در ۵ میلی لیتر آب مقطر حل کنید.
- ۲.۵ میلی لیتر اسید استیک، ۲۵ میلی لیتر متانول و حدود ۰.۲۵ میلی لیتر ائوزین y نشانگر اضافه کنید.
- ترجیحاً با یک همزن مغناطیسی هم بزنید.
- با محلول نیترات-نقره تیتر نمایید.
- مولاریته محلول را از طریق فرمول بالا محاسبه کنید:
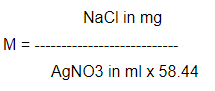
خلاصه
این ماده یک ترکیب شیمیایی با فرمول شیمیایی AgNO3 است. این ترکیب از یک پیوند یونی بین کاتیون نقره یعنی Ag+ و آنیون نیترات NO+3 تشکیل شده است. نیترات نقره در بسیاری از زمینهها مانند زیست شناسی، سنتز شیمیایی و پزشکی و دارویی کاربردهای فراوانی دارد.
جهت خرید و یا استعلام قیمت با ما تماس بگیرید یا در واتسپ پیام بزارید
مطالعه صدها مطلب علمی در حوزه بیولوژی
آرشیو جدیدترین خبرهای روز دنیای بیولوژی
نام مترجم: نگارالسادات موسوی