بیماری ها
سرطان آندومتر (Endometrial Cancer) چیست؟
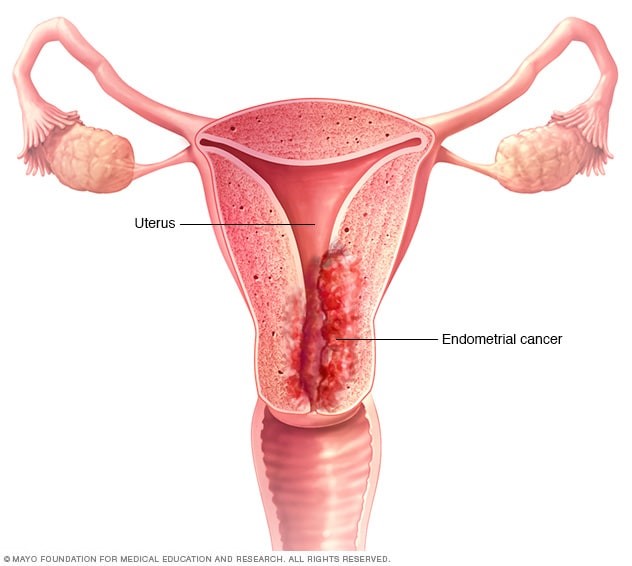
سرطان آندومتر (Endometrial Cancer) زمانی شروع میشود که سلولهای آندومتر (پوشش داخلی رحم) شروع به رشد خارج از کنترل میکنند. سلولها تقریباً در هر قسمت از بدن میتوانند به سرطان تبدیل شوند و به سایر قسمتهای بدن گسترش یابند.
در مورد رحم (uterus) و آندومتر (endometrium)
رحم اندامی تو خالی است که معمولاً به اندازه و شکل یک گلابی متوسط است. رحم محل رشد و نمو جنین در زمان بارداری است. این اندام دارای 2 بخش اصلی است (تصویر زیر را ببینید):
- قسمت بالایی رحم را بدن (body) یا بدنه (corpus) میگویند. (Corpus کلمه لاتین بدن است.)
- دهانه رحم (cervix) انتهای پایینی رحم است که آن را به واژن (vagina) وصل میکند.
وقتی مردم در مورد سرطان رحم صحبت میکنند، معمولاً منظورشان سرطانهایی است که در بدنه رحم شروع میشوند، نه دهانه رحم. (سرطان دهانه رحم یک نوع سرطان جداگانه است.)
بدن رحم دارای 2 لایه اصلی است:
- میومتر (myometrium) لایه بیرونی است. این لایه ضخیم ماهیچه ای برای بیرون راندن کودک در هنگام تولد مورد نیاز است.
- آندومتر (endometrium) لایه داخلی است. در طول چرخه قاعدگی زنانه، هورمونها باعث تغییر آندومتر میشوند. استروژن باعث ضخیم شدن آندومتر میشود تا در صورت بارداری بتواند جنین را تغذیه کند.
- اگر بارداری وجود نداشته باشد، استروژن در مقادیر کمتری تولید میشود و هورمون بیشتری به نام پروژسترون ساخته میشود. این هورمون باعث میشود که پوشش آندومتر از رحم خارج شده و به جریان قاعدگی (پریود) تبدیل شود. این چرخه تا یائسگی تکرار میشود.
همچنین لایه ای از بافت به نام سروزا (serosa) وجود دارد که قسمت بیرونی رحم را میپوشاند.
انواع سرطان آندومتر
سرطان آندومتر (که به آن کارسینوم آندومتر – endometrial carcinoma – نیز گفته میشود) در سلولهای پوشش داخلی رحم (آندومتر) شروع میشود. این نوع سرطان شایع ترین نوع سرطان در رحم است.
کارسینومهای آندومتر را میتوان بر اساس ظاهر سلولها در زیر میکروسکوپ به انواع مختلفی تقسیم کرد. (اینها انواع بافت شناسی – histologic types – نامیده میشوند.) این انواع عبارتند از:
- آدنوکارسینوما (Adenocarcinoma، اکثر سرطانهای آندومتر نوعی آدنوکارسینوم به نام سرطان اندومتریوئید یا endometrioid cancer هستند)
- کارسینوسارکوم رحم یا CS (Uterine carcinosarcoma، در ادامه و در بخش مبحث درجه بندی پوشش داده شده است)
- سرطان سلولی سنگفرشی (Squamous cell carcinoma)
- کارسینوم سلول کوچک (Small cell carcinoma)
- کارسینوم انتقالی (Transitional carcinoma)
- کارسینوم سروزی (Serous carcinoma)
کارسینوم سلول شفاف (Clear-cell carcinoma)، آدنوکارسینوم موسینوس (mucinous adenocarcinoma)، کارسینوم تمایز نیافته (undifferentiated carcinoma)، کارسینوم تمایز یافته (dedifferentiated carcinoma) و آدنوکارسینوم سروزی (adenocarcinomas Serous) از انواع کمتر شایع آدنوکارسینوم آندومتر هستند. آنها نسبت به بسیاری از انواع سرطان آندومتر تمایل به رشد و گسترش سریعتری دارند. آنها اغلب تا زمانی که تشخیص داده شوند به خارج از رحم گسترش یافته اند.
سرطان اندومتریوئید (Endometrioid cancer)
اکثر سرطانهای آندومتر آدنوکارسینوم هستند و سرطان آندومتریوئید شایع ترین نوع آدنوکارسینوم است. سرطان آندومتروئید از سلولهای غده ای شروع میشود و بسیار شبیه پوشش طبیعی رحم (اندومتر) است. برخی از این سرطانها دارای سلولهای سنگفرشی (سلولهای سنگفرشی سلولهای صاف و نازک هستند) و همچنین سلولهای غده ای هستن .
انواع (یا انواع فرعی) بسیاری از سرطانهای اندومتریوئید وجود دارد که عبارتند از:
- آدنوکارسینوم (با تمایز سنگفرشی)
- آدنوآکانتوما (Adenoacanthoma)
- آدنوسکواموس (Adenosquamous، سلول مختلط یا mixed cell)
- کارسینوم ترشحی (Secretory carcinoma)
- کارسینوم مژک دار (Ciliated carcinoma)
- آدنوکارسینوم ویلوگلندولار (Villoglandular adenocarcinoma)
درجه بندی سرطان آندومتر
درجه سرطان آندومتر بر اساس میزان سازماندهی سلولهای سرطانی به غدههایی است که شبیه غدد موجود در یک اندومتر طبیعی و سالم هستند.
در سرطانهای درجه پایین (درجه 1 و 2)، تعداد بیشتری از سلولهای سرطانی غدد تشکیل میدهند. در سرطانهای درجه بالاتر (درجه 3)، تعداد بیشتری از سلولهای سرطانی بی نظم هستند و غدد تشکیل نمیدهند.
- تومورهای درجه 1 دارای 95 درصد یا بیشتر از غدد تشکیل دهنده بافت سرطانی هستند.
- تومورهای درجه 2 بین 50 تا 94 درصد از غدد تشکیل دهنده بافت سرطانی را دارند.
- تومورهای درجه 3 کمتر از نیمی از غدد تشکیل دهنده بافت سرطانی را دارند. سرطانهای درجه 3 تهاجمی هستند (به سرعت رشد میکنند و گسترش مییابند) و چشم انداز بدتری را نسبت به سرطانهای درجه پایین دارند.
درجات 1 و 2 سرطان آندومتروئید از نوع 1 آندومتر هستند. سرطانهای نوع 1 معمولاً خیلی تهاجمی نیستند و به سرعت به بافتهای دیگر سرایت نمیکنند. تصور میشود که سرطان آندومتر نوع 1 ناشی از وجود استروژن بیش از حد است. آنها گاهی در اثر هیپرپلازی آتیپیک (atypical hyperplasia)، رشد بیش از حد غیر طبیعی سلولها در آندومتر ایجاد میشوند. (برای اطلاعات بیشتر در این مورد به مبحث عوامل خطرزا سرطان آندومتر مراجعه کنید.)
تعداد کمی از سرطانهای آندومتر، سرطان آندومتر نوع 2 هستند. سرطانهای نوع 2 به احتمال زیاد بیشتر رشد میکنند و در خارج از رحم پخش میشوند، آنها چشم انداز ضعیفتری دارند (نسبت به سرطانهای نوع 1). پزشکان تمایل دارند این سرطانها را با شدت بیشتری درمان کنند.
به نظر نمیرسد که این سرطانها در اثر وجود استروژن بیش از حد ایجاد شوند. سرطانهای نوع 2 شامل همه کارسینومهای آندومتر غیر از نوع 1 میشود، مانند کارسینوم سروز پاپیلاری، کارسینوم سلول شفاف، کارسینوم تمایز نیافته و کارسینوم آندومتروئید درجه 3. این سرطانها به هیچ وجه شبیه اندومتر طبیعی نیستند و به همین دلیل به آنها با تمایز ضعیف (poorly differentiated) یا درجه بالا (high-grade) میگویند.
کارسینوسارکوم رحم (CS) در آندومتر شروع میشود و دارای ویژگیهای کارسینوم آندومتر و سارکوم است. (سارکوم سرطانی است که در سلولهای عضلانی رحم شروع میشود.) در گذشته، CS نوع دیگری از سرطان رحم به نام سارکوم رحم در نظر گرفته میشد (به ادامه مبحث مراجعه کنید)، اما پزشکان اکنون بر این باورند که CS یک کارسینوم آندومتر است که بسیار غیر طبیعی است به حدی که دیگر شباهت زیادی به سلولهایی که از آنها گرفته شده است، ندارد (تمایز ضعیفی دارد).
CS رحم یک کارسینوم آندومتر نوع 2 است. تومورهای CS به عنوان تومورهای مزودرم مختلط بدخیم (malignant mixed mesodermal tumors) یا تومورهای مختلط مولرین بدخیم (malignant mixed mullerian tumors یا MMMTs) نیز شناخته میشوند. آنها حدود 3 درصد از سرطانهای رحم را تشکیل میدهند.
انواع دیگر سرطان در رحم
سارکوم رحم از لایه عضلانی (میومتر) یا بافت همبند رحم شروع میشود. این سرطانها شامل لیومیوسارکوم رحم (uterine leiomyosarcomas) و سارکوم استرومای آندومتر (endometrial stromal sarcomas) است. این سرطانها در این مطلب پوشش داده نشده اند اما در مطلب سارکوم رحم به تفصیل مورد بحث قرار گرفته اند.
سرطانهایی که از دهانه رحم شروع میشوند و سپس به رحم سرایت میکنند با سرطانهایی که در بدن رحم شروع میشوند، متفاوت هستند. آنها در مبحث سرطان دهانه رحم توضیح داده شده اند.
آمار کلیدی برای سرطان آندومتر
سرطان آندومتر چقدر شایع است؟
در ایالات متحده، سرطان آندومتر (پوشش داخلی رحم) شایع ترین سرطان اندامهای تناسلی زنانه است. تخمینهای انجمن سرطان آمریکا برای سرطان رحم در ایالات متحده برای سال 2022 عبارتند از:
- حدود 65950 مورد جدید سرطان بدن رحم (جسم رحم یا بدن) تشخیص داده میشود.
- حدود 12550 زن بر اثر سرطانهای بدن رحم خواهند مرد.
این تخمینها شامل سرطان آندومتر و سارکوم رحم میشود. تا 10 درصد از سرطانهای بدن رحم سارکوم هستند، بنابراین اعداد واقعی برای موارد سرطان آندومتر و مرگ و میر کمی کمتر از این تخمینها است.
احتمال ابتلا به سرطان آندومتر مادام العمر
سرطان آندومتر عمدتاً زنان یائسه را تحت تأثیر قرار میدهد. میانگین سنی زنانی که مبتلا به سرطان آندومتر تشخیص داده میشود 60 سال است. این سرطان در زنان زیر 45 سال غیر معمول است.
این سرطان در زنان سیاه پوست بیشتر از زنان سفید پوست دیده میشود و زنان سیاه پوست بیشتر در معرض مرگ ناشی از آن هستند.
امروزه بیش از 600000 بازمانده از سرطان آندومتر در ایالات متحده وجود دارد.
علائم و نشانههای سرطان آندومتر
چند علامت وجود دارد که ممکن است به ابتلا به سرطان آندومتر اشاره کند. برخی از آنها با پیشرفت سرطان (رشد و گسترش) شایع تر هستند.
خونریزی غیر معمول واژینال، لکه بینی یا وجود سایر ترشحات
حدود 90 درصد از زنان مبتلا به سرطان آندومتر خونریزی غیر طبیعی واژن دارند. این وضعیت ممکن است شامل تغییر در دورههای قاعدگی آنها، خونریزی بین دورهها یا خونریزی بعد از یائسگی باشد. مشکلات غیر سرطانی نیز میتوانند باعث خونریزی غیر طبیعی شوند اما مهم است که پزشک فوراً هر گونه خونریزی نامنظم را بررسی کند. اگر یائسگی را پشت سر گذاشته اید، بسیار مهم است که هرگونه خونریزی واژینال، لکه بینی یا ترشحات غیر طبیعی را به پزشک خود گزارش دهید.
ترشحات غیر خونی واژن نیز ممکن است نشانه سرطان آندومتر باشد. حتی اگر نمیتوانید خون را در ترشحات ببینید، به این معنی نیست که سرطان وجود ندارد. هر گونه ترشح غیر طبیعی باید توسط پزشک بررسی شود.
درد لگن، وجود توده و کاهش وزن
درد در لگن، احساس وجود توده (تومور) و کاهش وزن ناخواسته نیز میتواند از علائم ابتلا به سرطان آندومتر باشد. این علائم در مراحل بعدی بیماری بیشتر دیده میشود. با این حال، هرگونه تاخیر در مراجعه به پزشک ممکن است باعث پیشرفت بیشتر بیماری شود. این امر شانس موفقیت روند درمان را کاهش میدهد.
اگرچه هر یک از این علائم میتواند ناشی از چیزهایی غیر از سرطان نیز باشد اما مهم است که آنها را توسط پزشک بررسی کنید.
چه چیزی باعث سرطان آندومتر میشود؟
ما هنوز دقیقاً نمیدانیم که چه چیزی باعث بیشتر موارد ابتلا سرطان آندومتر میشود اما میدانیم که عوامل خطرزایی مانند چاقی و عدم تعادل هورمونی وجود دارد که به شدت با این سرطان مرتبط هستند.
ما میدانیم که اکثر سلولهای سرطانی آندومتر دارای گیرندههای استروژن و یا پروژسترون در سطوح خود هستند. به نوعی، تعامل این گیرندهها و این هورمونها منجر به افزایش رشد آندومتر میشود. این رشد افزایش یافته میتواند بیش از پیش غیر طبیعی شود تا زمانی که به سرطان تبدیل شود.
همان طور که در بخش عوامل خطرزا ذکر خواهد شد، بسیاری از عوامل خطرزای شناخته شده سرطان آندومتر بر تعادل بین استروژن و پروژسترون در بدن تأثیر میگذارد.
دانشمندان در حال فهم بیشتر در مورد تغییرات در DNA ژنهای خاص هستند که زمانی رخ میدهد که سلولهای طبیعی آندومتر سرطانی میشوند.
عوامل خطرزای سرطان آندومتر
عامل خطرزا هر چیزی است که شانس ابتلا به بیماری مانند سرطان را افزایش دهد. سرطانهای مختلف عوامل خطرزا متفاوتی دارند. برخی از عوامل خطرزا مانند سیگار کشیدن یا قرار گرفتن در معرض نور خورشید را میتوان تغییر داد. سایر موارد، مانند سن یا سابقه خانوادگی فرد، قابل تغییر و تعدیل نیستند.
اگرچه عوامل خاصی میتوانند خطر ابتلا به سرطان آندومتر را در زنان افزایش دهند، اما همیشه این عوامل باعث این بیماری نمیشوند. بسیاری از زنان با وجود داشتن عوامل خطرزا هرگز به سرطان آندومتر مبتلا نمیشوند.
برخی از زنان مبتلا به سرطان آندومتر نیز هیچ عامل خطرزای شناخته شده ای ندارند.
حتی اگر یک زن مبتلا به سرطان آندومتر دارای یک یا چند عامل خطرزا باشد، هیچ راهی برای دانستن اینکه کدام یک از آنها باعث سرطان او شده است، وجود ندارد.
عوامل زیادی بر خطر ابتلا به سرطان آندومتر تأثیر میگذارد، از جمله:
- چاقی
- چیزهایی که بر سطح هورمونها تأثیر میگذارند، مانند مصرف استروژن بعد از یائسگی، قرصهای ضد بارداری یا تاموکسیفن. تعداد سیکلهای قاعدگی (در طول زندگی)، بارداری، تومورهای تخمدانی خاص و سندرم تخمدان پلی کیستیک (polycystic ovarian syndrome یا PCOS)
- استفاده از دستگاه داخل رحمی (IUD)
- سن
- رژیم غذایی و ورزش
- دیابت نوع 2
- سابقه خانوادگی (داشتن بستگان نزدیک مبتلا به سرطان آندومتر یا کولورکتال)
- داشتن سرطان سینه یا تخمدان در گذشته
- داشتن هیپرپلازی آندومتر (endometrial hyperplasia) در گذشته
- قرار گرفتن تحت پرتو درمانی لگنی برای درمان سرطانی دیگر
برخی از این موارد مانند بارداری، قرصهای ضد بارداری و استفاده از دستگاههای داخل رحمی با خطر کمتر سرطان آندومتر مرتبط هستند، در حالی که بسیاری از آنها با خطر بالاتری مرتبط هستند. این عوامل و چگونگی تأثیر آنها بر خطر ابتلا به سرطان آندومتر با جزئیات بیشتری در ادامه پوشش داده شده است.
چاقی
چاقی یک عامل خطرزا قوی برای سرطان آندومتر بوده و با تغییرات هورمونی مرتبط است که در زیر به جزئیات بیشتر پرداخته شده است. تخمدانهای یک زن بیشتر استروژن او را قبل از یائسگی تولید میکنند. اما بافت چربی میتواند برخی هورمونهای دیگر (به نام آندروژن) را به استروژن تبدیل کند. این موضوع میتواند بر سطح استروژن تأثیر بگذارد، به خصوص پس از یائسگی. داشتن بافت چربی بیشتر میتواند سطح استروژن زنان را افزایش دهد که همین امر خطر ابتلا به سرطان آندومتر را افزایش میدهد.
در مقایسه با زنانی که وزن سالم و مناسبی دارند، سرطان آندومتر در زنان دارای اضافه وزن دو برابر بیشتر است (BMI 25 تا 29.9) و بیش از 3 برابر در زنان چاق شایع است (BMI > 30). شما میتوانید BMI خود را با استفاده از فرمول شاخص توده بدنی (BMI) پیدا کنید.
افزایش وزن با افزایش سن و تغییرات وزنی مکرر (بارها افزایش وزن و کاهش وزن در طول زندگی) نیز با خطر بالاتر سرطان آندومتر پس از یائسگی مرتبط است.
عوامل هورمونی
تعادل هورمونی زنان در ایجاد اکثر سرطانهای آندومتر نقش دارد. بسیاری از عوامل خطرزای سرطان آندومتر بر سطح استروژن تأثیر میگذارد. قبل از یائسگی، تخمدانها منبع اصلی 2 نوع اصلی هورمونهای زنانه استروژن (estrogen) و پروژسترون (progesterone) هستند.
تعادل بین این هورمونها هر ماه در طول چرخه قاعدگی زنان تغییر میکند. این پدیده باعث ایجاد قاعدگی ماهیانه در زنان و حفظ سلامت آندومتر میشود. تغییر در تعادل این هورمونها به سمت استروژن بیشتر، خطر ابتلا به سرطان آندومتر را در زنان افزایش میدهد.
پس از یائسگی، تخمدانها تولید این هورمونها را متوقف میکنند اما مقدار کمی استروژن هنوز هم به طور طبیعی در بافت چربی ساخته میشود. استروژن حاصل از بافت چربی بعد از یائسگی تأثیر بیشتری نسبت به قبل از یائسگی دارد.
استروژن درمانی (Estrogen therapy)
درمان علائم یائسگی با هورمونها به عنوان هورمون درمانی یائسگی (menopausal hormone therapy، یا گاهی اوقات درمان جایگزینی هورمونی یا hormone replacement therapy) شناخته میشود. استروژن بخش اصلی این روند درمانی است. درمان با استروژن میتواند به کاهش گر گرفتگی، بهبود خشکی واژن و جلوگیری از ضعیف شدن استخوانها (پوکی استخوان) که میتواند با یائسگی رخ دهد، کمک کند.
اما استفاده از استروژن به تنهایی (بدون پروژسترون) میتواند منجر به سرطان آندومتر در زنانی شود که هنوز رحم دارند. برای کاهش این خطر، یک پروژسترون ( خود پروژسترون یا دارویی مانند آن) باید همراه با استروژن داده شود. این روش هورمون درمانی ترکیبی (combination hormone therapy) نامیده میشود.
زنانی که پروژسترون را همراه با استروژن برای درمان علائم یائسگی مصرف میکنند، خطر ابتلا به سرطان آندومتر را در خود افزایش نمیدهند. با این حال، مصرف این ترکیب شانس ابتلای زنان به سرطان سینه و همچنین خطر لخته شدن خون به شکل جدی را افزایش میدهد.
اگر بعد از یائسگی هورمون مصرف میکنید (یا قصد مصرف آن را دارید)، مهم است که در مورد خطرات احتمالی (از جمله سرطان، لخته شدن خون، حملات قلبی و سکته) با پزشک خود صحبت کنید.
مانند هر داروی دیگری، هورمونها باید با کمترین دوز مورد نیاز و در کوتاه ترین زمان ممکن برای کنترل علائم استفاده شوند. مانند هر دارویی که برای مدت طولانی مصرف میکنید، باید به طور منظم به پزشک خود مراجعه کنید. متخصصان معاینات سالیانه لگنی را توصیه میکنند. اگر خونریزی یا ترشحات غیر طبیعی از واژن خود دارید، باید فوراً به پزشک مراجعه کنید. (تا معاینه بعدی خود منتظر نمانید).
قرصهای ضد بارداری (Birth control pills)
استفاده از قرصهای ضد بارداری (داروهای ضد بارداری خوراکی) خطر ابتلا به سرطان آندومتر را کاهش میدهند. میزان این خطر در زنانی که برای مدت طولانی قرص مصرف میکنند کمتر است و این محافظت حداقل تا 10 سال پس از قطع مصرف قرص توسط زن باقی میماند. اما مهم است که هنگام انتخاب یک روش پیشگیری از بارداری به تمام خطرات و فواید آن توجه شود. خطر سرطان آندومتر تنها یکی از عواملی است که باید در نظر گرفته شود. ایده خوبی است که در مورد مزایا و معایب انواع مختلف کنترل بارداری با مشاور پزشکی و بهداشتی خود صحبت کنید.
تعداد کل سیکلهای قاعدگی
داشتن چرخههای قاعدگی بیشتر در طول زندگی یک زن، خطر ابتلا به سرطان آندومتر را افزایش میدهد. شروع دورههای قاعدگی (پریود) قبل از 12 سالگی و یا یائسگی در مراحل بعدی زندگی، این خطر را افزایش میدهد. شروع زود هنگام قاعدگی برای زنانی که یائسگی زودرسی داشته اند، یک عامل کمتر خطرزا است. به همین ترتیب، یائسگی دیررس نیز ممکن است منجر به ایجاد خطر بالاتر در زنانی که قاعدگی آنها در اواخر دوران نوجوانی شروع شده است، نباشد.
بارداری
تعادل هورمونی در دوران بارداری به سمت پروژسترون بیشتر تغییر میکند. بنابراین داشتن بارداریهای زیاد به محافظت در برابر سرطان آندومتر کمک میکند. زنانی که هرگز باردار نشدهاند در معرض خطر بیشتری هستند، به خصوص اگر نابارور نیز باشند (نمیتوانند باردار شوند).
تاموکسیفن (Tamoxifen)
تاموکسیفن (Tamoxifen) دارویی است که برای کمک به پیشگیری و درمان سرطان سینه استفاده میشود. تاموکسیفن به عنوان یک ضد استروژن در بافت سینه عمل کرده اما مانند یک استروژن در رحم عمل میکند. این دارو در زنانی که یائسگی را پشت سر گذاشته اند، میتواند باعث رشد دیواره رحم شود که خطر ابتلا به سرطان آندومتر را افزایش میدهد.
خطر ابتلا به سرطان آندومتر ناشی از تاموکسیفن کم است (کمتر از 1 درصد در سال). زنانی که تاموکسیفن مصرف میکنند باید این خطر را در مقابل فواید این دارو در درمان و پیشگیری از سرطان سینه با یکدیگر در نظر بگیرند. این موضوعی است که زنان باید با پزشکان خود در میان بگذارند. اگر تاموکسیفن مصرف میکنید، باید سالیانه معاینات زنان و زایمان داشته باشید و حتماً هرگونه خونریزی غیر طبیعی را به پزشکتان گزارش دهید زیرا این عارضه میتواند نشانه سرطان آندومتر باشد.
تومورهای تخمدانی
نوع خاصی از تومور تخمدان – تومور سلولی گرانولوزا (granulosa cell tumor) – اغلب استروژن میسازد. استروژن ساخته شده توسط یکی از این تومورها به روش ترشح هورمون از تخمدانها کنترل نمیشود و گاهی اوقات میتواند منجر به ایجاد سطوح بالای استروژن شود. عدم تعادل هورمونی ناشی از آن میتواند آندومتر را تحریک کرده و حتی منجر به سرطان آندومتر شود. در واقع، گاهی اوقات خونریزی واژینال ناشی از سرطان آندومتر اولین علامت وجود یکی از این تومورها است.
سندرم تخمدان پلی کیستیک (Polycystic ovarian syndrome)
زنان مبتلا به بیماری به نام سندرم تخمدان پلی کیستیک (PCOS) دارای سطوح هورمونی غیر طبیعی مانند سطوح آندروژن (androgen، هورمونهای مردانه) و استروژن و سطوح پایین تر پروژسترون هستند. افزایش استروژن نسبت به پروژسترون میتواند شانس ابتلا به سرطان آندومتر را در زنان افزایش دهد. PCOS همچنین یکی از علل اصلی ناباروری در زنان است.
استفاده از دستگاه داخل رحمی
به نظر میرسد زنانی که از دستگاه داخل رحمی (intrauterine device یا IUD) برای کنترل بارداری استفاده میکنند، کمتر در معرض خطر ابتلا به سرطان آندومتر هستند. اطلاعات در مورد این اثر محافظتی محدود به IUDهایی است که حاوی هورمون نیستند. محققان هنوز مطالعه نکردهاند که آیا انواع جدیدتر IUD که پروژسترون آزاد میکنند تأثیری بر خطر سرطان آندومتر دارند یا خیر. اما این آی یو دیها گاهی برای درمان حالات پیش سرطانی و سرطانهای اولیه آندومتر در زنانی که مایل به باردار شدن در آینده هستند، استفاده میشوند.
سن
خطر ابتلا به سرطان آندومتر با افزایش سن در زنان افزایش مییابد.
رژیم غذایی و ورزش
رژیم غذایی پرچرب میتواند خطر ابتلا به بسیاری از سرطانها از جمله سرطان آندومتر را افزایش دهد. از آن جایی که غذاهای چرب نیز غذاهای پرکالری هستند، رژیم غذایی پرچرب میتواند منجر به چاقی شود که یک عامل خطرزا شناخته شده برای سرطان آندومتر میباشد. بسیاری از دانشمندان فکر میکنند که در واقع این راه اصلی است که در آن رژیم غذایی پرچرب بواسطه آن خطر ابتلا به سرطان آندومتر را افزایش میدهد. برخی از دانشمندان فکر میکنند که غذاهای چرب ممکن است تأثیر مستقیمی بر نحوه استفاده بدن از استروژن داشته باشند که خطر ابتلا به سرطان آندومتر را افزایش میدهد.
فعالیت بدنی خطر ابتلا به سرطان آندومتر را کاهش میدهد. بسیاری از مطالعات نشان دادهاند که زنانی که بیشتر ورزش میکنند کمتر در معرض خطر ابتلا به سرطان آندومتر هستند، در حالی که برخی دیگر نشان میدهند که زنانی که زمان بیشتری را در حالت نشسته سپری میکنند در معرض خطر بیشتری برای ابتلا به این نوع سرطان هستند.
دیابت (Diabetes)
خطر ابتلا به سرطان آندومتر ممکن است در زنان مبتلا به دیابت نوع 2 دو برابر بیشتر باشد. اما دیابت در افرادی که اضافه وزن داشته و فعالیت کمتری نیز دارند، شایعتر است که این مورد نیز از عوامل خطرزا سرطان آندومتر است. وجود این امر یافتن یک رابطه واضح را دشوار میکند.
سابقه خانوادگی
سرطان آندومتر در برخی از خانوادهها شایع است. برخی از این خانوادهها نیز خطر ابتلا به سرطان روده بزرگ را دارند. این وضعیت اختلال سرطان روده بزرگ غیر پولیپوز ارثی (HNPCC یا hereditary nonpolyposis colon cancer) نامیده میشود. نام دیگر HNPCC سندرم لینچ (Lynch syndrome) است. در بیشتر موارد، این اختلال به دلیل نقص در ژن ترمیم عدم تطابق MLH1 یا ژن MSH2 ایجاد میشود. اما حداقل 5 ژن دیگر میتوانند باعث ایجاد HNPCC شوند: MLH3، MSH6، TGBR2، PMS1 و PMS2. کپی غیر طبیعی از هر یک از این ژنها توانایی بدن را برای ترمیم آسیب به DNA یا کنترل رشد سلولی کاهش میدهد. این پدیده منجر به ایجاد خطر بسیار بالای سرطان روده بزرگ و همچنین خطر بالای سرطان آندومتر میشود. زنان مبتلا به این سندرم تا 70 درصد در معرض خطر ابتلا به سرطان آندومتر در برخی مواقع هستند ( این خطر برای زنان به طور کلی حدود 3 درصد است). این حالت خطر ابتلا به سرطان تخمدان نیز افزایش مییابد.
برخی از خانوادهها تنها به سرطان آندومتر مبتلا میشوند. این خانوادهها ممکن است یک اختلال ژنتیکی متفاوت داشته باشند که هنوز کشف نشده است.
سرطان سینه (Breast cancer) یا تخمدان (ovarian cancer)
زنانی که سرطان سینه یا سرطان تخمدان داشته اند نیز ممکن است خطر ابتلا به سرطان آندومتر را در خود افزایش دهند. برخی از عوامل خطرزای رژیم غذایی، هورمونی و تولید مثلی برای سرطان سینه و تخمدان نیز خطر سرطان آندومتر را افزایش میدهند.
هیپرپلازی آندومتر (Endometrial hyperplasia)
هیپرپلازی آندومتر افزایش رشد آندومتر است. هیپرپلازی خفیف (Mild) یا ساده (simple) – شایع ترین نوع – احتمال بسیار کمی برای تبدیل شدن به سرطان دارد. این بیماری ممکن است خود به خود یا پس از درمان با هورمون درمانی از بین برود. اگر هیپرپلازی “آتیپیک” نامیده شود، شانس بیشتری برای تبدیل شدن به سرطان دارد.هایپرپلازی آتیپیک ساده (Simple atypical hyperplasia) در صورت عدم درمان در حدود 8 درصد موارد به سرطان تبدیل میشود.هایپرپلازی آتیپیک پیچیده (Complex atypical hyperplasia یا CAH) در صورت عدم درمان، در 29 درصد موارد خطر تبدیل شدن به سرطان را دارد و خطر ابتلا به سرطان آندومتر شناسایی نشده در این بیماری حتی بیشتر است. به همین دلیل، CAH معمولاً درمان میشود. (درمان این بیماری در مبحث «آیا سرطان آندومتر قابل پیشگیری است؟» توضیح داده شده است.)
پرتو درمانی قبلی لگن
پرتوهای مورد استفاده برای درمان برخی سرطانهای دیگر میتواند به DNA سلولها آسیب برساند و گاهی خطر ابتلا به سرطان نوع دوم مانند سرطان آندومتر را افزایش میدهد.
آیا میتوان از سرطان آندومتر پیشگیری کرد؟
هیچ راه مطمئنی برای پیشگیری از سرطان آندومتر وجود ندارد. اما کارهایی وجود دارد که میتوانید انجام دهید که ممکن است به کاهش خطر ابتلا به این بیماری کمک کند. آنها بر اساس تغییر در عوامل خطرزای شما در هر زمان ممکن انجام میشوند.
به وزن سالم برسید و آن را حفظ کنید
زنانی که اضافه وزن دارند یا چاق هستند در مقایسه با زنان با وزن مناسب تا 3 برابر بیشتر در معرض ابتلا به سرطان آندومتر هستند. رسیدن به وزن سالم و حفظ آن یکی از راههای کاهش خطر ابتلا به این سرطان است.
فعالیت بدنی داشته باشید
مطالعات سطوح بالاتر فعالیت بدنی را با خطرات کمتر ابتلا به سرطان آندومتر مرتبط کرده اند، بنابراین انجام فعالیت بدنی منظم (ورزش) ممکن است راهی برای کمک به کاهش خطر سرطان آندومتر باشد. یک سبک زندگی فعال میتواند به شما کمک کند تا وزن سالمی داشته باشید و همچنین خطر ابتلا به فشار خون بالا و دیابت (یکی دیگر از عوامل خطر سرطان آندومتر) را در خود کاهش دهید.
مزایا و معایب هورمون درمانی را با پزشک خود در میان بگذارید
استروژن برای درمان علائم یائسگی به اشکال مختلف مانند قرصها، چسبهای پوستی، شاتها، کرمها و حلقههای واژینال موجود است. اگر به استفاده از استروژن برای علائم یائسگی فکر میکنید، از پزشک خود بپرسید که چگونه این عامل بر خطر ابتلا به سرطان آندومتر تأثیر میگذارد. پروژستینها (Progestins، داروهای مشابه پروژسترون) میتوانند خطر ابتلا به سرطان آندومتر را در زنانی که استروژن درمانی میکنند، کاهش دهند اما این ترکیب خطر ابتلا به سرطان سینه را افزایش میدهد. اگر هنوز رحم خود را دارید و در حال استفاده از استروژن درمانی هستید، حتما این موضوع را با پزشک خود در میان بگذارید.
اختلالات موجود در آندومتر را درمان کنید
دریافت درمان مناسب برای اختلالات پیش سرطانی آندومتر راه دیگری برای کاهش خطر ابتلا به سرطان آندومتر است. بیشتر سرطانهای آندومتر در طی چند سال ایجاد میشوند. بسیاری از آنها احتمالاً پس از تغییرات کمتر جدی در اندومتر به نام هیپرپلازی آندومتر شروع میشوند. (برای اطلاعات بیشتر در این مورد به عوامل خطرزا سرطان آندومتر مراجعه کنید.)
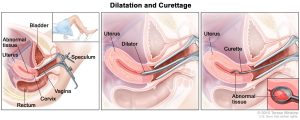
برخی از موارد هیپرپلازی بدون درمان برطرف میشود اما گاهی اوقات نیاز به درمان هورمونی یا حتی جراحی نیز دارند. درمان با پروژستینها (به هورمون درمانی برای سرطان آندومتر مراجعه کنید) و اتساع و کورتاژ (dilation and curettage یا D&C) یا هیسترکتومی (hysterectomy، برداشتن رحم) میتواند از تبدیل شدن هیپرپلازی به سرطان جلوگیری کند. (D&C در مبحث آزمایشات سرطان آندومتر توضیح داده شده است.)
خونریزی غیر طبیعی واژینال شایع ترین علامت پیش سرطانی و سرطان آندومتر است. اگر خونریزی غیر معمول دارید، به پزشک مراجعه کرده و فورا آن را بررسی کنید.
آیا میتوان سرطان آندومتر را زود تشخیص داد؟
بهترین راه برای یافتن سرطان آندومتر در زمانی که کوچک است (در مراحل اولیه) این است که در صورت داشتن علائم و نشانههای سرطان آندومتر، مانند خونریزی غیر طبیعی واژینال یا ترشحات (که در بین پریودها بدتر میشوند یا بعد از یائسگی اتفاق میافتند) به پزشک مراجعه کنید. تشخیص زود هنگام شانس درمان موفقیت آمیز سرطان را افزایش میدهد.
اکثر زنان مبتلا به سرطان آندومتر خونریزی غیر طبیعی واژن دارند. با این حال، برخی از سرطانهای آندومتر ممکن است قبل از ایجاد علائم و نشانهها به مرحله پیشرفته برسند. این بدان معنی است که سرطان بزرگ است و ممکن است قبل از ایجاد هر گونه مشکلی گسترش یافته باشد.
تستهای تشخیص زود هنگام سرطان آندومتر
تشخیص زود هنگام (که غربالگری – screening – نیز نامیده میشود) به استفاده از آزمایشات برای یافتن بیماری مانند سرطان در افرادی که علائم آن بیماری را ندارند، اشاره دارد. آزمایشهای تشخیص زود هنگام میتوانند به یافتن برخی از انواع سرطان در مراحل اولیه کمک کنند – زمانی که کوچک هستند و فراتر از جایی که در آن شروع شده اند، گسترش نیافته اند.
اگر در معرض خطر ابتلا متوسط هستید
در حال حاضر، هیچ آزمایش یا آزمایش غربالگری برای یافتن زود هنگام سرطان آندومتر در زنانی که در معرض خطر متوسط ابتلا به سرطان آندومتر هستند و هیچ علامتی ندارند، وجود ندارد.
انجمن سرطان آمریکا توصیه میکند که در زمان یائسگی، به همه زنان در مورد خطرات و علائم سرطان آندومتر گفته شود و آنها شدیدا تشویق شوند که هرزگونه خونریزی، ترشح یا لکه بینی واژینال را به پزشک خود گزارش دهند.
زنان همچنین باید در مورد معاینه منظم لگن با پزشک خود صحبت کنند. معاینه لگن میتواند برخی از سرطانها، از جمله برخی سرطانهای پیشرفته رحم را پیدا کند اما برای یافتن سرطانهای اولیه آندومتر چندان مفید نیست.
تستهای غربالگری مورد استفاده برای سرطان دهانه رحم، مانند تست پاپ (Pap test) یا تست HPV (human papillomavirus یا ویروس پاپیلومای انسانی) تستهای موثری برای سرطان آندومتر نیستند. تست پاپ که زنان را از نظر سرطان دهانه رحم غربالگری میکند، گاهی اوقات میتواند برخی از سرطانهای اولیه آندومتر را پیدا کند اما آزمایش خوبی برای این نوع سرطان نیست. برای دریافت اطلاعات بیشتر در این زمینه به مبحث تستهای غربالگری سرطان دهانه رحم در مطلب سرطان دهانه رحم مراجعه کنید.
اگر در معرض خطر ابتلا بیشتری هستید
انجمن سرطان آمریکا توصیه میکند که بیشتر زنانی که در معرض خطر ابتلا به سرطان آندومتر هستند، باید از خطر ابتلا به سرطان آندومتر مطلع شوند و هر زمان که خونریزی غیر طبیعی واژینال داشتند به پزشک خود مراجعه کنند. این شامل زنانی میشود که به دلیل سن، یائسگی دیررس، زایمان نکردن، ناباروری، چاقی، دیابت، فشار خون بالا، درمان با استروژن یا درمان با تاموکسیفن خطر ابتلا در آنها افزایش مییابد.
زنانی که سرطان روده بزرگ غیر پولیپوز ارثی (HNPCC یا سندرم لینچ) دارند (یا ممکن است داشته باشند) در معرض خطر بسیار بالایی برای ابتلا به سرطان آندومتر هستند.
اگر چندین نفر از اعضای خانوادهتان سرطان روده بزرگ یا اندومتر داشته اند، برای اطلاع از خطر ابتلا به HNPCC در خانواده خود، مشاوره ژنتیک را در نظر بگیرید. اگر شما (یا یکی از بستگان نزدیکتان) آزمایش ژنتیک داده باشد و مشخص شود که در یکی از ژنهای HNPCC دارای جهش است، شما در معرض خطر ابتلا به سرطان آندومتر و همچنین انواع دیگر سرطان هستید. برای اطلاعات بیشتر در این مورد به مبحث درک تست ژنتیک مراجعه کنید.
انجمن سرطان آمریکا به زنانی که HNPCC دارند (یا ممکن است داشته باشند) توصیه میکند که آزمایش سالانه سرطان آندومتر با بیوپسی آندومتر از سن 35 سالگی را انجام دهند. این امر در مورد زنانی که حامل جهشهای ژنی مرتبط با HNPCC هستند و زنانی که احتمالاً حامل چنین جهشی هستند (آنهایی که دارای جهش شناخته شده در خانواده هستند) و زنان خانوادههایی که تمایل به ابتلا به سرطان روده بزرگ دارند و در آن آزمایشهای ژنتیکی انجام نشده است، صدق میکند.
گزینه دیگر برای زنی که HNPCC دارد (یا ممکن است داشته باشد) این است که پس از اتمام فرزند آوری، هیسترکتومی (hysterectomy) انجام دهد.
آزمایشات سرطان آندومتر
سرطان آندومتر اغلب پس از مراجعه خانم به پزشک به دلیل داشتن علائم تشخیص داده میشود.
اگر احتمال ابتلا به سرطان آندومتر در شما وجود دارد، باید توسط متخصص زنان معاینه شوید. این فرد یک پزشک آموزش دیده برای تشخیص و درمان بیماریهای دستگاه تناسلی زنان است. متخصص زنان میتواند سرطان آندومتر را تشخیص داده و گاها آن را درمان کند. متخصصان در درمان سرطان آندومتر و سایر اندامهای تناسلی زنانه، انکولوژیست زنان (gynecologic oncologists) نامیده میشوند. این پزشکان میتوانند تمام مراحل سرطان آندومتر را درمان میکنند.
تاریخچه پزشکی و معاینه فیزیکی
اگر هر یک از علائم سرطان آندومتر را دارید (به مبحث علائم و نشانههای سرطان آندومتر مراجعه کنید)، باید فوراً به پزشک مراجعه کنید. پزشک در مورد علائم، عوامل خطرزا و سابقه پزشکی شما سوال خواهد کرد. پزشک همچنین معاینه فیزیکی و معاینه لگن را نیز انجام میدهد.
سونوگرافی (Ultrasound)
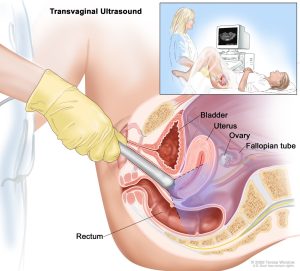
سونوگرافی اغلب یکی از اولین آزمایشاتی است که برای بررسی رحم، تخمدانها و لولههای فالوپ در زنان مبتلا به مشکلات احتمالی زنانه استفاده میشود. اولتراسوند از امواج صوتی برای گرفتن عکس از داخل بدن استفاده میکند. یک دستگاه کوچک (که مبدل – transducer – یا کاوشگر – probe – نامیده میشود) امواج صوتی را منتشر کرده و پژواکها را هنگام جهش از اندامها دریافت میکند. یک کامپیوتر پژواکها را به تصاویر تبدیل میکند.
برای سونوگرافی لگن، مبدل روی پوست قسمت تحتانی شکم (abdomen) حرکت میکند. اغلب، برای گرفتن عکسهای خوب از رحم، تخمدانها، لولههای فالوپ و مثانه باید پر باشند. به همین دلیل است که از زنانی که سونوگرافی لگن دریافت میکنند، خواسته میشود قبل از انجام آزمایش، آب زیادی بنوشند.
سونوگرافی ترانس واژینال (transvaginal ultrasound یا TVUS) اغلب برای بررسی رحم بهتر است. برای این آزمایش، پروب TVUS (که مانند مبدل اولتراسوند عمل میکند) داخل واژن قرار میگیرد. از تصاویر TVUS میتوان برای مشاهده اینکه آیا رحم حاوی توده (تومور) است یا اینکه آندومتر ضخیم تر از حد معمول است یا خیر، استفاده کرد که میتواند نشانه سرطان آندومتر باشد. همچنین این روش ممکن است به بررسی اینکه آیا سرطان در لایه عضلانی رحم (میومتر) رشد میکند یا خیر، کمک کند.
ممکن است قبل از سونوگرافی از یک لوله کوچک برای قرار دادن آب نمک (سالین یا saline) در رحم استفاده شود. این کار به پزشک کمک میکند تا پوشش رحم را با وضوح بیشتری ببیند. این روش سونوگرافی انفوزیون نمک (saline infusion sonogram) یا هیستروسونوگرافی (hysterosonogram) نامیده میشود. (Sonogram اصطلاح دیگری برای سونوگرافی است.)
سونوگرافی میتواند برای دیدن پولیپ (رشد) آندومتر، اندازه گیری ضخامت آندومتر به پزشکان کمک کند تا ناحیه ای را که میخواهند بیوپسی کنند، مشخص کنند.
نمونه برداری از بافت آندومتر
برای اینکه متوجه شوند دقیقاً چه نوع تغییر آندومتر وجود دارد، پزشک باید مقداری بافت را خارج کند تا بتوان آن را آزمایش کرده و با میکروسکوپ بررسی کرد. بافت آندومتر را میتوان با بیوپسی (نمونه برداری) آندومتر یا با اتساع و کورتاژ (D&C) همراه با هیستروسکوپی یا بدون آن برداشت. متخصص زنان معمولاً یک سری اقدامات را انجام میدهد که در زیر توضیح داده شده است.
بیوپسی آندومتر (Endometrial biopsy)
بیوپسی آندومتر رایج ترین آزمایش مورد استفاده برای سرطان آندومتر است و در زنان یائسه بسیار دقیق است. این آزمایش در مطب پزشک قابل انجام است. یک لوله بسیار نازک و انعطاف پذیر از طریق دهانه رحم وارد رحم میشود. سپس با استفاده از ساکشن (suction)، مقدار کمی آندومتر از طریق لوله خارج میشود. ساکشن حدود یک دقیقه یا کمتر طول میکشد. درد این کار شباهت زیادی به دردهای قاعدگی دارد و با مصرف یک داروی ضد التهاب غیر استروئیدی (onsteroidal anti-inflammatory drug، مانند ایبوپروفن یا ibuprofen) قبل از عمل میتوان به آن کمک کرد. گاهی اوقات از یک سوزن نازک برای تزریق داروی بی حس کننده (بی حس کننده موضعی) به دهانه رحم درست قبل از عمل استفاده میشود تا به کاهش درد کمک کند.
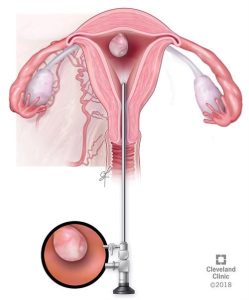
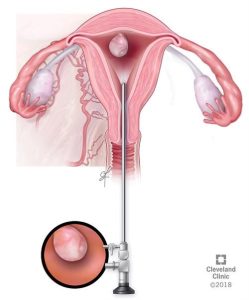
هیستروسکوپی (Hysteroscopy)
برای این روش، پزشک یک دستگاه بزرگ کننده کوچک (با قطر حدود 1/6 اینچ) را از طریق دهانه رحم وارد رحم میکند. برای دید بهتر از داخل (پوشش) رحم، رحم با آب نمک (سالین) پر میشود. این کار به پزشک اجازه میدهد تا هر چیز غیر طبیعی مانند سرطان یا پولیپ را پیدا کرده و از آن نمونه برداری کند. این کار معمولاً با استفاده از بی حسی موضعی (داروی بی حسی) در حالی که بیمار بیدار است، انجام میشود.
دیلاتاسیون و کورتاژ (Dilation and curettage یا D&C)
اگر نمونه بیوپسی آندومتر بافت کافی را فراهم نکند یا اگر بیوپسی نشان دهنده سرطان باشد اما نتایج نامشخص است، باید D&C انجام شود. در این روش سرپایی، دهانه رحم بزرگ شده (گشاد میشود) و از ابزار خاصی برای تراشیدن بافت از داخل رحم استفاده میشود. این کار ممکن است همراه با هیستروسکوپی یا بدون آن انجام شود.
این روش حدود یک ساعت طول میکشد و ممکن است نیاز به بیهوشی عمومی (حالتی که از داروها برای به خواب رفتن عمیق شما استفاده میشود) یا آرام بخش (داروها در داخل رگ شما تزریق میشوند تا شما را خواب آلود کنند) یا با تزریق بی حسی موضعی به دهانه رحم یا نخاع داشته باشد (اپیدورال یا epidural). D&C معمولاً در یک منطقه جراحی سرپایی یک کلینیک یا بیمارستان انجام میشود. اکثر زنان بعد از این روش احساس ناراحتی کمی دارند.
آزمایش نمونههای بافت آندومتر
نمونههای بافت آندومتر که با بیوپسی یا D&C برداشته شده اند با میکروسکوپ بررسی میشوند تا بررسی کنند آیا سرطان وجود دارد یا خیر. اگر سرطان پیدا شود، گزارش آزمایشگاهی، نوع سرطان آندومتر (مانند آندومتریوئید یا سلول شفاف) و درجه آن را نشان میدهد.
سرطان آندومتر بر اساس میزان طبیعی بودن ظاهر آندومتر در مقیاس 1 تا 3 درجه بندی میشود. (به مبحث «سرطان آندومتر چیست؟» مراجعه کنید) زنان مبتلا به سرطانهای درجه پایین کمتر احتمال دارد که به سرطان در سایر قسمتهای بدن خود مبتلا شوند و احتمال بازگشت سرطان پس از درمان (عود کردن) در آنها کمتر است.
آزمایش تغییرات ژنی و پروتئینی در سلولهای سرطانی
اگر پزشک به سرطان روده بزرگ غیر پولیپوز ارثی (HNPCC) به عنوان یک علت زمینهای سرطان آندومتر مشکوک باشد، سلولهای تومور را میتوان برای بررس وجود تغییرات پروتئینی و ژنی مورد آزمایش قرار داد. نمونههایی از تغییرات مرتبط با HNPCC عبارتند از:
- داشتن پروتئینهای ترمیم عدم تطابق (mismatch repair یا MMR) کمتر
- نقص در ژنهای ترمیم عدم تطابق (Defects in mismatch repair genes یا dMMR)
- تغییرات DNA (سطوح بالای ناپایداری در ریزماهواره – microsatellite – یا MSI-H) که میتواند زمانی اتفاق بیفتد که یکی از ژنهای ایجاد کننده HNPCC معیوب باشد.
اگر این تغییرات در پروتئین یا DNA وجود داشته باشد، پزشک ممکن است آزمایش ژنتیکی را برای ژنهایی که باعث ایجاد HNPCC میشوند، پیشنهاد دهد.
آزمایش سلولهای سرطانی برای dMMR، MSI-H و یا بار جهشی توموری بالا (TMB-H یا high tumor mutational burden) نیز ممکن است انجام شود تا بررسی کنند آیا درمان با ایمونوتراپی ممکن است گزینه مناسبی باشد یا خیر (به ویژه برای سرطانهای پیشرفتهتر آندومتر).
آزمایشاتی برای بررسی گسترش سرطان
اگر پزشک مشکوک باشد که سرطان شما پیشرفته است، احتمالاً باید آزمایشهای دیگری را برای بررسی گسترش سرطان انجام دهید.
اشعه ایکس قفسه سینه
ممکن است یک عکس رادیوگرافی ساده از قفسه سینه انجام شود تا مشخص شود آیا سرطان به ریههای شما سرایت کرده است یا خیر.
اسکن توموگرافی کامپیوتری (CT یا Computed tomography)
سی تی اسکن یک روش استفاده از اشعه ایکس است که تصاویر دقیق و مقطعی از داخل بدن شما ایجاد میکند. برای سی تی اسکن، در حالی که عکس برداری با اشعه ایکس انجام میشود، روی میز دراز میکشید. به جای گرفتن یک عکس، مانند یک اشعه ایکس استاندارد، یک سی تی اسکنر در حالی که دوربینش به دور شما میچرخد، عکسهای زیادی را از بدن شما میگیرد. سپس یک کامپیوتر این تصاویر را با هم ترکیب میکند تا تصویری از قسمتی از بدن شما ایجاد شود. این دستگاه از بسیاری از برشهای قسمتی از بدن شما که در حال مطالعه است، عکس میگیرد.
سی تی اسکن برای تشخیص سرطان آندومتر استفاده نمیشود. اما این روشها میتوانند کمک کنند که آیا سرطان به سایر اندامها سرایت کرده است و اینکه آیا بعد از درمان دوباره عود کرده است یا خیر.

تصویر برداری رزونانس مغناطیسی (Magnetic resonance imaging یا MRI)
اسکنهای MRI از امواج رادیویی و آهنرباهای قوی به جای اشعه ایکس استفاده میکنند. انرژی امواج رادیویی جذب میشود و سپس در الگویی که بر اساس نوع بافت و بیماریهای خاص شکل میگیرد، آزاد میشود. یک کامپیوتر الگوی امواج رادیویی منتشر شده توسط بافتها را به تصویری بسیار دقیق از داخل بدن تبدیل میکند.
این روش نیز برشهای مقطعی بدن را مانند یک سی تی اسکنر و همچنین برشهایی موازی با طول بدن شما را ایجاد میکند.
اسکن MRI برای بررسی مغز و نخاع بسیار مفید است. همچنین برخی پزشکان فکر میکنند که MRI روش خوبی برای تشخیص اینکه آیا سرطان آندومتر وجود دارد و تعیین اینکه تا چه اندازه به داخل بدن رحم رشد کرده است، میباشد. اسکن MRI همچنین ممکن است با تکنیک خاصی که از ذرات بسیار ریز اکسید آهن استفاده میکند، به یافتن غدد لنفاوی بزرگ شده نیز کمک کند. این ذرات به داخل ورید انتقال داده شده و در غدد لنفاوی مستقر میشوند، جایی که میتوان آنها را با MRI شناسایی کرد.
توموگرافی گسیل پوزیترون (Positron emission tomography یا PET)
در این آزمایش گلوکز رادیو اکتیو (قند) برای یافتن سلولهای سرطانی به فرد داده میشود. از آن جایی که سرطانها از گلوکز (قند) با سرعت بیشتری نسبت به بافتهای طبیعی استفاده میکنند، رادیو اکتیویته تمایل به جمع شدن در سرطان دارد. یک اسکنر میتواند رسوبات رادیو اکتیو را شناسایی کند. این آزمایش میتواند برای شناسایی مجموعههای کوچکی از سلولهای سرطانی مفید باشد. اسکنرهای ویژه اسکن PET را با سی تی اسکن ترکیب میکنند تا مناطق گسترش سرطان را با دقت بیشتری مشخص کنند. اسکن PET بخشی معمولی از کارهای اولیه سرطان آندومتر نیست اما ممکن است برای موارد پیشرفته تر استفاده شود.
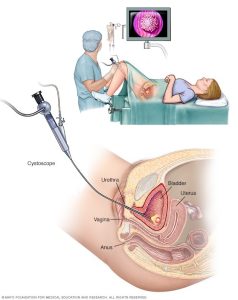
سیستوسکوپی (Cystoscopy) و پروکتوسکوپی (proctoscopy)
اگر زنی مشکلاتی داشته باشد که نشان دهد سرطان به مثانه یا راست روده سرایت کرده است، احتمالاً داخل این اندامها بواسطه مشاهده از طریق یک لوله روشن دیده میشود. در سیستوسکوپی لوله از طریق مجرای ادرار وارد مثانه میشود.
در پروکتوسکوپی لوله در رکتوم (rectum) قرار میگیرد. این معاینات به پزشک اجازه میدهد تا به دنبال یافتن سرطان باشد. نمونههای بافتی کوچک را نیز میتوان در طی این روشها برای انجام آزمایش برداشت. این نمونه برداریها را میتوان با استفاده از بی حسی موضعی انجام داد اما برخی از بیماران ممکن است نیاز به بیهوشی عمومی داشته باشند. پزشک به شما اطلاع میدهد که قبل و بعد از این آزمایشات چه انتظاری باید داشته باشید. این روشها در گذشته بسیار مورد استفاده قرار میگرفتند اما اکنون این روش به ندرت بخشی از روند کار برای سرطان آندومتر است.
آزمایشات خون
شمارش کامل خون (Complete blood count)
شمارش کامل خون (CBC) آزمایشی است که میزان سلولهای مختلف خون مانند گلبولهای قرمز، گلبولهای سفید و پلاکتها را اندازه گیری میکند. سرطان آندومتر ممکن است باعث خونریزی شود که همین امر میتواند منجر به کاهش تعداد گلبولهای قرمز خون (کم خونی یا anemia) شود.
آزمایش خون CA-125
CA-125 مادهای است که توسط بسیاری از سرطانهای آندومتر و تخمدان اما نه همه آنها، در جریان خون آزاد میشود. اگر زنی مبتلا به سرطان آندومتر باشد، سطح بسیار بالای CA-125 خون نشان میدهد که سرطان احتمالاً به خارج از رحم گسترش یافته است. برخی از پزشکان سطح CA-125 را قبل از جراحی یا سایر روندهای درمانی بررسی میکنند. اگر سطح این ماده در نتایج بالا رفته باشد، میتوان مجدداً این آزمایش را انجام داد تا بفهمیم که روند درمان چقدر خوب عمل میکند (در صورت برداشتن تمام سرطان، سطح این ماده پس از جراحی کاهش مییابد).
سطوح CA-125 برای تشخیص سرطان آندومتر مورد نیاز نیست، بنابراین این آزمایش بر روی همه بیماران انجام نمیشود.
مراحل سرطان آندومتر
پس از تشخیص سرطان آندومتر در یک زن، پزشکان سعی میکنند بفهمند که آیا این سرطان گسترش یافته است یا خیر و اگر چنین است، این گسترش تا چه حد است. این فرآیند مرحله بندی (staging) نامیده میشود. مرحله سرطان، میزان سرطان در بدن را توصیف میکند. این کار به تعیین اینکه سرطان چقدر جدی است و بهترین روش درمان آن کمک میکند. مرحله یکی از مهم ترین عوامل در تصمیم گیری برای درمان سرطان و تعیین میزان موفقیت روند درمان است.
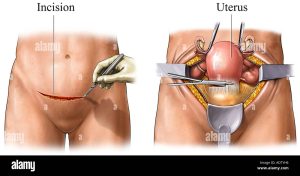
مراحل سرطان آندومتر از مرحله I (1) تا IV (4) متغیر است. به عنوان یک قاعده، هرچه این عدد کمتر باشد، سرطان کمتر گسترش یافته است. عدد بالاتر، مانند مرحله IV، به معنای گسترش سرطان به سایر قسمتهای بدن است. در یک مرحله، حرف قبلی به معنای مرحله پایین تر است. اگرچه سرطان هر فرد منحصر به فرد است اما سرطانهایی که مراحل مشابهی دارند، چشم انداز مشابهی نیز داشته و اغلب به روش مشابهی نیز درمان میشوند.
مرحله سرطان چگونه تعیین میشود؟
2 سیستم مورد استفاده برای مرحله بندی سرطان آندومتر، سیستم FIGO (فدراسیون بین المللی زنان و زایمان یا International Federation of Gynecology and Obstetrics) و سیستم مرحله بندی TNM کمیته مشترک آمریکا در سرطان اساساً یکسان هستند.
هر دوی آنها این سرطان را بر اساس 3 عامل مرحله بندی (طبقه بندی) میکنند:
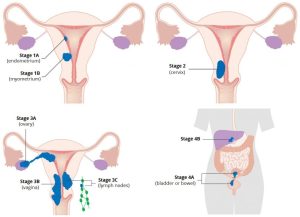
- وسعت (اندازه) تومور (T): سرطان تا چه اندازه به داخل رحم رشد کرده است؟ آیا سرطان به ساختارها یا اندامهای مجاور رسیده است؟
- گسترش به غدد لنفاوی مجاور (N): آیا سرطان به غدد لنفاوی پارا آئورت (para-aortic lymph nodes) گسترش یافته است؟ این غدد لنفاوی در لگن یا اطراف آئورت (شریان اصلی که از قلب به سمت پشت شکم و لگن میرود) قرار گرفته اند.
- گسترش (متاستاز) به نقاط دور دست (M): آیا سرطان به غدد لنفاوی دور دست یا اندامهای دور دست در سایر قسمتهای بدن گسترش یافته است؟
اعداد یا حروف بعد از T، N و M جزئیات بیشتری در مورد هر یک از این عوامل ارائه میدهند. اعداد بالاتر به معنای پیشرفته تر بودن سرطان است. هنگامی که دسته بندیهای T، N، و M یک فرد مشخص شد، این اطلاعات در فرآیندی به نام گروه بندی مرحله ای (stage grouping) با یکدیگر ترکیب میشوند تا یک مرحله کلی را تعیین کنند.
سیستم مرحله بندی از مرحله پاتولوژیک (pathologic stage) استفاده میکند. این مرحله با بررسی بافت برداشته شده در طی یک عمل جراحی مشخص میشود. این روش به عنوان مرحله بندی جراحی (surgical staging) نیز شناخته میشود. گاهی اوقات، اگر جراحی بلافاصله امکان پذیر نباشد، به جای آن به سرطان یک مرحله بالینی (clinical stage) داده میشود. این مرحله بر اساس نتایج یک معاینه فیزیکی، بیوپسی و آزمایشات تصویر برداری انجام شده قبل از جراحی مشخص میشود.
میزان بقا (زنده مانی) برای سرطان آندومتر
نرخ بقا میتواند به شما ایده دهد که چند درصد از افراد مبتلا به همان نوع و مرحله سرطان در مدت زمان معینی (معمولاً 5 سال) پس از تشخیص هنوز زنده هستند. این آمار نمیتوانند به شما بگویند که چقدر زنده خواهید ماند اما ممکن است به شما کمک کنند تا درک بهتری از احتمال موفقیت روند درمانیتان داشته باشید.
به خاطر داشته باشید که میزان بقا یک عدد تخمینی است و اغلب بر اساس نتایج قبلی تعداد زیادی از افرادی است که سرطان خاصی داشته اند اما این آمار نمیتوانند پیش بینی کنند که در مورد فرد خاصی چه اتفاقی خواهد افتاد. این اعداد میتوانند گیج کننده باشند و ممکن است شما را به پرسیدن سوالات بیشتری سوق دهند. پزشک شما با وضعیت شما آشناست. از وی بپرسید که چگونه این اعداد ممکن است برای شما اعمال شوند.
نرخ بقای نسبی 5 ساله (5-year relative survival rate) چقدر است؟
نرخ بقای نسبی، زنان با همان نوع و مرحله سرطان آندومتر را با زنان موجود در کل جمعیت مقایسه میکند. برای مثال، اگر نرخ بقای نسبی 5 ساله برای مرحله خاصی از سرطان آندومتر 90 درصد باشد، این عدد به این معنی است که زنانی که به آن سرطان مبتلا هستند، به طور متوسط حدود 90 درصد این احتمال را دارا هستند که تا 5 سال آینده پس از تشخیص ابتلا به بیماری زنده بمانند.
این اعداد از کجا میآیند؟
انجمن سرطان آمریکا به اطلاعات پایگاه داده SEER که توسط موسسه ملی سرطان (National Cancer Institute یا NCI) نگهداری میشوند، برای بدست آوردن آمار بقای انواع مختلف سرطان متکی است.
پایگاه داده SEER نرخ بقای نسبی 5 ساله سرطان آندومتر در ایالات متحده را بر اساس میزان گسترش سرطان بررسی میکند. با این حال، پایگاه داده SEER سرطانها را بر اساس مراحل FIGO یا AJCC TNM (مرحله 1، مرحله 2، مرحله 3 و غیره) گروه بندی نمیکند. در عوض این پایگاه سرطانها را به مراحل موضعی، منطقه ای و دور دسته بندی میکند:
- موضعی (Localized): هیچ نشانه ای از گسترش سرطان به خارج از رحم وجود ندارد.
- منطقه ای (Regional): سرطان از رحم به ساختارها یا غدد لنفاوی مجاور گسترش یافته است.
- دور (Distant): سرطان به نقاط دورتر بدن مانند ریهها، کبد یا استخوانها گسترش یافته است.
نرخ بقای نسبی 5 ساله برای سرطان آندومتر
(این اعداد بر اساس اطلاعات بدست آمده از افرادی است که بین سالهای 2011 تا 2017 مبتلا به سرطان آندومتر تشخیص داده شدهاند.)
درک اعداد
- این اعداد فقط برای مرحله سرطان در هنگام اولین تشخیص صدق میکنند. اگر سرطان رشد کند، گسترش یابد یا پس از درمان عود کند، دیگر اعمال نمیشوند.
- این اعداد همه چیز را در نظر نمیگیرند. میزان بقا بر اساس میزان گسترش سرطان گروه بندی میشود اما سن، سلامت کلی، میزان واکنش سرطان به روند درمان و سایر عوامل نیز بر وضعیت شما تأثیر میگذارند.
- زنانی که اکنون مبتلا به سرطان آندومتر تشخیص داده میشوند، ممکن است چشم انداز بهتری نسبت به این اعداد داشته باشند. درمانها با گذشت زمان بهبود مییابند و این اعداد بر اساس اطلاعات زنانی است که حداقل پنج سال زودتر تشخیص داده شده و درمان شده اند.
سرطان آندومتر چگونه درمان میشود؟
جراحی (Surgery) برای سرطان آندومتر
جراحی اغلب روش درمانی اصلی سرطان آندومتر است و شامل هیسترکتومی، اغلب همراه با سالپنگو اوفورکتومی (salpingo-oophorectomy) و برداشتن غدد لنفاوی است. در برخی موارد، شستشوی لگن انجام شده، امنتوم (omentum) برداشته شده و یا بیوپسی صفاقی (peritoneal biopsy) انجام میشود. اگر سرطان در سراسر لگن و شکم (belly) گسترش یافته باشد، ممکن است یک روش توده زدایی (debulking procedure، حذف حد الامکان سرطان) انجام شود. در ادامه به تفصیل به این موارد پرداخته شده است.

هیسترکتومی
انواع هیسترکتومی
روش درمانی اصلی سرطان آندومتر، جراحی برای خارج کردن رحم و دهانه رحم است. این عمل هیسترکتومی (hysterectomy) نامیده میشود. هنگامی که رحم از طریق یک برش (incision) در شکم برداشته میشود، این عمل هیسترکتومی ساده (simple abdominal hysterectomy) یا کامل شکم (total abdominal hysterectomy) نامیده میشود.
اگر رحم از طریق واژن برداشته شود، به آن هیسترکتومی واژینال (vaginal hysterectomy) میگویند. این روش ممکن است یک گزینه برای زنانی باشد که برای سایر انواع جراحی از سلامت کافی برخوردار نیستند.
هنگامی که سرطان آندومتر به دهانه رحم یا ناحیه اطراف دهانه رحم (به نام پارامتریوم یا parametrium) گسترش یافته است، هیسترکتومی رادیکال (radical hysterectomy) انجام میشود. در این عمل تمام رحم، بافتهای کنار رحم (پارامتریوم و رباطهای رحمی خاجی) و قسمت بالایی واژن (کنار دهانه رحم) برداشته میشود. این عمل اغلب از طریق شکم انجام میشود اما میتوان آن را از طریق واژن نیز انجام داد.
جراحیهایی که همراه با هیسترکتومی انجام میشوند
در هنگام درمان سرطان آندومتر، برداشتن رحم و نه تخمدانها نادر است. (با این حال، ممکن است در موارد خاصی برای زنانی که پیش از زمان یائسگی خود هستند نیز انجام شود.) برداشتن تخمدانها و لولههای فالوپ را سالپنگو اوفورکتومی دوطرفه (bilateral salpingo-oophorectomy یا BSO) مینامند. در واقع این کار بخشی از هیسترکتومی نیست. این یک روش جداگانه است که در طی همان عمل انجام میشود.
برای تصمیم گیری در مورد تعیین مرحله سرطان، غدد لنفاوی موجود در لگن و اطراف آئورت نیز باید برداشته شوند. به این عمل دیسکسیون غدد لنفاوی (lymph node dissection) میگویند.
میتوان این کار را از طریق همان برش هیسترکتومی شکمی انجام داد. اگر هیسترکتومی به صورت واژینال انجام شود، غدد لنفاوی را میتوان با جراحی لاپاراسکوپی (laparoscopic surgery) برداشت. (به مبحث «جراحی غدد لنفاوی» در ادامه مراجعه کنید.)
هیسترکتومی چگونه انجام میشود؟
همان طور که در بالا ذکر شد، این جراحی را میتوان از طریق یک برش بزرگ در شکم انجام داد. این عمل از طریق واژن نیز قابل انجام است. جراحی لاپاراسکوپی یا جراحی کم تهاجمی گزینه دیگری است که موارد انجام آن رو به افزایش است.
لاپاراسکوپی تکنیکی است که به جراح اجازه میدهد داخل شکم و لگن را از طریق لولههای باریکی که از طریق برشهای بسیار کوچک ایجاد شده در شکم وارد میشوند، ببیند. ابزارهای جراحی بلند و ریز را میتوان از طریق لولهها کنترل کرد. این کار به جراح اجازه میدهد بدون ایجاد برش بزرگ در شکم عمل را انجام دهد. این روش با داشتن درد و از دست دادن خون کمتر مرتبط است و میتواند زمان بهبودی پس از جراحی را نیز کوتاه کند.
هم هیسترکتومی ساده و هم هیسترکتومی رادیکال را میتوان از طریق شکم با استفاده از جراحی لاپاراسکوپی انجام داد. همچنین ممکن است از جراحی لاپاراسکوپی برای کمک به برداشتن ایمن سایر اندامها و بافتها هنگام انجام هیسترکتومی واژینال استفاده شود.
به نظر میرسد که جراحی لاپاراسکوپی برای سرطان آندومتر به همان اندازه روشهای باز سنتیتر برای بیمار مناسب است، اگر که توسط جراحی انجام شود که تجربه زیادی در جراحیهای سرطان لاپاراسکوپی دارد.
رویکرد رباتیک به طور فزاینده ای برای انجام روشهای لاپاراسکوپی مورد استفاده قرار میگیرد و نتایج تقریباً یکسان است. در جراحی رباتیک، جراح روی یک پنل کنترل در اتاق عمل مینشیند و بازوهای رباتیک را حرکت میدهد تا از طریق ایجاد برشهای کوچک عمل را انجام دهد. جراحیهای رباتیک نسبت به جراحیهای لاپاراسکوپی معمولی مدت زمان بیشتری طول میکشند.
برای هر یک از این روشها، از بیهوشی عمومی استفاده میشود تا بیمار در خواب عمیق باشد و در حین عمل احساس درد نکند.
سالپنگو اوفورکتومی دوطرفه (Bilateral salpingo-oophorectomy)
در این عمل هم لولههای فالوپ و هم هر دو تخمدان برداشته میشود. این روش معمولاً همزمان با برداشتن رحم (چه با هیسترکتومی ساده یا هیسترکتومی رادیکال) برای درمان سرطان آندومتر انجام میشود. برداشتن هر دو تخمدان به این معنی است که اگر قبلاً یائسه نشده باشید، یائسه خواهید شد.
اگر کمتر از 45 سال سن و سرطان آندومتر مرحله اول دارید، ممکن است بخواهید با جراح خود در مورد حفظ تخمدان خود صحبت کنید. حتی با وجود این که زنانی که تخمدانهایشان برداشته میشود، احتمال کمتری برای بازگشت سرطان دارند اما به نظر نمیرسد که برداشتن تخمدانها به آنها کمک کند تا عمر طولانیتری داشته باشند.
جراحی غدد لنفاوی (Lymph node surgery)
تشریح غدد لنفاوی لگنی و پارا آئورت عملی است که برای برداشتن غدد لنفاوی از لگن و ناحیه کنار آئورت انجام میشود. این گرهها برای بررسی اینکه آیا حاوی سلولهای سرطانی هستند که از تومور آندومتر گسترش یافته باشد، آزمایش میشوند. این اطلاعات بخشی از یافتن مرحله جراحی سرطان است.
زمانی که اکثر یا تمام غدد لنفاوی آن ناحیه برداشته شوند، عمل جراحی را دیسکسیون غدد لنفاوی (lymph node dissection) مینامند. این کار معمولاً همزمان با عمل برداشتن رحم (هیسترکتومی) انجام میشود. اگر هیسترکتومی شکمی انجام میدهید، غدد لنفاوی را نیز میتوان از طریق همان برش برداشت. در زنانی که هیسترکتومی واژینال انجام داده اند، غدد لنفاوی ممکن است با جراحی لاپاراسکوپی برداشته شوند.
هنگامی که تنها تعداد کمی از غدد لنفاوی در یک ناحیه برداشته میشود، به آن نمونه برداری از غدد لنفاوی (lymph node sampling) میگویند.
بسته به نوع و درجه سرطان، میزان سرطان در رحم (اندازه تومور)، و میزان نفوذ سرطان به عضله رحم و نتایج آزمایش تصویر برداری، ممکن است نیازی به برداشتن غدد لنفاوی نباشد.
نقشه برداری غدد لنفاوی نگهبان (Sentinel lymph node mapping)
اگر آزمایشهای تصویر برداری به وضوح نشانههایی از گسترش سرطان به غدد لنفاوی لگن شما را نشان ندهند، میتوان از نقشه برداری غدد لنفاوی نگهبان (SLN) برای سرطان آندومتر در مراحل اولیه استفاده کرد. برای انجام این کار، رنگ آبی یا سبز به ناحیه سرطانی، نزدیک دهانه رحم تزریق میشود. سپس جراح به دنبال غدد لنفاوی که آبی یا سبز میشوند (در اثر وجود رنگ)، میگردد. این غدد لنفاوی همانهایی هستند که سرطان ابتدا به آنها وارد میشود (گرههای نگهبان). آنها برداشته شده و آزمایش میشوند تا بررسی کنند آیا سلولهای سرطانی در آنها وجود دارد یا خیر. اگر چنین باشد، غدد لنفاوی بیشتری خارج میشوند زیرا احتمالاً سلولهای سرطانی در آنها نیز وجود دارد. اگر سلولهای سرطانی در گرههای نگهبان وجود نداشته باشند، گره دیگری برداشته نمیشود. این روش معمولاً همزمان با جراحی برداشتن رحم (هیسترکتومی) انجام میشود. پزشک با شما در مورد اینکه آیا نقشه برداری SLN گزینه مناسبی برای شماست یا خیر، صحبت خواهد کرد.
شستشوی لگن (Pelvic washings، شستشوی صفاقی یا peritoneal lavage)
در این روش، جراح حفرههای شکم و لگن را با آب نمک (سالین) شستشو میدهد. سپس مایع جمع آوری میشود (با استفاده از مکش) و به آزمایشگاه فرستاده میشود تا بررسی کنند که آیا حاوی سلولهای سرطانی است یا خیر. به این روش شستشوی صفاقی (peritoneal lavage) نیز میگویند. اگر سلولهای سرطانی آندومتر در مایع وجود داشته باشند، مرحله سرطان ممکن است تغییر کند (مرحله جراحی) و مراحل بعدی روند درمانی نیز ممکن است تحت تاثیر قرار گیرد.
روشهای دیگری که ممکن است برای بررسی گسترش سرطان استفاده شود
Omentectomy: امنتوم (omentum) لایه ای از بافت چربی است که محتویات شکم را به نوعی مانند یک پیش بند میپوشاند. سرطان گاهی به این بافت نیز سرایت میکند. هنگامی که این بافت طی یک عمل از بدن خارج میشود، به آن اومنتکتومی (omentectomy) میگویند.
اگر سرطان در آن جا گسترش یافته باشد، ممکن است این کار در طول هیسترکتومی انجام شود. بیوپسی از امنتوم نیز ممکن است برای بررسی گسترش سرطان انجام شود. (تکههای کوچک خارج شده و برای بررسی وجود سلولهای سرطانی آزمایش میشوند.)
بیوپسی صفاقی (Peritoneal biopsies): به بافت پوشاننده لگن و شکم، صفاق (peritoneum) میگویند. بیوپسی صفاقی قطعات کوچکی از این پوشش را برای بررسی سلولهای سرطانی جدا میکند.
حجم زدایی تومور (Tumor debulking)
اگر سرطان در سراسر شکم گسترش یافته باشد، جراح ممکن است سعی کند تا حد امکان تومور را خارج کند. به این عمل debulking میگویند. کاهش حجم توده سرطانی میتواند به روندهای درمانی دیگر مانند پرتو درمانی یا شیمی درمانی کمک کند تا بهتر عمل کنند. بنابراین، ممکن است در درمان برخی از انواع سرطان آندومتر مفید باشد.
بهبودی پس از جراحی
مدت زمان بستری شدن در بیمارستان برای هیسترکتومی شکمی معمولاً 3 تا 7 روز است. میانگین مدت بستری شدن در بیمارستان پس از هیسترکتومی رادیکال شکمی حدود 5 تا 7 روز است. بهبودی کامل ممکن است تا 4 تا 6 هفته طول بکشد. روش لاپاراسکوپی و هیسترکتومی واژینال معمولاً برای بهبودی نیاز به بستری شدن در بیمارستان 1 یا 2 روزه و بهبودی کامل 2 تا 3 هفتگی دارند. عوارض این جراحیها شایع نیست و به روش جراحی بستگی دارد. این عوارض شامل آسیب عصبی یا عروقی، خونریزی بیش از حد، عفونت زخم، لخته شدن خون و آسیب به بافتهای مجاور (سیستمهای ادراری و روده) هستند.
هیسترکتومی رادیکال بر اعصاب کنترل کننده مثانه تأثیر میگذارد، بنابراین از کاتتر (catheter) برای تخلیه ادرار بلافاصله پس از جراحی استفاده میشود. اغلب این قطعه حداقل برای چند روز در بدن نگهداری میشود. اگر پس از برداشتن کاتتر، مثانه به طور کامل بهبود نیافته باشد، ممکن است دوباره داخل این اندان قرار داده شود. گزینه دیگر این است که به شما نشان داده میشود که چگونه خودتان چند بار در روز کاتتر بگذارید تا مثانه خود را تخلیه کنید. با گذشت زمان، عملکرد مثانه باز میگردد.
عوارض جانبی جراحی
هر گونه هیسترکتومی باعث ناباروری میشود (شما دیگر نمیتوانید باردار شوید).
برای زنانی که قبل از جراحی دچار یائسگی نشده بودند، برداشتن تخمدانها بلافاصله باعث یائسگی میشود. این پدیده میتواند منجر به بروز علائمی مانند گر گرفتگی، تعریق شبانه و خشکی واژن شود. این وضعیت در دراز مدت، میتواند منجر به پوکی استخوان و افزایش خطر ابتلا به بیماری قلبی شود که همه زنان یائسه را تحت تاثیر قرار میدهد.
برداشتن غدد لنفاوی در لگن میتواند منجر به تجمع مایع در پاها و اندام تناسلی شود. این امر میتواند به یک مشکل مادام العمر به نام ادم لنف (lymphedema) تبدیل شود. اگر بعد از جراحی به شما پرتو نیز داده شود، احتمال بیشتری برای ایجاد این عارضه وجود دارد.
جراحی و علائم یائسگی نیز میتوانند بر زندگی جنسی شما تأثیر بگذارند.
با تیم درمانی خود در مورد عوارض جانبی که ممکن است بلافاصله بعد از جراحی و یا مدتها بعد از آن داشته باشید، صحبت کنید. ممکن است کارهایی وجود داشته باشد که بتوانید برای جلوگیری از بروز عوارض جانبی انجام دهید. بهتر است بدانید که چه انتظاری باید از وضعیت خود داشته باشید تا بتوانید فورا کمک بگیرید.
پرتو درمانی (Radiation Therapy) برای سرطان آندومتر
پرتو درمانی از پرتوهای پرانرژی (مانند اشعه ایکس) برای از بین بردن سلولهای سرطانی استفاده میکند. برای درمان سرطان آندومتر میتوان آن را به دو روش تجویز کرد:
- با قرار دادن مواد رادیو اکتیو در داخل بدن. به این روش پرتو درمانی داخلی (internal radiation therapy) یا براکی تراپی (brachytherapy) میگویند.
- با استفاده از دستگاهی که پرتوهای تشعشعی را روی تومور متمرکز میکند، دقیقاً مانند عکس برداری با اشعه ایکس. به این روش پرتو درمانی خارجی (external beam radiation therapy) میگویند.
در برخی موارد هم از براکی تراپی و هم از پرتو درمانی خارجی استفاده میشود. برای انجام این کار، معمولاً ابتدا تابش پرتو خارجی و سپس براکی تراپی به فرد داده میشود. مرحله و درجه سرطان برای کمک به تصمیم گیری در مورد مناطقی که باید با پرتو درمانی درمان شوند و انتخاب نوع پرتو درمانی استفاده میشود.
پرتو درمانی اغلب بعد از جراحی برای درمان سرطان آندومتر استفاده میشود. این کار میتواند هر سلول سرطانی را که ممکن است هنوز در ناحیه تحت درمان باشد از بین ببرد. اگر برنامه درمانی شما شامل پرتو دهی بعد از جراحی باشد، قبل از شروع پرتو درمانی به شما فرصت داده میشود تا بهبود پیدا کنید. اغلب، برای بهبودی حداقل 4 تا 6 هفته مورد نیاز است.
در موارد دیگری، ممکن است قبل از جراحی برای کمک به کوچک کردن تومور پرتو داده شود تا برداشتن آن آسانتر شود.
زنانی که از سلامت کافی برای جراحی برخوردار نیستند ممکن است به عنوان دوره درمانی اصلی خود رادیو تراپی را دریافت کنند.
براکی تراپی (Brachytherapy)
زنانی که رحم (و دهانه رحم) خود را برداشته اند، ممکن است قسمت بالایی واژن را با براکی تراپی درمان کنند. به این روش براکی تراپی واژینال (vaginal brachytherapy) میگویند. یک منبع تشعشعی (یک ماده رادیو اکتیو) در یک سیلندر (که اپلیکاتور – applicator – نامیده میشود) قرار گرفته و سپس سیلندر داخل واژن قرار میگیرد. (بسیار شبیه قرار گرفتن یک تامپون محکم درون واژن است.) اندازه سیلندر و میزان تشعشع در آن به شرایط بیمار بستگی دارد. قسمت بالایی واژن، نزدیک ترین قسمت به رحم، همیشه درمان میشود. با براکی تراپی، پرتوها عمدتاً ناحیه واژن را که در تماس با سیلندر است، تحت تأثیر قرار میدهند. ساختارهای مجاور مانند مثانه و راست روده کمتر در معرض تابش قرار میگیرند.
این روش در بخش پرتو درمانی بیمارستان یا مرکز پرتو درمانی انجام میشود. 2 نوع براکی تراپی برای سرطان آندومتر استفاده میشود، نرخ با دوز کم (low-dose rate یا LDR) و نرخ با دوز بالا (high-dose rate یا HDR).
- در براکی تراپی LDR، اپلیکاتور با منبع تشعشع موجود در آن حدود 1 تا 4 روز در بدن باقی میماند. بیمار باید بی حرکت باشد تا اپلیکاتور در طول درمان حرکت نکند، بنابراین معمولاً باید در طول درمان در بیمارستان بماند.
از آن جایی که بیمار باید بی حرکت بماند، این شکل از براکی تراپی خطر لخته شدن خون در پاها به شکل جدی (به نام ترومبوز وریدی عمقی یا DVT یا deep venous thrombosis) را به همراه دارد. LDR معمولاً در ایالات متحده استفاده نمیشود.
- در براکی تراپی HDR، تابش قوی تر است. هر درمان زمان بسیار کوتاهی (معمولاً کمتر از یک ساعت) طول میکشد و تابش فقط 10 تا 20 دقیقه است. اپلیکاتور تنها زمانی در محل قرار میگیرد که درمان انجام شود. شما میتوانید همان روز به خانه بروید. برای سرطان آندومتر، براکی تراپی HDR ممکن است به صورت هفتگی یا حتی روزانه برای حداقل 3 دوز انجام شود.
شایع ترین عارضه جانبی تغییر در پوشش واژن است. (که واژینیت پرتویی – radiation vaginitis – نامیده میشود. این موضوع در ادامه و در بخش عوارض جانبی با جزئیات بیشتر مورد بحث قرار گرفته است). در صورت وجود درد میتوان داروهایی را برای تحمل درد در هنگام وجود اپلیکاتور در واژن مصرف کرد.
پرتو درمانی خارجی (External beam radiation therapy)
در این نوع درمان پرتو از منبعی خارج از بدن ارسال میشود.
پرتو درمانی خارجی اغلب 5 روز در هفته به مدت 4 تا 6 هفته انجام میشود. پوستی که ناحیه درمان را میپوشاند با جوهری دائمی یا نشانههای ریز به دقت مشخص میشود. یک قالب مخصوص لگن و کمر به صورت سفارشی برای شما ساخته میشود تا مطمئن شوند که شما در هر دوره درمانی دقیقاً در همان موقعیت قرار دارید. هر دوره درمانی کمتر از نیم ساعت طول میکشد اما مراجعه روزانه به مرکز پرتو درمانی لازم است.
گاهی اوقات شیمی درمانی همراه با اشعه برای کمک به عملکرد بهتر آن انجام میشود. به این عمل شیمی پرتویی (chemoradiation) میگویند.
عوارض جانبی پرتو درمانی
عوارض جانبی کوتاه مدت
عوارض جانبی رایج پرتو درمانی شامل خستگی، ناراحتی معده یا اسهال است. خستگی شدید که ممکن است تا حدود 2 هفته پس از شروع روند درمانی شروع نشود نیز شایع است. اسهال رایج است اما معمولاً با داروهای بدون نسخه قابل کنترل است. حالت تهوع و استفراغ ممکن است رخ دهد اما اینها نیز با دارو قابل درمان اند. این عوارض جانبی با دریافت پرتوهای خارجی بیشتر از براکی تراپی رایج هستند.
هنگامی که شیمی درمانی همراه با پرتو درمانی انجام میشود، عوارض جانبی بدتر میشود.
تغییرات پوستی که میتواند از قرمزی خفیف تا پوسته پوسته شدن و ایجاد تاول متغیر باشند، بسیار رایج هستند. پوست ممکن است مایعی را آزاد کند که میتواند منجر به عفونت شود، بنابراین باید مراقب تمیز کردن و محافظت از ناحیه در معرض اشعه باشید. گاهی اوقات، با بهبودی، پوست در ناحیه تحت درمان تیرهتر یا غیر انعطاف پذیرتر (سختتر) میشود.
اشعه میتواند مثانه را تحریک کند و ممکن است در ادرار کردن مشکل داشته باشید. تحریک مثانه که سیستیت پرتویی (radiation cystitis) نامیده میشود، میتواند منجر به بروز ناراحتی، خون در ادرار و میل به ادرار مکرر شود.
تشعشع همچنین میتواند باعث تحریک در روده شود. تحریک یا خونریزی مقعدی را پروکتیت پرتویی (radiation proctitis) مینامند. گاهی اوقات این عارضه با تنقیه (enemas) حاوی استروئید (مانند هیدروکورتیزون یا hydrocortisone) یا شیافهای حاوی یک ضد التهاب درمان میشود.
تشعشع میتواند واژن را تحریک کند و منجر به ناراحتی و ترشح شود. این عارضه واژینیت پرتویی (radiation vaginitis) نامیده میشود. در صورت بروز، پزشک ممکن است دوش و شست وشوی واژن همراه با محلول رقیق پراکسید هیدروژن را توصیه کند. هنگامی که تحریک شدید باشد، زخمهای بازی در واژن ایجاد میشوند که ممکن است نیاز به درمان با کرم استروژن (estrogen cream) داشته باشند.
تشعشع همچنین میتواند منجر به کاهش شمارش خون و ایجاد کم خونی (میزان گلبول قرمز پایین) و لکوپنی (leukopenia، میزان گلبول سفید پایین) شود. شمارش خون معمولاً در عرض چند هفته پس از قطع پرتو درمانی به حالت عادی بر میگردد.
عوارض جانبی طولانی مدت
پرتو درمانی ممکن است باعث ایجاد تغییراتی در پوشش داخلی واژن شود که منجر به خشکی واژن میشوند. این امر پس از براکی تراپی واژینال نسبت به پرتو درمانی لگنی شایع تر است. در برخی موارد بافت اسکار (جای زخم) میتواند در واژن ایجاد شود. بافت اسکار میتواند واژن را کوتاهتر یا باریکتر کند (به نام تنگی واژن) که میتواند رابطه جنسی (ورود به واژن) را دردناک کند. یک زن میتواند با کشیدن دیوارههای واژن خود برای چندین بار در هفته از ایجاد این مشکل جلوگیری کند.
این کار را میتوان با داشتن رابطه جنسی برای 3 تا 4 بار در هفته یا با استفاده از گشاد کننده واژن (یک لوله پلاستیکی یا لاستیکی که برای کشش واژن استفاده میشود) انجام داد. با این حال، خشکی واژن و درد هنگام رابطه جنسی میتواند از عوارض جانبی طولانی مدت پرتو درمانی باشد. برخی از مراکز دارای فیزیوتراپیستهایی هستند که در درمان مشکلات موجود در کف لگن تخصص دارند که میتواند به درمان این علائم موجود در واژن و گاهی اوقات بهبود عملکرد جنسی کمک کند. اگر این مشکلات شما را آزار میدهد، در این مورد از پزشک خود سوال کنید.
تشعشعات لگنی میتواند به تخمدانها آسیب برساند و در نتیجه یائسگی زودرس ایجاد شود. این موضوع برای اکثر زنانی که برای سرطان آندومتر تحت درمان قرار میگیرند مشکلی را ایجاد نمیکند زیرا آنها قبلاً یائسه شده اند، چه به طور طبیعی چه در نتیجه جراحی برای درمان سرطان (هیسترکتومی و برداشتن تخمدانها).
پرتو درمانی لگنی همچنین میتواند منجر به بروز انسداد شود که مانع از تخلیه مایع از پاها میگردد. این پدیده میتواند منجر به تورم شدید، به نام ادم لنف شود. ادم لنف یک عارضه جانبی طولانی مدت است. این عارضه پس از قطع دوره تابش از بین نمیرود. در واقع ممکن است چندین ماه یا حتی سالها پس از پایان درمان نیز ایجاد نشود.
اگر غدد لنفاوی لگن در طی جراحی برای برداشتن سرطان برداشته شوند، این عارضه جانبی بیشتر رایج است. فیزیوتراپیستهای تخصصی وجود دارند که میتوانند به درمان این مشکل کمک کنند. در صورت بروز آن مهم است که فوراً روند درمان را شروع کنید.
تابش به لگن میتواند استخوانها را ضعیف کند و منجر به شکستگی لگنی شود. این مسئله مهم است که زنانی که سرطان آندومتر داشته اند در صورت داشتن درد لگن فوراً با پزشک خود تماس بگیرند. چنین دردی ممکن است ناشی از شکستگی، سرطان عود کرده (سرطانی که پس از درمان عود میکند) یا سایر شرایط جدی باشد.
تابش لگن همچنین میتواند منجر به ایجاد مشکلات طولانی مدت مثانه (سیستیت پرتویی) یا روده (پروکتیت پرتویی) شود. به ندرت، آسیب اشعه به روده میتواند باعث انسداد (به نام obstruction) یا ایجاد یک اتصال غیر طبیعی بین روده و واژن یا پوست خارجی شود (به نام فیستول یا fistula). این شرایط ممکن است نیاز به درمان با جراحی داشته باشند.
اگر عوارض جانبی ناشی از پرتو درمانی را دارید، آنها را با پزشک خود در میان بگذارید. کارهایی وجود دارد که میتوانید برای تسکین این علائم یا جلوگیری از بروز آنها انجام دهید.
شیمی درمانی (Chemotherapy) برای سرطان آندومتر
شیمی درمانی (chemo) استفاده از داروهایی است که سلولهای سرطانی را از بین میبرند. آنها به رگ تزریق شده یا از طریق دهان و به عنوان قرص مصرف میشوند. این داروها وارد جریان خون میشوند و به تمام بدن میرسند. به همین دلیل، زمانی که سرطان آندومتر فراتر از آندومتر به سایر قسمتهای بدن گسترش یافته و جراحی انجام نمیشود، شیمی درمانی اغلب بخشی از روند درمان است.
همچنین این روش معمولاً برای سرطانهای درجه بالا که به سرعت رشد میکنند و گسترش مییابند و سرطانهایی که پس از درمان عود کرده اند نیز استفاده میشود.
شیمی درمانی برای درمان سرطان آندومتر مرحله I و II استفاده نمیشود.
در بیشتر موارد، ترکیبی از داروهای شیمی درمانی استفاده میشود. شیمی درمانی ترکیبی نسبت به مصرف یک دارو به تنهایی بهتر عمل میکند.
شیمی درمانی اغلب به صورت چرخه ای تجویز میشود: یک دوره درمان و به دنبال آن یک دوره استراحت. داروهای شیمی درمانی ممکن است در یک یا چند روز در هر چرخه تجویز شوند.
داروهای شیمی درمانی مورد استفاده برای درمان سرطان آندومتر ممکن است شامل موارد زیر باشد:
- پاکلیتاکسل (Taxol یا Paclitaxel)
- کربوپلاتین (Carboplatin)
- دوکسوروبیسین (Adriamycin یا Doxorubicin) یا دوکسوروبیسین لیپوزومی (Doxil یا liposomal doxorubicin)
- سیس پلاتین (Cisplatin)
- Docetaxel (Taxotere)

اغلب، 2 یا چند دارو برای دوره درمان با یکدیگر ترکیب میشوند. رایج ترین ترکیبات شامل کربوپلاتین/پاکلیتاکسل و سیس پلاتین/دوکسوروبیسین است. در موارد کمتر رایج ممکن است از کربوپلاتین/دوستاکسل و سیس پلاتین/پکلیتاکسل/دوکسوروبیسین نیز استفاده شود.
برای کارسینوسارکوم، داروی شیمی درمانی ایفوسفامید (Ifex یا ifosfamide) اغلب به تنهایی یا همراه با سیس پلاتین یا پاکلیتاکسل استفاده میشود. داروی هدفمند به نام تراستوزوماب (Herceptin یا trastuzumab) ممکن است برای کارسینوسارکومهایی که HER2 مثبت هستند، اضافه شود. (HER2 پروتئینی است که به رشد و گسترش سریع تر برخی از سلولهای سرطانی کمک میکند. میتوانید در مورد آن در مبحث وضعیت سرطان پستان HER2 اطلاعات بیشتری کسب کنید.)
گاهی اوقات شیمی درمانی برای چند سیکل و به دنبال آن پرتو درمانی داده میشود. سپس دوباره شیمی درمانی داده میشود. به این روش sandwich therapy میگویند. این روش گاهی اوقات برای سرطان سروزی پاپیلاری آندومتر و کارسینوسارکوم رحم استفاده میشود.
یکی دیگر از گزینههای درمانی، دادن شیمی درمانی همراه با اشعه (به نام کمورادیشن یا شیمی پرتویی یا chemoradiation) است. شیمی درمانی میتواند به عملکرد بهتر پرتو درمانی کمک کند اما ممکن است برای بیمار سخت تر باشد زیرا این ترکیب باعث بروز عوارض جانبی بیشتری میشود.
عوارض جانبی شیمی درمانی
این داروها سلولهای سرطانی را از بین میبرند اما میتوانند به برخی از سلولهای طبیعی نیز آسیب برسانند که به نوبه خود عوارض جانبی ایجاد میکند. عوارض جانبی شیمی درمانی به داروهای مورد استفاده، مقدار مصرف و مدت زمان درمان بستگی دارد. عوارض جانبی رایج عبارتند از:
- تهوع و استفراغ
- از دست دادن اشتها
- زخمهای دهانی
- زخمهای واژنی
- ریزش مو
همچنین، بیشتر داروهای شیمی درمانی میتوانند به سلولهای تولید کننده خون مغز استخوان نیز آسیب بزنند. این پدیده میتواند منجر به کاهش تعداد سلولهای خونی شود، مانند:
- گلبولهای سفید پایین که خطر ابتلا به عفونت را افزایش میدهد.
- تعداد کم پلاکتها که میتواند باعث بروز خونریزی یا کبودی پس از بریدگیها یا جراحات جزئی شود.
- گلبولهای قرمز پایین (کم خونی) که میتواند باعث مشکلاتی مانند خستگی و تنگی نفس شود.
اکثر عوارض جانبی شیمی درمانی با گذشت زمان و پس از پایان دوره درمانی بهتر میشوند اما برخی از آنها میتوانند برای مدت طولانی ادامه داشته باشند. داروهای مختلف میتوانند عوارض جانبی مختلفی را ایجاد کنند. به عنوان مثال، دوکسوروبیسین میتواند به مرور زمان به عضله قلب آسیب برساند. با افزایش دوز کل دارو، احتمال آسیب قلبی افزایش مییابد، بنابراین پزشکان برای دریافت دوکسوروبیسین محدودیتهایی را تعیین میکنند.
سیس پلاتین میتواند باعث آسیب کلیه شود، بنابراین قبل و بعد از شیمی درمانی به شما مایعات زیادی به شکل IV تزریق میشود تا به محافظت از کلیهها کمک کند. سیس پلاتین و پاکلیتاکسل هر دو میتوانند باعث آسیب عصبی (به نام نوروپاتی یا neuropathy) شوند. این عارضه میتواند منجر به بی حسی، سوزن سوزن شدن یا حتی درد در دستها و پاها شود.
ایفوسفامید میتواند به پوشش مثانه آسیب برساند و باعث خونریزی آن شود (به نام سیستیت هموراژیک یا hemorrhagic cystitis). برای جلوگیری از بروز این امر، ممکن است همراه با شیمی درمانی به شما مقادیر زیادی مایعات و دارویی به نام مسنا (mesna) به شکل IV داده شود.
قبل از شروع شیمی درمانی، حتما در مورد داروها و عوارض جانبی احتمالی آنها با تیم مراقبت پزشکی خود صحبت کنید.
اگر در حین شیمی درمانی عوارض جانبی داشتید، به یاد داشته باشید که راههایی برای پیشگیری یا درمان بیشتر آنها وجود دارد. به عنوان مثال، بسیاری از داروهای ضد تهوع وجود دارند که میتوانند به پیشگیری یا کاهش تهوع و استفراغ کمک کنند. حتماً هر گونه عوارض جانبی را به تیم مراقبتهای پزشکی خود اطلاع دهید. درمان فوری آنها اغلب از بدتر شدن آنها جلوگیری میکند.
هورمون درمانی (Hormone Therapy) برای سرطان آندومتر
در این نوع روش درمانی از هورمونها یا داروهای مسدود کننده هورمون برای درمان سرطان استفاده میشود. این روش مشابه هورمون درمانی نیست که برای کاهش علائم یائسگی (هورمون درمانی یائسگی یا menopausal hormone therapy) انجام میشود.
این روش اغلب برای درمان سرطان آندومتر که پیشرفته است (مرحله III یا IV) یا سرطانی که پس از درمان بازگشته است (عود کرده است) استفاده میشود. هورمون درمانی اغلب همراه با شیمی درمانی استفاده میشود.
درمان هورمونی برای سرطان آندومتر میتواند شامل موارد زیر باشد:
- پروژستینها (Progestins، این اصلی ترین درمان هورمونی مورد استفاده است.)
- تاموکسیفن (Tamoxifen)
- آگونیستهای هورمون آزاد کننده هورمون لوتئینه کننده (آگونیستهای LHRH یا Luteinizing hormone-releasing hormone agonists)
- مهارکنندههای آروماتاز ( Aromatase inhibitors یا AIs)
در حال حاضر، هیچ نوع درمان هورمونی که بهترین روش درمانی برای سرطان آندومتر باشد، یافت نشده است.
پروژستینها (Progestins)
روش درمان هورمونی اصلی برای سرطان آندومتر از پروژسترون یا داروهایی مانند آن (به نام پروژستین) استفاده میکند. 2 نوع از رایج ترین پروژستینهای مورد استفاده عبارتند از:
- مدروکسی پروژسترون استات (Provera یا Medroxyprogesterone acetate) که میتواند به صورت تزریقی یا به شکل قرص به بیمار داده شود.
- مژسترول استات (Megace یا Megestrol acetate) که به صورت قرص یا مایع داده میشود.
این داروها رشد سلولهای سرطانی آندومتر را کند میکنند. مشخص شده است که آنها در درمان زنان مبتلا به سرطان آندومتر که میخواهند در آینده باردار شوند مفید هستند و این یک حوزه مورد علاقه تحقیقاتی برای محققان است.
عوارض جانبی میتواند شامل موارد زیر باشد:
- گر گرفتگی
- تعریق شبانه
- افزایش وزن (ناشی از احتباس مایعات و افزایش اشتها)
- بدتر شدن افسردگی
- افزایش سطح قند خون در زنان مبتلا به دیابت
- لخته شدن خون به شکل جدی (این عارضه نادر است)
گاهی اوقات هیپرپلازی آندومتر و سرطانهای اولیه آندومتر را میتوان با یک دستگاه داخل رحمی (IUD) که حاوی پروژستینی به نام لوونورژسترل (levonorgestrel) است، درمان کرد. این دارو ممکن است با یک داروی هورمونی دیگر مانند مدروکسی پروژسترون استات یا آگونیست هورمون آزاد کننده هورمون لوتئین کننده ترکیب شود.
تاموکسیفن (Tamoxifen)
تاموکسیفن یک داروی ضد استروژن است که اغلب برای درمان سرطان سینه استفاده میشود. این دارو همچنین ممکن است برای درمان سرطان پیشرفته یا عود کننده آندومتر نیز استفاده شود. جایگزینی پروژسترون و تاموکسیفن گزینه ای است که به نظر میرسد خوب عمل کند و بهتر از پروژسترون به تنهایی توسط بیمار تحمل شود.
هدف از درمان با تاموکسیفن این است که هر گونه استروژن در بدن زن را از افزایش رشد سلولهای سرطانی دور نگه دارد. اگرچه تاموکسیفن ممکن است استروژن را از “تغذیه” سلولهای سرطانی باز دارد اما مانند یک استروژن ضعیف در سایر قسمتهای بدن عمل میکند.
این دارو باعث تحلیل استخوان نمیشود اما میتواند باعث گر گرفتگی و خشکی واژن شود. زنانی که تاموکسیفن مصرف میکنند نیز در معرض خطر بیشتری برای لخته شدن خون در پاها هستند.
آگونیستهای هورمون آزاد کننده هورمون لوتئینه کننده (Luteinizing hormone-releasing hormone agonists)
اکثر زنان مبتلا به سرطان آندومتر در بخشی از روند درمان خود، تخمدانهای خود را برداشته اند. برخی از زنان ممکن است تحت پرتو درمانی قرار داشته باشند که تخمدانهای آنها را غیر فعال کرده است. این پدیده به جلوگیری از تولید استروژن در بدن کمک میکند و همچنین ممکن است رشد سرطان را کاهش دهد.
آگونیستهای هورمون آزاد کننده هورمون لوتئین کننده (آگونیستهای LHRH) داروهایی هستند که سطح استروژن را در زنانی که هنوز تخمدانهای فعال دارند کاهش میدهند. این داروها تخمدانها را در زنانی که یائسه شده اند، خاموش میکنند تا استروژن تولید نکنند.
گوسرلین (Zoladex یا Goserelin) و لوپرولید (Lupron یا leuprolide) داروهایی هستند که ممکن است برای درمان سرطان آندومتر استفاده شوند. آنها هر 1 تا 3 ماه به عنوان واکسن تزریق میشوند. این داروها آگونیستهای هورمون آزاد کننده گنادوتروپین (called gonadotropin-releasing hormone یا GNRH) نیز نامیده میشوند.
عوارض جانبی میتواند شامل هر یک از علائم یائسگی مانند گر گرفتگی و خشکی واژن باشد. مصرف آنها همچنین میتوانند باعث درد عضلات و مفاصل شوند. اگر این داروها برای مدت طولانی (سالها) مصرف شوند، میتوانند استخوانها را ضعیف کرده و گاهی منجر به پوکی استخوان شوند.
مهارکنندههای آروماتاز (Aromatase inhibitors)
حتی پس از برداشتن تخمدانها (یا غیر فعال شدن آنها)، استروژن همچنان در بافت چربی ساخته میشود. این بافت منبع اصلی استروژن بدن میشود. داروهایی به نام مهارکنندههای آروماتاز می توانند از ساخت این استروژن جلوگیری کرده و سطح استروژن را حتی بیشتر کاهش دهند. نمونههایی از مهارکنندههای آروماتاز عبارتند از لتروزول (Femara یا letrozole)، آناستروزول (Arimidex یا anastrozole) و exemestane (Aromasin).
این داروها اغلب برای درمان سرطان سینه استفاده میشوند اما میتوانند در درمان سرطان آندومتر نیز مفید باشند. آنها اغلب برای درمان زنانی استفاده میشوند که نمیتوانند جراحی را انجام دهند اما پزشکان در حال بررسی راههای دیگری هستند که این داروها در آنها میتوانند به شکل مفیدی عمل کنند.
عوارض جانبی میتواند شامل سردرد، درد مفاصل و عضلات و گر گرفتگی باشد. اگر این داروها برای مدت طولانی (سالها) مصرف شوند، میتوانند استخوانها را ضعیف کرده و گاهی منجر به پوکی استخوان شوند. این داروها هنوز برای تعیین بهترین روش استفاده از آنها برای درمان سرطان آندومتر در حال بررسی هستند.
درمان هدفمند (Targeted therapy) برای سرطان آندومتر
درمان هدفمند درمان با داروهایی است که برای هدف قرار دادن تغییرات خاصی در سلولهای سرطانی ساخته شده اند. داروهای هدفمند درمانی، متفاوت از داروهای استاندارد شیمی درمانی عمل میکنند.
آنها معمولاً عوارض جانبی متفاوت (و گاهی اوقات با شدت کمتری) نسبت به شیمی درمانی دارند.
درمان هدفمند برای درمان بسیاری از انواع سرطان استفاده میشود اما هنوز برای درمان سرطان آندومتر یک روش جدید است. فقط تعداد کمی از این داروها در حال حاضر استفاده میشوند. برخی از این موارد تنها به عنوان بخشی از یک کار آزمایی بالینی ارائه میشوند اما بسیاری دیگر در حال مطالعه هستند. این داروها بیشتر برای درمان سرطانهای پرخطر آندومتر و سرطانهایی که پس از درمان گسترش یافته (متاستاز) یا عود کرده اند، استفاده میشوند.
لنواتینیب (Lenvatinib)
Lenvatinib (Lenvima) نوعی دارو است که به عنوان مهار کننده کیناز (kinase inhibitor) شناخته میشود. این دارو کمک میکند تا تومورها از تشکیل رگهای خونی جدید باز بمانند و همچنین برخی از پروتئینهای سلولهای سرطانی را که به طور معمول به رشد آنها کمک میکنند، هدف قرار میدهند.
میتوان آن را همراه با داروی ایمونوتراپی پمبرولیزوماب (Keytruda) برای درمان برخی از سرطانهای پیشرفته آندومتر، معمولاً پس از حداقل یک دوره درمان دارویی دیگر استفاده کرد.
Lenvatinib به صورت کپسول یک بار در روز مصرف میشود.
عوارض جانبی شایع عبارتند از اسهال، خستگی، درد مفاصل یا عضلات، از دست دادن اشتها، تهوع و استفراغ، زخمهای دهانی، کاهش وزن، فشار خون بالا و تورم در بازوها یا پاها. عوارض جانبی کمتر شایع اما جدیتر میتواند شامل خونریزی جدی، لخته شدن خون، فشار خون بسیار بالا، اسهال شدید، ایجاد سوراخهایی در روده و نارسایی کلیه، کبد یا قلب باشد.
بواسیزوماب (Bevacizumab)
بواسیزوماب (Avastin) متعلق به دسته ای از داروها به نام مهارکنندههای رگ زایی است. برای رشد و گسترش سرطانها، آنها نیاز به ساخت رگهای خونی جدید برای تغذیه خود دارند (فرآیندی به نام رگ زایی یا angiogenesis). این دارو به پروتئینی به نام VEGF (که سیگنال تشکیل رگهای خونی جدید را میدهد) میچسبد و رشد سرطان را کند یا متوقف میکند.
بواسیزوماب اغلب همراه با شیمی درمانی تجویز میشود اما میتوان آن را به تنهایی نیز تجویز کرد، معمولاً پس از آزمایش سایر درمانهای دارویی.
این دارو به صورت انفوزیون داخل ورید (IV) هر 2 تا 3 هفته تجویز میشود.
عوارض جانبی شایع عبارتند از فشار خون بالا، خستگی، خونریزی، کاهش تعداد گلبولهای سفید خون، سردرد، زخمهای دهانی، از دست دادن اشتها و اسهال. عوارض جانبی نادر اما احتمالاً جدی شامل لخته شدن خون، خونریزی شدید، بهبود آهسته زخم، ایجاد سوراخ در روده بزرگ (perforations) و ایجاد اتصالات غیر طبیعی بین روده و پوست یا مثانه (fistulas) است. اگر سوراخ یا فیستول ایجاد شود، میتواند منجر به بروز عفونت شدید شود و ممکن است در این مورد نیاز به جراحی نیز باشد.
مهارکنندههای mTOR (mTOR inhibitors)
این داروها پروتئین سلولی به نام mTOR را مسدود میکنند که به طور معمول به رشد سلولها و تقسیم آنها به سلولهای جدید کمک میکند. این داروها ممکن است به تنهایی داده شوند یا به داروهای شیمی درمانی یا هورمون درمانی برای درمان سرطانهای پیشرفته (در مرحله بالاتر) آندومتر یا آنهایی که پس از درمان عود میکنند، اضافه شوند.
Everolimus (Afinitor) به عنوان قرص یک بار در روز مصرف میشود.
عوارض جانبی شایع شامل زخمهای دهانی، اسهال، حالت تهوع، احساس ضعف یا خستگی، تنگی نفس و سرفه است. اورولیموس همچنین میتواند باعث کاهش شمارش خون، افزایش لیپیدهای خون (کلسترول و تری گلیسیرید) و افزایش قند خون شود، بنابراین پزشک در حین مصرف این دارو، اغلب میزان عناصر موجود در خون شما را بررسی میکند.
Temsirolimus (Torisel) به صورت انفوزیون داخل وریدی (IV) معمولاً یک بار در هفته تجویز میشود. این دارو را میتوان به تنهایی تجویز کرد.
شایع ترین عوارض جانبی این دارو زوائد پوستی، ضعف، زخمهای دهانی، اسهال، حالت تهوع، از دست دادن اشتها، تجمع مایع در صورت یا پاها و افزایش سطح قند و کلسترول خون است. به ندرت، عوارض جانبی جدی تری گزارش شده است.

ایمونوتراپی (Immunotherapy) برای سرطان آندومتر
ایمونوتراپی درمان با داروهایی است که به سیستم ایمنی بدن فرد کمک میکنند تا سلولهای سرطانی را بهتر بشناسد و آنها را از بین ببرند.
مهارکنندههای ایست بازرسی ایمنی (Immune checkpoint inhibitors)
بخش مهمی از سیستم ایمنی، توانایی آن در جلوگیری از حمله به سلولهای طبیعی بدن است. برای انجام این کار، از پروتئینهای «نقطه بازرسی یا checkpoint» روی سلولهای ایمنی استفاده میکنند که مانند سوئیچهایی عمل میکنند که باید روشن (یا خاموش شوند) تا پاسخ ایمنی را شروع کنند. سلولهای سرطانی گاهی اوقات از این نقاط بازرسی برای جلوگیری از حمله سیستم ایمنی استفاده میکنند.
داروهایی که این نقاط بازرسی را هدف قرار میدهند (به نام مهارکنندههای ایمن ایست بازرسی) میتوانند برای درمان برخی از سرطانهای آندومتر استفاده شوند.
مهارکنندههای PD-1 (PD-1 inhibitors)
پمبرولیزوماب (Keytruda یا Pembrolizumab) و دوستارلیماب (dostarlimab یا Jemperli) داروهایی هستند که PD-1، پروتئینی روی سلولهای سیستم ایمنی به نام سلولهای T را هدف قرار میدهند. PD-1 به طور معمول به جلوگیری از حمله سلولهای T به سایر سلولهای بدن (از جمله برخی از سلولهای سرطانی) کمک میکند. با مسدود کردن PD-1، این داروها پاسخ ایمنی در برابر سلولهای سرطانی را تقویت میکنند. این پدیده میتواند برخی از تومورها را کوچک کرده یا رشد آنها را کند کند.
پمبرولیزوماب را میتوان به تنهایی برای درمان سرطانهای پیشرفته آندومتر استفاده کرد، معمولاً میتوان این دارو را پس از آزمایش سایر روشهای درمانی، اگر جراحی یا پرتو درمانی گزینههای مناسبی نباشند و اگر سلولهای سرطانی دارای یکی از موارد زیر باشند، تجویز کرد:
- سطح بالایی از ناپایداری ریز ماهواره (high level of microsatellite instability یا MSI-H) یا نقص در ژن تعمیر عدم تطابق (dMMR یا defect in a mismatch repair gene)
- بار جهش توموری بالا (high tumor mutational burden یا TMB-H) به این معنی که سلولها دارای جهشهای ژنی زیادی هستند.
سلولهای تومور را میتوان برای بررسی وجود این تغییرات آزمایش کرد.
پمبرولیزوماب همچنین میتواند همراه با داروی هدفمند لنواتینیب (Lenvima) برای درمان سرطانهای پیشرفته آندومتر که دارای کمبود MMR (dMMR) یا MSI بالا (MSI-H) نیستند، معمولاً پس از حداقل یک دوره درمان دارویی دیگر استفاده شود.
این دارو به صورت انفوزیون داخل وریدی (IV) معمولاً هر 3 یا 6 هفته یک بار تجویز میشود.
Dostarlimab را میتوان برای درمان سرطان پیشرفته یا عود کننده آندومتر، پس از انجام شیمی درمانی و در صورتی که سلولهای سرطانی نقصی در ژن ترمیم ناسازگاری (dMMR) داشته باشند، استفاده کرد.
این دارو به صورت انفوزیون داخل وریدی (IV) معمولاً ابتدا هر 3 هفته یکبار و سپس هر 6 هفته یکبار تجویز میشود.
عوارض جانبی احتمالی
عوارض جانبی این داروها میتواند شامل موارد زیر باشد:
- احساس خستگی یا ضعف
- تب
- سرفه
- حالت تهوع
- خارش
- زوائد پوستی
- از دست دادن اشتها
- درد عضلانی یا مفصلی
- تنگی نفس
- یبوست یا اسهال
سایر عوارض جانبی جدی تر کمتر رخ میدهند. این عوارض جدی میتواند شامل موارد زیر باشند:
واکنشهای انفوزیون (Infusion reactions): برخی از افراد ممکن است در حین مصرف یکی از این داروها، واکنش انفوزیون داشته باشند. این عارضه مانند یک واکنش آلرژیک است و میتواند شامل تب، لرز، برافروختگی صورت، زوائد پوستی، خارش پوست، احساس سرگیجه، خس خس سینه و مشکل در تنفس باشد. مهم است که در صورت داشتن هر یک از این علائم در حین مصرف یکی از این داروها، فوراً به پزشک یا پرستار خود اطلاع دهید.
واکنشهای خود ایمنی (Autoimmune reactions): این داروها اساساً با حذف یکی از محافظهای سیستم ایمنی بدن عمل میکنند. گاهی اوقات این امر باعث میشود که سیستم ایمنی بدن به سایر قسمتهای آن حمله کند که همین امر میتواند باعث ایجاد مشکلات جدی یا حتی تهدیدک ننده زندگی در ریهها، رودهها، کبد، غدد هورمون ساز، کلیهها، پوست یا سایر اندامها شود.
بسیار مهم است که هر گونه عوارض جانبی جدید را فوراً به تیم مراقبتهای بهداشتی و پزشکی خود گزارش دهید. اگر عوارض جانبی جدی دارید، ممکن است لازم باشد که روند درمان قطع شود و دوزهای بالایی از کورتیکواستروئیدها (corticosteroids) برای سرکوب سیستم ایمنی برای شما تجویز شود.
انتخابهای درمانی برای سرطان آندومتر، بر اساس مرحله
مرحله (وسعت) سرطان آندومتر مهم ترین عامل در انتخاب روش درمان آن است. اما عوامل دیگری نیز میتوانند بر گزینههای درمانی شما تأثیر بگذارند، از جمله نوع سرطان، سن و سلامت کلی شما و اینکه آیا میخواهید بچه دار شوید یا خیر. آزمایشهایی که روی سلولهای سرطانی انجام میشوند نیز برای یافتن پاسخ اینکه آیا درمانهای خاصی مانند هورمون درمانی و درمان هدفمند ممکن است بر این نوع سرطان مؤثر واقع شوند، انجام میگیرند.
جراحی اولین روند درمانی تقریباً برای تمام زنان مبتلا به سرطان آندومتر است. این عمل شامل برداشتن رحم، لولههای فالوپ و تخمدانها است. (به این عمل سالپنگوئوفورکتومی دوطرفه کامل هیسترکتومی یا TH/BSO یا total hysterectomy bilateral salpingo-oophorectomy گفته میشود). غدد لنفاوی از لگن و اطراف آئورت نیز ممکن است برداشته شده (برش غدد لنفاوی لگنی و پارا آئورت [LND یا para-aortic lymph node dissection] یا نمونه برداری) و برای تعیین میزان گسترش سرطان آزمایش شوند.
شستشوی لگن نیز ممکن است انجام شود. بافتهای برداشته شده در جراحی برای مشاهده میزان گسترش سرطان (مرحله) مورد آزمایش قرار میگیرند. بسته به مرحله سرطان، درمانهای دیگری مانند پرتو درمانی و یا شیمی درمانی ممکن است توصیه شود.
برای برخی از زنانی که هنوز میخواهند باردار شوند، ممکن است جراحی برای مدتی به تعویق بیفتد و به جای آن از روشهای درمانی دیگری استفاده شود.
اگر وضعیت سلامتی زنی به اندازه کافی برای انجام جراحی خوب نباشد، از دورههای درمانی دیگری مانند پرتو درمانی استفاده میشود.
مرحله اول (I) سرطان
در مرحله اول سرطان فقط در رحم است. بیماری به غدد لنفاوی یا مکانهای دور سرایت نکرده است.
مرحله اول سرطان آندومتروئید
درمان استاندارد شامل جراحی برای برداشتن و مرحله بندی سرطان است (به مباحث بالا مراجعه کنید). گاهی اوقات این تنها روند درمانی مورد نیاز است. سپس بیمار از نزدیک برای بررسی وجود علائم بازگشت سرطان (عود) تحت نظر قرار میگیرد.
برای زنانی که تومورهای درجه بالاتری دارند، احتمالاً پس از جراحی پرتو درمانی توصیه میشود. میتوان از براکی تراپی واژن (VB یا Vaginal brachytherapy)، پرتو درمانی لگنی یا هر دو نیز استفاده کرد.
برخی از زنان جوانتر مبتلا به سرطان آندومتر اولیه ممکن است بدون برداشتن تخمدانها رحم خود را خارج کنند. این کار از بروز یائسگی و مسائلی که میتواند با آن به وجود بیاید جلوگیری میکند. این کار همچنین احتمال عود سرطان را افزایش میدهد اما احتمال مرگ در اثر سرطان را افزایش نمیدهد. این روش ممکن است چیزی باشد که بخواهید با پزشک خود در میان بگذارید.
زنانی که به دلیل مشکلات پزشکی دیگر نمیتوانند عمل جراحی انجام دهند یا به دلیل سن بالا ضعیف هستند، اغلب فقط با پرتو درمانی (پرتوهای خارجی و یا براکی تراپی واژینال) درمان میشوند.
درمان ناباروری برای سرطانهای اندومتریوئید درجه 1 مرحله IA: برای زنان جوانی که هنوز میخواهند بچه دار شوند، ممکن است در حالی که از پروژسترون درمانی برای درمان سرطان استفاده میشود، عمل جراحی به تعویق بیفتد. درمان با پروژستین میتواند باعث کوچک شدن یا حتی از بین رفتن سرطان برای مدتی شود و به زن فرصتی برای باردار شدن بدهد. با این حال، این روش آزمایشی است و اگر بیمار از نزدیک تحت نظر نباشد، میتواند برای وی خطرناک باشد.
بیوپسی آندومتر یا D&C باید هر 3 تا 6 ماه انجام شود. اگر بعد از 6 ماه هنوز سرطان وجود نداشته باشد، زن میتواند اقدام به بارداری کند. او هر 6 ماه یک بار از نظر بررسی وجود سرطان معاینه میشود. از آن جایی که سرطان اغلب دوباره عود میکند، پزشکان TH/BSO را پس از کامل شدن فرزند آوری توصیه میکنند.
در بسیاری از مواقع، درمان با پروژسترون جواب نمیدهد و سرطان بهتر نمیشود یا به رشد خود ادامه میدهد. به تعویق انداختن عمل جراحی میتواند به سرطان فرصت انتشار به خارج از رحم بدهد. اگر سرطان طی 6 تا 12 ماه از بین نرفت، جراحی برای برداشتن و مرحله بندی سرطان (هیسترکتومی و برداشتن لولههای فالوپ و تخمدانها) توصیه میشود.
نظر دوم انکولوژیست زنان و پاتولوژیست (برای تایید درجه سرطان) قبل از شروع درمان با پروژسترون مهم است. مراجعه به متخصص باروری نیز ایده خوبی است. درک این نکته مهم است که این یک درمان استاندارد نیست و ممکن است خطر رشد و گسترش سرطان را افزایش دهد.
انواع دیگر سرطان آندومتر مرحله اول
سرطانهایی مانند کارسینوم سروز پاپیلاری، کارسینوم سلول شفاف یا کارسینوسارکوما به احتمال زیاد در هنگام تشخیص به خارج از رحم گسترش یافته اند. بدن زنان مبتلا به این نوع تومورها به خوبی آنهایی که تومورهای درجه پایین تر دارند، عمل نمیکند.
اگر بیوپسی انجام شده قبل از جراحی، سرطان با درجه بالا را نشان دهد، جراحی ممکن است گسترده تر باشد. همراه با هیسترکتومی کامل و برداشتن لولههای فالوپ و تخمدانها، غدد لنفاوی لگنی و پارا آئورت نیز برداشته شده و اغلب اوقات امنتوم نیز برداشته و حذف میشود.
پس از جراحی، شیمی درمانی (chemo) همراه با پرتو درمانی یا بدون آن برای جلوگیری از عود سرطان انجام میشود. شیمی درمانی معمولاً شامل داروهای کربوپلاتین و پاکلیتاکسل میشود اما میتوان از داروهای دیگر نیز استفاده کرد.
اگر سرطان را نتوان با جراحی برداشت، هم شیمی درمانی (chemotherapy و هم از پرتو درمانی استفاده میشود. گاهی اوقات، تومور پس از آن کوچک میشود به طوری که میتوان برای برداشتن آن جراحی انجام داد.
سرطانهای مرحله دوم (II)
زمانی که سرطان آندومتر در مرحله دوم باشد، به بافت همبند دهانه رحم گسترش یافته است اما هنوز در خارج از رحم رشد نکرده است.
یکی از گزینههای درمانی این است که ابتدا جراحی و سپس پرتو درمانی انجام شود. این جراحی شامل هیسترکتومی رادیکال (کل رحم، بافتهای کنار رحم و قسمت بالایی واژن برداشته میشود)، برداشتن لولههای فالوپ و تخمدانها (BSO) و برش غدد لنفاوی لگنی و پارا آئورت (LND) یا نمونه برداری است. پرتو درمانی، اغلب هم شامل براکی تراپی واژینال و هم پرتو درمانی خارجی لگن است که ممکن است پس از بهبودی بیمار بعد از عمل جراحی انجام شود. گزینه دیگر این است که ابتدا پرتو درمانی و سپس یک هیسترکتومی ساده، BSO و نمونه برداری احتمالی LND یا غدد لنفاوی انجام دهید.
غدد لنفاوی که برداشته شده اند از نظر وجود سلولهای سرطانی بررسی میشوند. اگر سرطان در آنها وجود داشته باشد، سرطان واقعاً مرحله در مرحله دوم نیست و در مرحله IIIC است.
در برخی موارد، یک زن مبتلا به سرطان آندومتر در مراحل اولیه ممکن است به دلیل ابتلا به بیماریهای دیگر بسیار ضعیف یا بیمار باشد تا بتواند با خیال راحت تحت جراحی قرار گیرد. این زنان با پرتوهای خارجی و براکی تراپی درمان میشوند.
برای زنان مبتلا به سرطانهای با درجه بالا، مانند کارسینوم سرووز پاپیلاری یا کارسینوم سلول شفاف، جراحی ممکن است شامل انتکتومی و بیوپسی صفاقی همراه با هیسترکتومی کامل، برداشتن لولههای فالوپ و تخمدانها، برشهای غدد لنفاوی لگنی و پارا آئورت و لگن باشد. انجام شستشوها پس از جراحی، پرتو درمانی، شیمی درمانی یا هر دو ممکن است برای جلوگیری از عود سرطان تجویز شود. شیمی درمانی معمولاً شامل داروهای کربوپلاتین و پاکلیتاکسل یا احتمالاً سیس پلاتین و دوکسوروبیسین است.
فردی که در مرحله دوم کارسینوسارکوم رحمی قرار دارد، اغلب همان نوع جراحی را انجام میدهد که برای سرطان با درجه بالا استفاده میشود. پس از جراحی، ممکن است از پرتو درمانی، شیمی درمانی یا هر دو استفاده شود. شیمی درمانی اغلب شامل پاکلیتاکسل و کربوپلاتین است اما ممکن است در عوض شامل ایفوسفامید، همراه با پاکلیتاکسل یا سیس پلاتین باشد.
سرطانهای مرحله III
در مرحله سوم، سرطان آندومتر به خارج از رحم گسترش یافته است.
اگر جراح فکر کند که تمام تودههای سرطانی قابل مشاهده قابل برداشتن هستند، هیسترکتومی انجام شده و هر دو تخمدان و لولههای فالوپ برداشته میشوند. گاهی اوقات زنان مبتلا به سرطان مرحله سوم نیاز به هیسترکتومی رادیکال دارند. تشریح غدد لنفاوی لگنی و پارا آئورت نیز ممکن است انجام شود. شستشوی لگنی نیز انجام میشود و ممکن است امنتوم از بدن خارج شود. برخی از پزشکان تلاش میکنند تا سرطانهای باقی مانده را حذف کنند (عملی به نام debulking) اما مشخص نیست که این کار به بیماران کمک میکند تا عمر طولانی تری داشته باشند یا خیر.
اگر آزمایشهای انجام شده قبل از جراحی نشان دهند که سرطان بیش از حد گسترش یافته است که نمیتواند به طور کامل برداشته شود، در موارد نادر، ممکن است قبل از هر عمل جراحی، پرتو درمانی انجام شود. این روش ممکن است آن قدر تومور را کوچک کند که جراحی را به یک گزینه مناسب برای بیمار تبدیل کند. برای سرطانهای پیشرفته آندومتر که با جراحی یا پرتو درمانی قابل درمان نیستند، درمان با داروی ایمونوتراپی پمبرولیزوماب ممکن است یک گزینه باشد.
مرحله IIIA: سرطان مرحله IIIA به بافت پوشاننده رحم (سروز) یا سایر بافتهای لگن مانند لولههای فالوپ یا تخمدانها (آدنکس یا adnexa) گسترش یافته است. برای این سرطانها، روش درمانی پس از جراحی ممکن است شامل شیمی درمانی، پرتو درمانی یا هر دو باشد. پرتو به لگن یا هر دو شکمو لگن داده میشود. براکی تراپی واژینال نیز اغلب استفاده میشود.
مرحله IIIB: در این مرحله سرطان به واژن گسترش یافته است. پس از جراحی، سرطان مرحله IIIB ممکن است با شیمی درمانی و یا پرتو درمانی درمان شود.
مرحله IIIC: این نوع شامل سرطانهایی است که به غدد لنفاوی لگن (مرحله IIIC1) و یا به غدد لنفاوی اطراف آئورت (مرحله IIIC2) گسترش یافته اند. روند درمان شامل جراحی و به دنبال آن انجام شیمی درمانی و یا پرتو درمانی است.
برای زنان مبتلا به سرطانهای درجه بالا، مانند کارسینوم سرووز پاپیلاری یا کارسینوم سلول شفاف، جراحی ممکن است شامل آمنتکتومی و بیوپسی صفاقی همراه با هیسترکتومی کامل، برداشتن هر دو تخمدان و لولههای فالوپ، برشهای غدد لنفاوی لگنی و پارا آئورت باشد.
شستشوی لگنی پس از جراحی، شیمی درمانی، پرتو درمانی یا هر دو ممکن است برای جلوگیری از عود سرطان تجویز شود. شیمی درمانی معمولاً شامل داروهای کربوپلاتین و پاکلیتاکسل یا سیس پلاتین و دوکسوروبیسین است.
زنان مبتلا به کارسینوسارکوم رحم مرحله III اغلب از همان نوع جراحی استفاده میکنند که برای سرطان با درجه بالا استفاده میشود. پس از انجام جراحی، ممکن است از پرتو درمانی، شیمی درمانی یا هر دو استفاده شود. شیمی درمانی اغلب شامل داروی پاکلیتاکسل و کربوپلاتین است اما ایفوسفامید همراه با پاکلیتاکسل یا سیس پلاتین نیز ممکن است استفاده شوند. روشهای درمانی هدفمند و یا ایمونوتراپی نیز ممکن است گزینههای مناسبی برای برخی از زنان باشند.
سرطانهای مرحله IV
مرحله IVA: این سرطانهای آندومتر به مثانه یا روده رشد کرده اند.
مرحله IVB: این سرطانهای آندومتر به غدد لنفاوی خارج از لگن یا ناحیه پارا آئورت گسترش یافته اند. این مرحله همچنین شامل سرطانهایی است که به کبد، ریهها، امنتوم یا سایر اندامها گسترش یافته اند.
برخی از سرطانهای آندومتر مرحله IV هستند زیرا به غدد لنفاوی شکم (و نه فقط لگن و ناحیه پارا آئورت) گسترش یافته اند اما به هیچ ناحیه دیگری سرایت نکرده اند. زنان مبتلا به این نوع گسترش سرطانی ممکن است نتایج بهتری داشته باشند اگر تمام سرطانی که دیده میشود، برداشته شود (حجم زدایی شود) و نمونه برداری از نواحی دیگر شکم، وجود سلولهای سرطانی را نشان ندهد.
در اغلب موارد سرطان آندومتر مرحله IV، سرطان بیش از حد گسترش یافته است که نمیتوان با جراحی آن را برداشت. هیسترکتومی و برداشتن لولههای فالوپ و تخمدانها همچنان ممکن است برای جلوگیری از خونریزی بیش از حد انجام شود. به همین دلیل ممکن است از پرتو درمانی نیز استفاده شود. هنگامی که سرطان به سایر نقاط بدن گسترش یافته است، ممکن است هورمون درمانی مورد استفاده قرار گیرد. اما سرطانهای با درجه بالا و آنهایی که گیرندههای پروژسترون و استروژن قابل تشخیص روی سلولهای سرطانی ندارند، احتمالاً به هورمون درمانی پاسخ نمیدهند.
مصرف ترکیبی از داروهای شیمی درمانی ممکن است برای مدتی به برخی از زنان کمک کنند. داروهایی که اغلب مورد استفاده قرار میگیرند پاکلی تاکسل، دوکسوروبیسین و کربوپلاتین یا سیس پلاتین هستند. این داروها اغلب با هم و به صورت ترکیبی استفاده میشوند. کارسینوسارکوم مرحله IV اغلب با همان شیمی درمانی درمان میشود. سیس پلاتین، ایفوسفامید و پاکلیتاکسل نیز ممکن است با یکدیگر ترکیب شوند.
داروهای هدفمند و یا داروهای ایمونوتراپی نیز ممکن است گزینههایی برای برخی از زنان مبتلا به سرطان آندومتر پیشرفته باشند.
زنان مبتلا به مرحله IV سرطان آندومتر باید شرکت در آزمایشات بالینی شیمی درمانی یا سایر درمانهای جدید را در نظر بگیرند.
سرطان آندومتر عود کننده
زمانی که پس از گذراندن روند درمان سرطان دوباره عود میکند، این سرطان عود کننده (recurrent) نامیده میشود. عود میتواند موضعی (در همان جایی که شروع شده است یا نزدیک آن ناحیه) یا دور (گسترش به اندامهایی مانند ریهها یا استخوانها) باشد. روند درمان بستگی به میزان سرطان و محل آن و همچنین نوع روش درمانی دارد که برای اولین بار استفاده شده است.
برای عودهای موضعی، مانند لگن، از جراحی (گاهی با پرتو درمانی به دنبال آن) استفاده میشود. برای زنانی که شرایط پزشکی دیگری دارند که آنها را قادر به انجام عمل جراحی نمیکند، پرتو درمانی به تنهایی یا همراه با هورمون درمانی استفاده میشود.
برای عودهای دور، ممکن است از جراحی و یا پرتو درمانی متمرکز در زمانی استفاده شود که سرطان فقط در چند نقطه کوچک (مانند ریهها یا استخوانها) ایجاد شده باشد. زنانی که تومورهای عود کننده گسترده تری دارند (سرطان گسترده) مانند کسانی که در مرحله چهارم سرطان آندومتر قرار دارند، درمان میشوند.
برای این بیماران هورمون درمانی یا شیمی درمانی توصیه میشود. سرطانهای با درجه پایین حاوی گیرندههای پروژسترون، به احتمال زیاد به هورمون درمانی پاسخ میدهند. سرطانهای درجه بالاتر و آنهایی که گیرندههای قابل تشخیصی ندارند بعید است در طول هورمون درمانی کوچک شوند اما ممکن است به شیمی درمانی پاسخ دهند. ممکن است در برخی موارد از درمان هدفمند و ایمونوتراپی نیز استفاده شود. آزمایشات بالینی روشهای درمانی جدید گزینههای مناسب دیگری برای این افراد هستند.
مظالعه بیشتر:
سرطان استخوان (Bone Cancer) چیست؟
سرطان مجرای صفراوی (Bile Duct Cancer) چیست؟
مترجم: فاطمه فریادرس