دستگاه ها
pH متر چیست و 12 مطلب کلیدی درباره آن
pH متر
همچنین به آن “pH متر پتانسیومتری” نیز میگویند زیرا تغییرات الکتریکی بین الکترود Ph و الکترود مرجع را اندازهگیری میکند.تغییر پتانسیل الکتریکی به اسیدیته یا Ph سوسپانسیون مرتبط است.از این وسیله برای آزمایش، کنترل کیفیت و … استفاده میشود.کلمه pH از p، رقم علمی لگاریتم منفی و H، نماد شیمیایی هیدروژن به دست آمده است.pH واحد اندازهگیری است که سطح اسیدی یا قلیایی بودن یک سوسپانسیون را بیان میکند. در محدوده 0 تا 14 درجهبندی میشود. pH = -log[H+]
در سال 1909، شیمیدان آلمانی برنده جایزه نوبل، فریتز هابز ( 1868 – 1934 ) و شاگردش زیگمونت کلمنشیویکز ( 1886 – 1963 ) ایده الکترود شیشهای را توضیح دادند. pH متر الکترونیکی مدرن در سال 1934 توسط یک شیمیدان آمریکایی، آرنولد بکمن ( 1900 – 2004 ) معرفی شد.
اندازهگیریpH
نرخ pH یک ماده مستقیما با درجه غلظت یون هیدروژن [+H] و یون هیدروکسیل [-OH] مرتبط است.
دادههای کمی ارائه شده از طریق Ph متر، نسبت حرکت یک اسید یا باز را بر حسب فعالیت یون هیدروژن نشان میدهد.
اگر مقدار غلظت +H از غلظت -OH در ماده بیشتر باشد، ماده ماهیت اسیدی دارد. (pH کمتر از 7)
اگر مقدار غلظت -OH از غلظت +H در ماده بیشتر باشد، ماده ماهیت بازی دارد. (pH بیشتر از 7)
اگر مقادیر یکسانی از یونهای +H و -OH وجود داشته باشد، ماده خنثی است و pH آن 7 است.
یونهای هیدروژن و هیدروکسیل آزاد دارای اسید و باز هستند. ارتباط بین یونهای هیدروژن و یونهای هیدروکسیل در یک سوسپانسیون عرضهشده، برای مجموعهای از شرایط ثابت است، هرکدام با شناسایی دیگری قابل حل است.
اصل کار pH متر :
pH متر از چند جزء حیاتی مانند الکترود اندازهگیری، الکترود مرجع و حسگر دما تشکیل شده است.
pH متر ولتاژ یک سلول الکتروشیمیایی را تخمین میزند و بر اساس سنسور دما pH یک سوسپانسیون را تعیین میکند.
اکثر pH مترها حاوی الکترودهای ترکیبی هستند که در آنها الکترودها و سنسور دما در یک قاب ساخته میشوند.
مجموع جبری پتانسیلهای الکترود اندازهگیری، الکترود مرجع و محل اتصال مایع به عنوان پتانسیل کلی یا ولتاژ شناخته میشود.
الکترود مرجع حاوی محلول خنثی مانند محلول کلریدپتاسیم با غلظت ثابت است و ولتاژ پایداری میدهد.
در مقابل، پتانسیل الکترود اندازهگیری کاملا به pH سوسپانسیون بستگی دارد.
تغییرات پتانسیل (ولتاژ) بین یک غشای شیشهای الکترود اندازهگیری و یک الکترود مرجع (در مایع نمونه غوطهور شدهاست) که مورد بررسی قرار گرفتهاست، تخمین زده میشود.
هنگامی که دو الکترود در سوسپانسیون نمونه غوطهور میشوند، فرآیند تبادل یونی اتفاق میافتد که در آن برخی از یونهای هیدروژن به سمت سطح بیرونی الکترود اندازهگیری جریان مییابند و برخی از یونهای فلزی را در آن جابجا میکنند.
فرآیندهای مبادلهای علاوه بر این، در سطح داخلی الکترود شیشهای از تعلیق نمونه انجام میشود.
این یک تنوع بالقوه (فعالیت یون هیدروژن) در بین آنها ایجاد میکند. پتانسیل اتصال مایع معمولا دقیق است که اساسا به شدت یونهای موجود در سوسپانسیون نمونه بستگی دارد.
هر سه پتانسیل توسط ولتمتر مقاومت ظاهری بالا خلاصه و رتبهبندی میشود.
ولتاژ پتانسیل تولید شده فراتر از غشای الکترود شیشهای وابسته به دما است. (با ضریب دمایی حدود 0.3% در هر درجه سانتیگراد)
pH مترها مقرراتی برای بهبود اندازهگیری pH با تغییر دما دارند و به عنوان جبران خودکار دما (ATC) نامیده میشوند.
خروجی ولتمتر مقاومت ظاهری، مطالعات ولتاژ است و دارای کالیبره برای اندازهگیری دقیق pH میباشد.
کالیبراسیون با غوطهور کردن الکترود اندازهگیری در مایع بافر با pH شناخته شده انجام میشود که به درک خواندن میلیولت به عنوان اندازهگیری pH سوسپانسیون نمونه در دمای تحویل شده، کمک میکند.
بخشهای کلیدی pH متر
- بررسی شدن محلول
- الکترود شیشهای، متشکل از:
یک لایه باریک از شیشه سیلیس شامل نمکهای فلزی که داخل آن محلول کلرید پتاسیم وجود دارد.
- یک الکترود داخلی
- ساختهشده از نقره/کلرید نقره.
- یونهای هیدروژن تولید شده در محلول آزمایشی با سطح بیرونی شیشه ارتباط برقرار میکند.
- یونهای هیدروژن تولید شده در محلول کلرید پتاسیم با سطح داخلی شیشه ارتباط برقرار میکنند.
- این مقیاس، تغییر ولتاژ بین دو سطح شیشه را تنظیم میکند و این تفاوت پتانسیل را به اندازه عددی pH تبدیل میکند.
- الکترود مرجع به عنوان یک خط پایه یا مرجع برای تجزیه و تحلیل عمل میکند – یا میتوانید آن را برای تکمیل مدار در نظر بگیرید.
روش کار pH متر
- pH متر را با فشار دادن کلید ON روی دستگاه روشن کنید. پس از روشن کردن pH متر، نشانگر MEAS و نشانگر ATC روی LCD ظاهر میشود.
- سپس الکترودها را با آب مقطر بشویید.
- دمای نمونه را در 25 درجه سانتیگراد نگه دارید.
- پس از آن، الکترودها را در داخل نمونه غوطهور کرده و آن را هم بزنید تا یک نمونه همگن ایجاد شود. مطمئن شوید که نوک الکترود در نمونه کامل شدهاست.
- صبر کنید تا عدد خوانده شده ثابت شود.
- هنگامی که عدد خوانده شده تثبیت شد، نشانگر READY فعال میشود. پس از آن عدد را با فشار دادن کلید HOLD و سپس کلید ENTER ذخیره کنید.
- حالا pH و مقدار دما را ثبت کنید.
- در نهایت الکترودها را با آب مقطر بشویید و با محلول بافر آن را ذخیره کنید.
کالیبراسیون pH متر
برای دستیابی به اندازهگیریهای بسیار دقیق، pH متر باید قبل از هر اندازهگیری کالیبره شود. همچنین کالیبراسیون یک بار در روز انجام میشود. کالیبراسیون مورد نیاز است زیرا الکترود شیشهای، پتانسیلهای الکترواستاتیکی قابل تکرار را در دورههای زمانی طولانیتری ارائه نمیدهد.
- ابتدا مطمئن شوید که حالت اندازهگیری صحیح در pH متر انتخاب شدهاست.
- سپس الکترود را با آب مقطر بشویید. الکترودها را با کاغذ پاک نکنید، در غیر این صورت باعث ایجاد بار الکترواستاتیکی روی الکترودها میشود.
- تمام استانداردها و نمونهها قبل از استفاده به دمای 25 درجه سانتیگراد میرسند.
- اکنون الکترودها را در محلول بافر استاندارد یا محلول کالیبراسیون (ph 7 / ph 10) غوطهور کنید. مطمئن شوید که نقطه انتهایی الکترودها به طور کامل در محلول بافر غوطهور شدهاست. برای ایجاد نمونه همگن، الکترودها را در بافر هم بزنید.
- اکنون با فشار دادن کلید CAL/MEAS وارد حالت کالیبراسیون pH شوید. علامت CAL نمایش داده خواهدشد.
- عدد اندازهگیری شده توسط نمایشگر اولیه نشان داده میشود، در حالی که عدد نشان دادهشده محلول بافر استاندارد pH ، توسط صفحه ثانویه کوچکتر نمایش داده میشود.
- صبر کنید تا مقادیر نشان دادهشده تثبیت شود.
- پس از تثبیت، کالیبراسیون را با فشار دادن کلید HOLD/ENTER تایید کنید. اکنون pH متر به محلول بافر فعلی کالیبره شدهاست.
- در نهایت الکترودها را با آب مقطر شسته و در محلول بافر قرار دهید.
انواع pH متر
بر اساس انواع مورد نیاز pH متر به چند کلاس تقسیم میشود از جمله:
- بر اساس قابلیت حمل، pH متر به دو دسته تقسیم میشود:
- pH متر قابل حمل: از پوشش گستردهای از ابزارها به طور منظم استفاده میشود، اما به استثنا استفاده از تجهیزات فشرده برق DC را نیز میتوان در صحنه تولید کرد.
- pH متر رومیزی: مانند pH متر قابل حمل
- pH متر قلمی: معمولا از یک مقیاس، محدوده اندازهگیری معمولی، برای تجهیزات آسان و مفید تشکیل شده است.
- بر اساس هدف، pH متر به دو دسته تقسیم میشود:
- pH متر آزمایشگاهی: محدوده اندازهگیری، چندکاره، دقت بالا.
- pH متر آنلاین صنعتی: با نیازهای پایداری عالی، کار ثابت، سطح خاصی از راندمان اندازهگیری، انعطافپذیری محیطی، قابلیت ضد تداخل، با خروجی آنالوگ، هوش دیجیتال، مرزهای بالا و پایین هشدار و عملکردهای کنترل شناسایی میشود.
- بر اساس سطح پیشرفته، pH متر به سه دسته تقسیم میشود:
- pH متر اقتصادی
- pH متر هوشمند
- pH متر دقیق یا به pH سنج اشارهگر، pH متر دیجیتال تقسیم میشود.
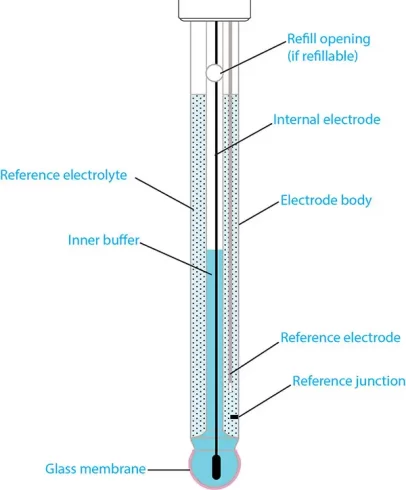
الکترود pH
الکترودهای pH از یک شیشه خاص تشکیل شدهاند که شدت یون هیدروژن را حس میکند.
شیشه از یونهای فلز قلیایی ساخته شدهاست. یک واکنش تبادل یونی بین یونهای فلز قلیایی شیشه و یونهای هیدروژن در محلول رخ میدهد. در نتیجه، این تبادل یونی، اختلاف پتانسیل اینجاد میکند.
پویشگر pH ترکیبی از دو الکترود مجزا مانند الکترود اندازهگیری pH و دیگری الکترود مرجع است.
محلول حاوی یونهای هیدروژن آزاد است و به تولید پتانسیل در محل اتصال بخش اندازهگیری کمک میکند.
هنگامی که قسمت داخلی با محلول پرکننده مرجع در تماس است، اختلاف پتانسیل روی قسمت مرجع ایجاد میشود. به طور خلاصه، الکترود pH اندازهگیری، ولتاژ متفاوتی تولید میکند و الکترود مرجع ولتاژ ثابتی را به متر تولید میکند.
سیگنال ولتاژ تولید شده از طریق پویشگر pH یک سیگنال مقاومت ظاهری بسیار کوچک و بزرگ است. مقاومت ظاهری داده ایجاب میکند که به تنهایی با دستگاههایی با مدارهای مقاومت ظاهری بالا ارتباط برقرار کند.
الکترودها برای اندازهگیری محیطهای آبی اختراع شدهاند. آنها برای استفاده در حلالهایی که هیچ یون هیدروژن آزاد ندارند، ساخته نشدهاند. مانند CCl4
الکترودها را همیشه مرطوب نگه دارید. برای عملکرد دقیق، شیشه نیاز به هیدراته شدن دارد.
برای انجام فرآیند تعویض، هیدراته کردن اجباری است.
اتصالاتی در الکترودهای pH وجود دارند که محلول پرکننده داخلی الکترود اندازهگیری را اندازهگیری میکنند. این اتصال میتواند توسط ذرات موجود در سوسپانسیون بسته شود و همچنین میتواند مسمومیت از طریق یونهای فلزی واقع در محلول را ایجاد کند.
برای حل یا پاک کردن مواد در محل اتصال، در صورت مشکوک شدن به گرفتگی اتصال، سنسور را در مقداری آب گرم فرو کنید. از pH سنجها، همیشه در حالت مرطوب نگهداری کنید. اگر از آن استفاده نمیشود، مناسب ترین حالت این است که الکترودها را در بافر 4.0 یا بافر 7.0 قرار دهید.
نقص الکترود معمولا از طریق پاسخ کند، عدد نشان دادهشده نامنظم یا عددی که تغییر نمیکند قابل تشخیص است. الکترودهای pH ضعیف هستند و طول عمر محدودی دارند.
مدت زمان کارکرد یک الکترود با نحوه صحیح نگهداری پویشگر و کاربرد pH تعیین میشود.
کالیبراسیون یک بخش حیاتی از کار با الکترود است. این نه تنها عملکرد دقیق الکترود را تضمین میکند، بلکه سیستم نیز به درستی کار میکند.
ساخت الکترودهای pH
الکترودهای شیشهای، الکترودهای pH پرکاربردی هستند که از لولههای شیشهای تشکیل شدهاند و با یک حباب شیشهای کوچک به پایان میرسند.
محلول بافر از کلریدها درون الکترودها بارگذاری میشود. یک سیم نقرهای پوشیده شده با کلرید نقره در داخل این محلول خیسانده شده است.
مقدار pH محلول در محدودهای مشخص قرار دارد – برای مثال میتواند 1.0 یا 7.0 باشد. (بافرهای مختلف استفاده شده توسط تولیدکنندگان مختلف)
حباب شیشهای قسمت فعال یک الکترود است.
بخش لولهای الکترود حاوی یک دیواره قوی و ضخیم است، در حالی که حباب حاوی یک دیواره نازک است.
محلول داخلی و خارجی هردو سطح شیشه را پروتونه میکنند و این عمل تا زمانی که تعادل حاصل شود، ادامه مییابد. پروتون های جذب شده هردو طرف شیشه را شارژ میکنند و مسئول ایجاد اختلاف پتانسیل هستند.
این پتانسیل در کمک با معادله نرنست (Nernest) تعریف میشود و به طور مستقیم معادل تغییر pH بین محلولها در هر دو سطح شیشه است.
اکثر الکترودهای pH که به صورت تجاری بدست میآیند، الکترودهای ترکیبی هستند که هم الکترودهای حساس به یون شیشه +H و هم الکترودهای مرجع بیشتری دارند و به راحتی در یک محفظه نصب میشوند.
الکترودهای pH جداگانه و الکترودهای مرجع هنوز برای کاربردهای خاص پذیرفته میشوند. آنها دقت بسیار زیادی را ارائه میدهند که گاهی اوقات برای اهداف تحقیقاتی مورد نیاز است. الکترودهای ترکیبی بسیار دقیق هستند و برای تمرین بسیار راحتتر هستند.
توسعه الکترود مرکب تا حد زیادی توسط فرآیندهایی تعیین میشود که باید هنگام تخمین pH انجام شود. ما نیاز به تخمین تغییرات پتانسیل در سطوح شیشه در الکترود شیشهای داریم. برای این کار به یک مدار بسته نیاز داریم.
مدار در محلولها – داخلی و خارجی – و pH متر قفل و ثابت شده است. اگرچه برای بازگشت دقیق و ثابت برآوردها، الکترودهای مرجع باید از مایع جدا شوند تا آلودگی متقاطع نداشته باشند – و اتصال و جدا کردن دو محلول در لحظه یکسان کار آسانی نیست.
بدنه الکترود حاوی یک سوراخ کوچک است که این اتصال را امکان پذیر میکند. این سوراخ شامل یک غشاء نفوذپذیر با فتیله سرامیکی است.
مایع داخلی به آرامی در محل اتصال حرکت میکند، بنابراین چنین الکترودهایی به عنوان الکترودهای جاری تعیین میشوند. برای کاهش نشتی، در الکترودهای ژل، محلول داخلی حالت ژل بخود میگیرد.
انواع الکترودها
سه نوع الکترود pH وجود دارد:
- الکترود شیشهای
- الکترود مرجع
- الکترود ژل ترکیبی
کاربرد pH متر
در صنایع کشاورزی از آن برای اندازهگیری pH خاک استفاده میشود.
برای اندازهگیری کیفیت آب برای منابع آب شهری، استخرهای شنا استفاده میشود.
در بسیاری از صنایع شیمیایی و دارویی از آن برای اندازهگیری مقدار pH محلولها استفاده میشود.
pH متر علاوه بر این در صنایع غذایی به ویژه برای محصولات لبنی مانند پنیر، کشک، ماست و غیره استفاده میشود.
همچنین در ساخت مواد شوینده نیز نقش حیاتی دارد.

مزایای pH متر
- کالیبراسیون pH قیمت پایین و بصرفهای دارد.
- pH مترهای جیبی برای کاربر مناسب هستند.
- حسابها و نتایج قابل اعتماد و خاص هستند.
معایب pH متر
- گرما بر برآوردها و نتایج عددی تاثیر میگذارد.
- کالیبراسیون با استفاده از الکترودهای شیشهای باید تمیز باشد زیرا رسوب روی الکترودها بر نتایج نهایی اثر میگذارد.
موارد ایمنی
الکترود را با مسئولیت و احتیاط لمس کنید زیرا شدیدا شکستنی و ظریف است.الکترود را همیشه در شرایط غوطهور در محلول مورد تایید شرکت یا محلول خنثی KCl نگهداری کنید.همیشه سطح داخلی مایع پرکننده را فراتر از سطح محلول اندازهگیری شده نگهداری کنید.الکترود (نوع جاری) را با محلول پرکننده دقیق (همانطور که سازنده پیشنهاد میکند – معمولا محلول KCl سه مولار اشباع) بارگیری کنید تا داخل آن خشک نشود.
اگر میخواهید از الکترودها برای مدت طولانی (برای جلوگیری از فرسودگی) استفاده نکنید، میتوانید آن را خشک نگه دارید. فرسودگی تنها زمانی اتفاق میافتد که الکترود مرطوب باشد. این کار را با الکترودهای ژلی انجام ندهید – برخی باید فقط در محلول قوی KCl قرار داده شوند.اگر الکترودها خشک هستند حداقل 24 ساعت قبل از استفاده آنها را خیس کنید.
هنگامی که از محلولی که حاوی موادی است که میتواند اتصال راببندد یا به حباب شیشهای بچسبد، استفاده میکنید، بلافاصله الکترودها را تمیز کنید.از غوطهور شدن الکترودها در حلالهایی که میتوانند شیشه را حل کنند، مانند اسید هیدروفلوروئیک (یا محلول اسیدی فلوراید) و مواد قلیایی غلیظ خودداری کنید.از غوطهور شدن الکترودها در محلولهای آبگیر مانند اتانول، اسید سولفوریک و غیره خودداری کنید.
از مالش یا پاک کردن لامپ الکترود خودداری کنید.الکترودها را با حلالهای آلی تمیز نکنید.
مطالعه صدها مطلب علمی در حوزه بیولوژی
آرشیو جدیدترین خبرهای روز دنیای بیولوژی





بسیار عالی
سلام چرا کالیبراسیون را از pH7شروع میکنیم؟
شروع کالیبراسیون از pH 7 باعث میشود که:
دستگاه بهطور دقیق در نقطه خنثی تنظیم شود.
خطای اندازهگیری به حداقل برسد.
فرآیند کالیبراسیون ساده و استاندارد شود.
این رویه تضمین میکند که اندازهگیریهای pH در شرایط مختلف اسیدی و قلیایی دقیق و قابلاعتماد باشند.
چگونه پی ادف بگیرم از مطالب
این قابلیت به زودی به سایت اضافه میشود
قیمت محلول مورد استفاده در این دستگاه میخواستم
سلام لطفا با آزمایشگاه تماس بگیرید.