اطلاعات عمومی,ویکی ژن
نوروآناتومی چیست؟ اهمیت نوروآناتومی در پژوهشهای نوروساینس
مقدمهای بر نوروآناتومی
نوروآناتومی (Neuroanatomy) شاخهای از علوم اعصاب است که به مطالعه ساختار و سازمانبندی دستگاه عصبی میپردازد. این دانش، پایه و اساس فهم عملکردهای مغز، بیماریهای عصبی و روشهای جراحی در حوزه نوروساینس است. آشنایی دقیق با نوروآناتومی به پژوهشگران و جراحان کمک میکند تا نواحی هدف را شناسایی کنند، مسیرهای عصبی را دنبال کنند و اثرات مداخلات جراحی یا آزمایشگاهی را پیشبینی نمایند.
ساختار کلی دستگاه عصبی
دستگاه عصبی به دو بخش اصلی تقسیم میشود:
- دستگاه عصبی مرکزی (CNS): شامل مغز و نخاع، محل پردازش و یکپارچهسازی اطلاعات حسی و حرکتی.
- دستگاه عصبی محیطی (PNS): شامل اعصاب جمجمهای و نخاعی که پیامها را بین CNS و سایر بخشهای بدن منتقل میکنند.
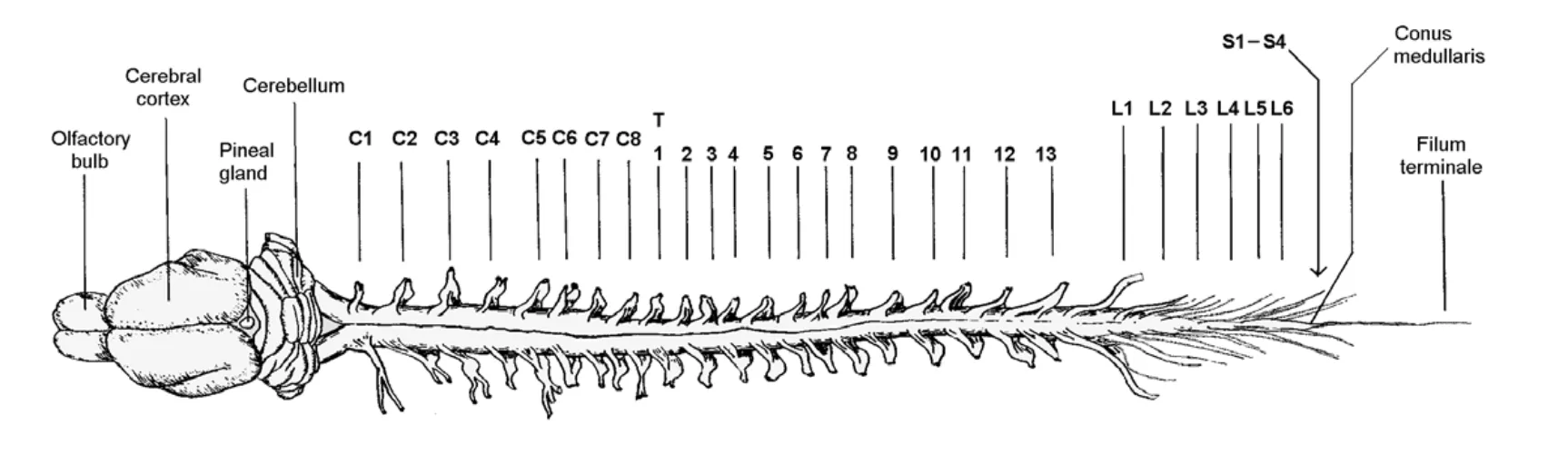
تقسیمبندیهای عملکردی مغز
- مغز قدامی (Forebrain): شامل قشر مخ (Cerebral Cortex) برای پردازش شناختی پیشرفته و ساختارهای زیرقشری مانند تالاموس و هیپوتالاموس.
- مغز میانی (Midbrain): مرکز پردازش برخی محرکهای حسی و کنترل حرکات چشم.
- مغز پسین (Hindbrain): شامل مخچه، پل مغزی و بصلالنخاع، مسئول کنترل حرکات، تعادل و عملکردهای حیاتی مانند تنفس.
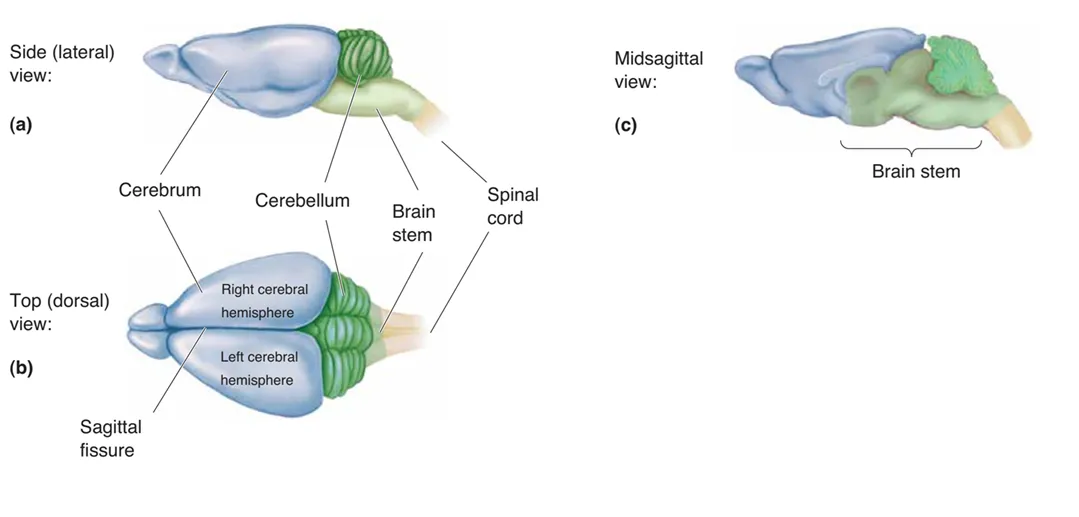
اصول شناسایی و مکانیابی ساختارها
در پژوهشها و جراحیهای حیوانات آزمایشگاهی (مثل رت یا موش)، استفاده از اطلس مغزی (Brain Atlas) برای یافتن مختصات دقیق ساختارهای هدف ضروری است. مختصات معمولاً نسبت به نقاط مرجع آناتومیک مانند Bregma یا Lambda تعریف میشوند.
اصول شناسایی و مکانیابی ساختارهای مغزی
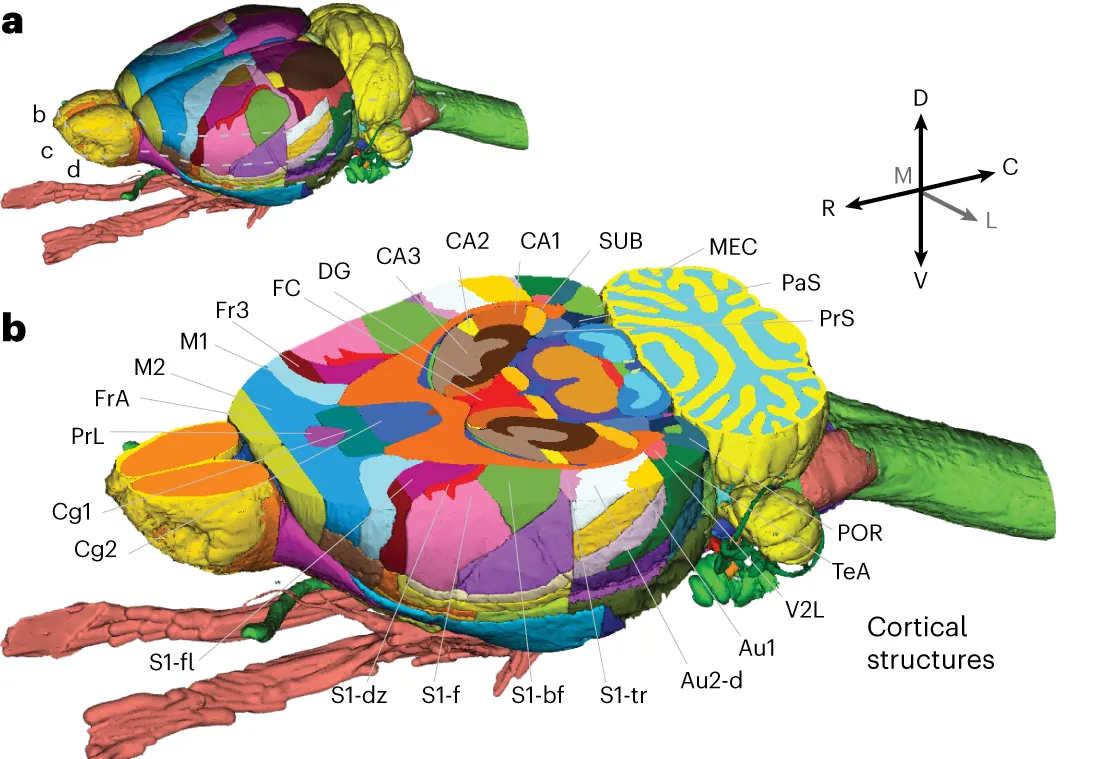
۱. استفاده از نقاط مرجع آناتومیک (Anatomical Landmarks)
در جراحیهای استریوتکسی حیوانات کوچک، ابتدا باید نقاط مرجع ثابت روی جمجمه شناسایی شوند. مهمترین این نقاط:
- Bregma: محل تلاقی بخیههای کرونال و ساژیتال جمجمه. معمولاً به عنوان مبدأ مختصات (۰,۰,۰) استفاده میشود.
- Lambda: محل تلاقی بخیههای ساژیتال و لامبدویید. از آن برای تأیید جهتگیری جمجمه و اصلاح شیب استفاده میشود.
نکته: برای جلوگیری از خطا، باید اطمینان حاصل شود که Bregma و Lambda در یک سطح افقی باشند. شگل زیر محل دقیق این نقاط را بر روی جمجمه نشان می دهد.
۲. سیستم مختصات سهبعدی استریوتکسی
ساختارهای مغزی بر اساس یک سیستم مختصات کارتزین تعریف میشوند:
- Anterior–Posterior (AP): فاصله جلو–عقب نسبت به Bregma.
- Medial–Lateral (ML): فاصله به سمت چپ یا راست خط وسط مغز.
- Dorsal–Ventral (DV): عمق نفوذ از سطح جمجمه یا سطح مغز.
مثال: مختصات AP = -3.0 mm, ML = +2.0 mm, DV = -5.5 mm یعنی ۳ میلیمتر به عقب، ۲ میلیمتر به سمت راست، و ۵٫۵ میلیمتر عمق از Bregma.
۳. استفاده از اطلس مغزی (Brain Atlas)
برای موش و رت، Paxinos & Watson Brain Atlas رایجترین منبع است. این اطلس حاوی:
- تصاویر برشهای متوالی مغز
- مختصات سهبعدی ساختارها
- مقیاس دقیق برای تبدیل فاصله روی جمجمه به موقعیت واقعی ساختار داخلی
کار با اطلس معمولاً شامل:
- پیدا کردن صفحه مورد نظر بر اساس AP
- شناسایی ساختار هدف (مثلاً هیپوکامپ CA1)
- یادداشت کردن ML و DV از اطلس
- وارد کردن مختصات در دستگاه استریوتکسی
۴. کالیبراسیون و بررسی خطای مکانیابی
حتی با مختصات دقیق، عواملی مانند تفاوتهای بین حیوانات، سن یا وزن میتوانند باعث تغییرات جزئی شوند. برای کاهش خطا:
- سطح جمجمه را تراز کنید( Bregma و Lambda همسطح)
- با استفاده از نقاط مرجع اضافی (مانند interaural line) موقعیت را بررسی کنید
- حرکت بازوی دستگاه استریوتکسی را قبل از نفوذ واقعی تست کنید
۵. ارتباط ساختاری–عملکردی
درک اینکه هر ناحیه هدف چه نقشی در پردازش عصبی دارد، مکانیابی را دقیقتر میکند. مثلاً:
- ناحیه موتور اولیه (M1) → کنترل حرکات ارادی
- هیپوکامپ → حافظه و جهتیابی فضایی
- استریاتوم → پردازش پاداش و کنترل حرکات
اهمیت نوروآناتومی در پژوهشهای نوروساینس
۱. هدفگیری دقیق در جراحیها و مداخلات
نوروآناتومی دقیق، نقشه راه جراح است. اگر نواحی مغزی بهدرستی شناسایی نشوند:
- تزریق دارو یا ویروس ژنتیکی ممکن است به ناحیه اشتباه برود.
- ثبت الکتروفیزیولوژی یا تحریک مغزی (مثل DBS) میتواند نتایج گمراهکننده ایجاد کند.
- برداشت بافت برای آنالیز مولکولی/بافتشناسی ممکن است بهجای ناحیه هدف، بخش دیگری را دربر بگیرد.
۲. ارتباط ساختار و عملکرد
پژوهشگران با دانستن محل دقیق ساختارها میتوانند:
- نتایج رفتاری را به تغییرات ساختاری مرتبط کنند.
- اثر مداخلات را در زمینه عملکرد طبیعی آن ناحیه تحلیل کنند. مثلاً:
- آسیب به هیپوکامپ → اختلال حافظه
- تحریک ناحیه V1 → تغییرات ادراک بصری
- تخریب استریاتوم → مشکلات حرکتی مشابه پارکینسون
۳. تفسیر دادههای تصویربرداری و ثبت سیگنال
چه در تصویربرداری MRI و چه در ثبت سیگنالهای ECoG یا LFP، دانستن دقیق جایگاه ساختارها کمک میکند:
- سیگنالها به ناحیه آناتومیک خاص نسبت داده شوند.
- دادهها بین حیوانات یا انسانها با ساختار متفاوت مقایسهپذیر باشند.
- الگوهای فعالیت مغزی به مسیرهای عصبی خاص مرتبط شوند.
۴. طراحی مدلهای بیماری
مدلسازی بیماریهای نورودژنراتیو یا نورولوژیک در حیوانات نیازمند آسیبزدن یا تغییر فعالیت نواحی خاص است:
- مدل پارکینسون → تخریب Substantia Nigra
- مدل آلزایمر → تزریق بتاآمیلوئید به هیپوکامپ
- مدل سکته مغزی → انسداد عروق نواحی حرکتی یا حسی
بدون دانش دقیق از نوروآناتومی، این مدلها غیرقابل اعتماد خواهند بود.
همچنین بخوانید: