اطلاعات عمومی,ویکی ژن
فناوری آنتی سنس در کشف دارو
مقدمهای بر فناوری آنتی سنس در کشف دارو
مفهوم فناوریهای الیگونوکلئوتیدی آنتیسنس مبتنی بر مسدود کردن فعالیت mRNA است که منجر به مهار خاص بیان ژن نامطلوب میشود.
برای مدت طولانی، این به عنوان یک استراتژی ایده آل برای استفاده از دانش جدید ژنومی برای کشف و توسعه دارو در نظر گرفته میشود. در سالهای اخیر، فنآوریهای الیگونوکلئوتیدی آنتیسنس بهطور گسترده بهعنوان ابزاری قوی و امیدوارکننده برای مهار بیان ژن به شیوهای خاص توالی مورد استفاده قرار گرفتهاند.
مکانیسمهای مولکولی الیگونوکلئوتیدهای آنتی سنس
الیگونوکلئوتیدهای آنتی سنس توالی کوتاهی از اسید نوکلئیک هستند که از 7 تا 30 نوکلئوتید تشکیل شده است. آنها میتوانند بر اساس قوانین جفت شدن باز واتسون-کریک به ناحیه خاصی از mRNA هدف متصل شوند و از بیان ژن ناخواسته جلوگیری کنند.
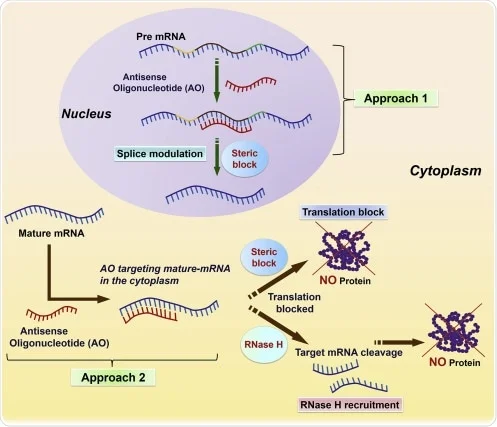
مکانیسم اثری که توسط آن الیگونوکلئوتیدهای آنتی سنس ترجمه mRNA را مهار میکنند بر اساس شیمی الیگونوکلئوتیدها است. به عنوان مثال، اولیگونوکلئوتیدهای متشکل از نواحی DNA مانند فسفودی استر فسفروتیوات و کایمریک از طریق جذب ریبونوکلئاز درون زا H (RNase H)، که یک ریبونوکلئاز در همه جا بیان شده است، ترجیحاً به رشتههای RNA-DNA متصل میشود و رشتههای RNA را آغاز میکند، کار میکنند.
الیگومرهای آنتی سنس اصلاح شده، که از ریبونوکلئاز H مانند اسیدهای نوکلئیک پپتیدی، مورفولینو استفاده نمیکنند، توانایی مهار سنتز پروتئین را از طریق هیبریداسیون در UTR 5′ یا نزدیک کدون شروع AUG دارند، که میتواند مونتاژ ریبوزوم را مسدود کند. آنها همچنین ممکن است زمانی که به اتصالات اینترون-اگزون هیبرید میشوند، اتصال را مهار کنند.
مکانیسمهای عمل الیگونوکلئوتیدهای آنتی سنس باید با مهار مستقیم ژن هدف در سطح RNA یا پروتئین توسط چندین اولیگونوکلئوتید آنتی سنس که علیه مکانهای مختلف روی RNA هدف هدایت میشوند و با عدم مهار توسط چندین اولیگونوکلئوتید کنترل درهم و ناهماهنگ نشان داده شود.
توسعه در شیمی اولیگونوکلئوتید آنتی سنس و روششناسی برای تحویل الیگونوکلئوتیدها به سلولها منجر به نتایج تکرارپذیری شده است که نشان میدهد اولیگونوکلئوتیدهای آنتیسنس مهار قوی و ویژهای از بیان ژن دارند. فناوری آنتی سنس در حال حاضر به عنوان یک فناوری اثبات شده برای توضیح عملکرد ژن هدف و شناسایی اهداف دارویی جدید در نظر گرفته میشود.
آینده فناوریهای الیگونوکلئوتیدی آنتی سنس
در دهه قبل، بهویژه در سال 1996، تنها تعداد انگشت شماری از مولکولهای ضد حس در آزمایشهای بالینی استفاده میشد. از این شش کارآزمایی، پنج کارآزمایی فقط در فاز I بودند. با این حال، در سالهای اخیر، رشد فوقالعادهای در تعداد کارآزماییهای بالینی مرتبط با آنتیسنس وجود داشت.
اداره غذا و دارو (FDA) یک مولکول الیگونوکلئوتید آنتی سنس را برای تجویز موضعی برای درمان رتینیت سیتومگالوویروس (CMV) تایید کرده است، که نشان میدهد داروهای ضد حس میتوانند به طور موثر در درمان بیماریهای موضعی استفاده شوند. تا به امروز، بیش از پنجاه الیگونوکلئوتید آنتی سنس در آزمایشهایی برای بیماریهای مختلف وجود دارد.
اکثر این داروها الیگونوکلئوتیدهایی هستند که برای جلوگیری از بیان ژن از طریق مکانیسم RNase H فرموله شده اند. علاوه بر این، بیش از 30 شرکت بیوتکنولوژی و داروسازی اعلام کردهاند که به درمانهای مبتنی بر RNAi علاقه دارند یا برنامه توسعه دارویی در حال اجرا دارند.
اخیراً، دادههای کارآزمایی بالینی برای این مولکولها که برای درمان کولیت اولسراتیو و لوسمی لنفوسیتی مزمن طراحی شدهاند، نشان دادهاند که اولیگونوکلئوتیدهایی که به صورت تزریقی یا خوراکی تحویل داده میشوند، اثر درمانی خاصی در اهداف خاص خود دارند و اعتبار بیشتری را برای درمان فراهم میکنند. انتظار می رود استفاده از فناوریهای الیگونوکلئوتیدی آنتی سنس در کشف دارو به نیازهای پزشکی برآورده نشده پاسخ دهد. بنابراین، نوید فناوری های الیگونوکلئوتیدی آنتی سنس قوی تر از همیشه است.
همچنین بخوانید:
- دوره مهارت آموزی طراحی دارو
- طراحی دارو چیست؟
- طراحی دارو به کمک کامپیوتر (Computer-Aided Drug Design (CADD)): انواع، موارد استفاده، مثالها و نرمافزارها
- تکنیک دارورسانی یا Drug delivery
مترجم: حنانه بریمانی