اطلاعات عمومی,بیماری ها,ویکی ژن
اسینتوباکتر بومانی (Acinetobacter baumannii): زیستگاه، مورفولوژی، ژنوم، بیماریزایی و درمان
زیستگاه اسینتوباکتر بومانی
- اولین اسینتوباکتر در خاک در سال 1911 توسط W. Beijerinck کشف شد.
- با محیط زیست آبزیان در ارتباط است.
- از خاک، آب، حیوانات و انسان بازیابی شده است.
- در ترشحات تنفسی و اوروفارنکس (Oropharynx) افراد آلوده یافت میشود.
- در محیط بیمارستان یافت میشود و 10 درصد از عفونتهای بیمارستانی در بخش مراقبتهای ویژه را تشکیل میدهد.
- گفته شده است که پوست انسان میتواند منبع عفونتهای شدید مانند باکتریمی (Bacteremia) باشد.
- دستگاه تنفسی، خون، مایع جنب (Pleural)، مجاری ادراری، زخمهای جراحی، CNS، پوست و چشمها ممکن است محلهایی برای عفونت یا کلونیزاسیون باشند.
- اسینتوباکتر بومانی به طور خاص بافتهای مرطوب مانند غشاهای مخاطی یا نواحی از پوست را که در معرض آسیب هستند، چه به صورت تصادفی و چه از طریق جراحت، هدف قرار میدهد.
- اسینتوباکتر بومانی به ندرت به عنوان بخشی از میکروفلور (Microflora) طبیعی پوست یافت میشود. با یک مطالعه تخمین زده شده که تنها 3٪ (حداکثر) از کل میکروفلورها را کلنیهای این باکتری تشکیل میهند.
- بیمارانی که از دستگاههای مصنوعی مانند کاتتر (Catheters)، ابزار بخیه، ونتیلاتور (Ventilator) استفاده کردهاند و افرادی که در ۹۰ روز گذشته تحت دیالیز یا درمان ضد میکروبی قرار گرفتهاند نیز در معرض خطر ابتلا به عفونت اسینتوباکتر بومانی هستند.
- اسینتوباکتر بومانی توانایی تشکیل بیوفیلم (Biofilm) روی سطح لوله تراشه (Endotracheal tube) را دارد که ممکن است سطح نسبتاً بالایی از کلونیزاسیون در قسمت تحتانی دستگاه تنفسی را ایجاد کند.
- اسینتوباکتر بومانی یک پاتوژن هوازی و فرصتطلب میباشد.
- اسینتوباکتر بومانی میتواند هفتهها در یک جسم بیجان زنده بماند.
- مطالعات اخیر نشان دادهاند که اسینتوباکتر بومانی را میتوان در منابع غیرمشکوک مانند غذا یا بندپایان یافت و همچنان منابع دیگری وجود دارند که باید کشف شوند.
- ایزولههای گونههای اسینتوباکتر در انواع مواد غذایی از جمله سبزیجات خام یافت شده است.
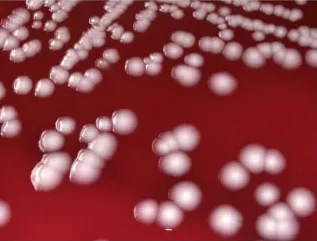
مورفولوژی اسینتوباکتر بومانی
- این باکتری میلهای شکل و گرم منفی بوده که در فاز ساکن (Stationary phase) از مراحل رشد کروی میشود.
- کوکوباسیلاری (Cocobacillary).
- اندازه آن 0.9 تا 1.6 میکرومتر در 1.5 تا 2.5 میکرومتر.
- به صورت جفت یا زنجیرهای جمع میشوند.
- پلئومورفیک (Pleomorphic) هستند.
- غیرمتحرک هستند (ممکن است تحرک انقباضی وجود داشته باشد).
- کپسوله شده هستند.
- غیر اسپورزا (Sporulate) هستند
- این باکتری حاوی پورینها (Porin) و کانالهای افلاکس (efflux) است که به مقاومت در برابر آنتیبیوتیکها کمک میکنند.
ژنوم اسینتوباکتر بومانی
- یک کروموزوم دایرهای منفرد
- جفت باز = 3976747
- کدینگ پروتئین = 3454
- یک سویه از اسینتوباکتر بومانی به نام AYE حاوی یک جزیره مقاومت 86 کیلوبازی به نام AbaR1 است که از 45 ژن مقاومت تشکیل شده است.
- اسینتوباکتر بومانی AYE دارای سه پلاسمید است، اما هیچ کدام حاوی نشانگرهای مقاومت نیستند.
ویژگیهای کشت اسینتوباکتر بومانی
- گونههای اسینتوباکتر باکتریهای اکیداً هوازی، کاتالاز (Catalase) مثبت، ایندول (Indole) منفی و اکسیداز (Oxidase) منفی هستند که عمدتاً کپسوله هستند.
- ابتلا به عفونت اسینتوباکتر بومانی به دلیل توانایی باکتری برای رشد در شرایط مزوترمال (Mesothermal) در دمای 37 درجه سانتیگراد در انسان ایجاد میشود.
- رایجترین محیطها جهت کشت اسینتوباکتر بومانی شامل مککانکی آگار (MacConkey Agar) و بلاد آگار گوسفندی است.
- برای جداسازی انتخابی باکتری، از محیطهای کشت آزمایشگاهی استاندارد مانند تریپتیکاز سوی آگار (Trypticase Soy Agar) و برین هارت اینفیوژن آگار (Brain Heart Infusion Agar) استفاده میشود.
- سویههای محیطی باکتریها میتوانند در طیف وسیعی از دما رشد کنند و برخی از سویههای سایکروفیل (psychrophilic) قادر به رشد در دمای 4 درجه سانتیگراد و برخی از سویههای گرمادوست (Thermophilic) قادر به رشد در دمای 48 درجه سانتیگراد هستند.
- رشد اسینتوباکتر بومانی وابسته به حضور فاکتورهای رشد در محیطهای مصنوعی است.
- توانایی باکتری برای رشد در آگارهای ساده مانند مککانکی آگار به دلیل استفاده از کربنهای آلی و منابع انرژی مختلف است.
- اسینتوباکتر بومانی میتواند از ترکیباتی مانند الکلهای آلیفاتیک (Aliphatic)، اسیدهای آمینه، اسیدهای چرب، قندها و بسیاری از ترکیبات آروماتیک (Aromatic) مقاوم مانند بنزن (Benzene)، سیکلوهگزانول (Cyclohexanol) و 2و3-بوتاندیول (2,3-butanediol) استفاده کند.
- ویژگیهای کشت و الگوهای رشد باکتری به عنوان روشی برای شناسایی اسینتوباکتر بومانی استفاده میشوند.
- نتایج کاتالاز مثبت و اکسیداز منفی به افتراق باکتریها از سایر جنسهای خانواده نایسریاسه (Neisseriaceae) کمک میکند.
- باکتریها از سیستم سیتوکروم (Cytochrome) به عنوان زنجیره انتقال الکترون با مهار فعالیت اکسیداز NADH به وسیله قرار گرفتن در معرض سیانید (Cyanide) استفاده میکنند.
در زیر برخی از ویژگیهای کشت اسینتوباکتر بومانی در محیطهای کشت مختلف آمده است:
الف. نوترینت آگار (Nutrient Agar)
- کلنیهای اسینتوباکتر بومانی در نوترینت آگار نرم و گاهی موکوئیدی به نظر میرسند. کلنیها به رنگ زرد کمرنگ تا سبز با اندازه قطر بین 1تا 2 میلیمتر هستند.
- در مورد نمونههای محیطی، کلنیها نرم با لبههای کامل و سطح برجسته هستند.
ب. مککانکی آگار
- کلنیهای اسینتوباکتر بومانی کوچک، نیمه شفاف و براق هستند که رشد ایزولههای باکتری را روی آگار نشان میدهند.
- بافت کلنیها بسته به منبع جداسازی ممکن است از نظر درجه غلظت از کَره مانند (Butyrous) تا نرم و موکوئیدی متفاوت باشد.
- اندازه کلنیها بین 2 تا 3 میلیمتر است، اما اندازه آنها ممکن است در انکوباسیون طولانی مدت کاهش یابد زیرا کلنیها تمایل به منقبض شدن دارند.
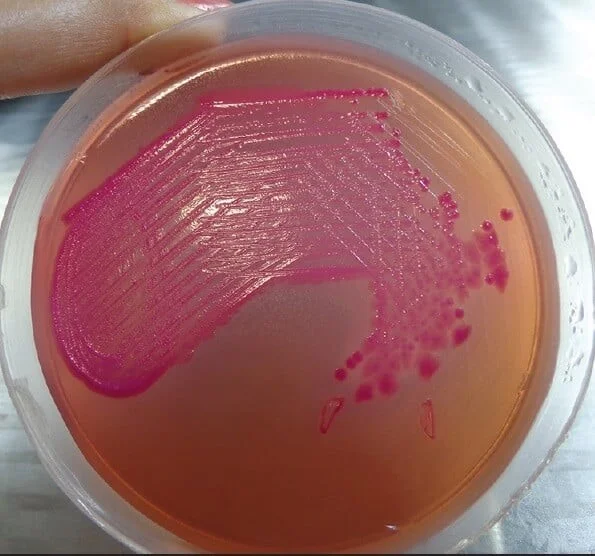
ویژگیهای بیوشیمیایی اسینتوباکتر بومانی
| ویژگیهای اصلی | خواص (اسینتوباکتر بومانی) |
| حلالیت صفرا | منفی (-ve) |
| کپسول | دارای کپسول |
| کاتالاز | مثبت (+ve) |
| سیترات (Citrate) | مثبت (+ve) |
| کواگولاز (Coagulase) | منفی (-ve) |
| تاژک | غیر تاژکدار |
| گاز | منفی (-ve) |
| هیدرولیز ژلاتین (Gelatin) | منفی (-ve) |
| رنگآمیزی گرم (Gram Staining) | منفی (-ve) |
| H2S | منفی (-ve) |
| همولیز (Hemolysis) | منفی (-ve) |
| ایندول (Indole) | منفی (-ve) |
| تحرک | غیر متحرک |
| متیل رد (Methyl Red (MR)) | منفی (-ve) |
| کاهش نیترات (Nitrate Reduction) | منفی (-ve) |
| اکسیداتیو – تخمیری (Oxidative-Fermentative (OF)) | غیر تخمیری (اکسیداتیو) |
| اکسیداز | منفی (-ve) |
| رنگدانه | منفی (-ve) |
| شکل | کوکوباسیلوس |
| اسپور | غیر اسپوردار |
| اورهآز (Urease) | منفی (-ve) |
| وگس پروسکوئر (Voges Proskauer (VP)) | منفی (-ve) |
| تخمیر | |
| دیناز (DNase) | منفی (-ve) |
| گالاکتوز (Galactose) | مثبت (+ve) |
| گلوکز (Glucose) | مثبت (+ve) |
| لاکتات (Lactate) | متغیر (+/-) |
| لاکتوز (Lactose) | عمدتا منفی (-ve)، در برخی موارد مثبت (+ve) |
| مالونات (Malonate) | مثبت (+ve) |
| مالتوز (Maltose) | متغیر (+/-) |
| مانیتول (Mannitol) | منفی (-ve) |
| مانوز (Mannose) | مثبت (+ve) |
| رامنوز (Rhamnose) | مثبت (+ve) |
| ساکارز (Sucrose) | منفی (-ve) |
| زایلوز (Xylose) | مثبت (+ve) |
| واکنشهای آنزیمی | |
| آرژنین دهیدرولاز (Arginine Dehydrolase) | مثبت (+ve) |
| آزلات (Azelate) | مثبت (+ve) |
| بتالاکتاماز (Beta-Lactamase) | مثبت (+ve) |
| هیدرولیز اسکولین (Esculin) | منفی (-ve) |
| هیستامین | منفی (-ve) |
| هیستیدین (Histidine) | مثبت (+ve) |
| لوسین (Leucine) | مثبت (+ve) |
| لیزین (Lysine) | متغیر (+/-) |
| مالات (Malate) | مثبت (+ve) |
| فنیلآلانین دآمیناز (Phenylalanine Deaminase) | مثبت (+ve) |
| هیدرولیز تیروزین (Tyrosine) | مثبت (+ve) |
فاکتورهای بیماریزایی اسینتوباکتر بومانی
- انتقال اسینتوباکتر و متعاقب آن بیمار شدن با سرسختی محیطی ارگانیسم، مقاومت در برابر خشک شدن و فرار از سیستم ایمنی میزبان، تسهیل میشود.
- ویژگیهای بیماری ایجاد شده توسط اسینتوباکتر در درجه اول ناشی از فرار باکتری از پاکسازی سریع توسط سیستم ایمنی ذاتی است، و به طور موثر رشد و ازدحام باکتریایی بالا را ممکن میکند که باعث ایجاد بیماری سپسیس (Sepsis) به واسطه گیرندههای ناقوسیشکل شماره ۴ (Toll-like receptor 4 (TLR4)) جهت شناسایی لیپوپلیساکارید (lipopolysaccharide (LPS)) میشود.
- پلیساکارید کپسولی یک عامل بیماریزای حیاتی است و هنگامی که LPS باعث شوک سپتیک (Septic) میشود، فرار از دستگاه ایمنی را امکانپذیر میکند.
- با این حال محرک اصلی نتایج بالینی، مقاومت آنتیبیوتیکی است.
بیماریزایی اسینتوباکتر بومانی
- نفوذ یک میکروارگانیسم نیاز به چسبندگی سلول به سلول برای ایجاد عفونت دارد.
- با این حال، توانایی اسینتوباکتر بومانی برای چسبیدن به سلولها/ سلولهای مخاطی در مقایسه با سایر میکروارگانیسمها کم است.
- چسبندگی کم و تهاجم اسینتوباکتر بومانی به شدت بیماریزایی کم آن وابسته است. با این حال این باکتری دارای یک توانایی آبگریز است که اتصال به مواد خارجی مانند پلاستیکهای مورد استفاده در دستگاههای درون عروقی را فراهم میکند.
- پروتئین غشای خارجی A (Outer membrane protein A (OmpA)) با بهبود چسبندگی، به ویژه به سلولهای اپیتلیال (Epithelial) دستگاه تنفسی مرتبط است. این پروتئین در میتوکندری و هسته قرار میگیرد و باعث بروز القای آپوپتوز (Apoptosis) مولکول سیتوکروم c شده که منجر به مرگ سلول میشود.
- اسینتوباکتر بومانی با خنثی کردن فاکتور H )یک تنظیمکننده کلیدی مسیر مکمل جایگزین) با کمک OmpA از کشته شدن ناشی از مسیر مکمل جایگزین فرار میکند. این پدیده به مقاومت سرمی اسینتوباکتر بومانی معروف است.
- OmpA باعث تشخیص سلولهای CD4+، فعال شدن و بلوغ سلولهای دندریتیک شده و موجب آپوپتوز زودرس آنها میشود.
- ترشح وزیکولهای غشای خارجی در محل عفونت که حاوی پروتئینهای مختلف مرتبط با بیماریزایی (پروتئاز (Protease)، فسفولیپاز (Phospholipase)، سوپراکسید دیسموتاز (Superoxide dismutase) و کاتالاز) هستند، پاسخ ایمنی ذاتی محلی را تسریع میکند و در نهایت موجب آسیب به بافت میشود.
- وزیکولهای غشای خارجی همچنین تشکیل بیوفیلم را در سطوح آبیوتیک (Abiotic) افزایش میدهند.
- کپسول پلیساکارید نقش اصلی را در محافظت از باکتری در برابر فاگوسیتوز (phagocytosis) توسط سیستم ایمنی ذاتی میزبان ایفا میکند. لیپوپلیساکاریدهای اسینتوباکتر بومانی از یک O- آنتیژن، یک هسته کربوهیدراتی و یک قسمت لیپید A تشکیل شده است. LPS یک عامل کموتاکتیک (Chemotactic) است که سلولهای التهابی را جذب کرده و آنها را وادار میکند تا مواد سیتوتوکسیک (Cytotoxic) خود را آزاد کنند.
- توانایی اسینتوباکتر بومانی برای تشکیل بیوفیلم بر روی سطوح زنده و غیر زنده، یک مکانیسم مقاومتی است که به خوبی مطالعه شده است. برای زنده ماندن در شرایط نامساعد، اسینتوباکتر بومانی از نظر متابولیکی در لایههای عمیقتر بیوفیلم ساکن میشود. نفوذ ضعیف و ناتوانی آنتیبیوتیکها در اثرگذاری بر روی باکتریهای ساکن در بیوفیلم باعث افزایش بیماریزایی آن میشود.
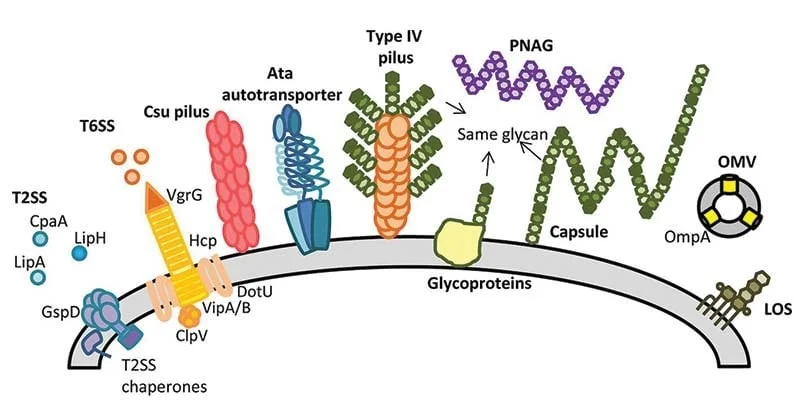
ویژگیهای بالینی اسینتوباکتر بومانی
- شایعترین تظاهرات بالینی عفونت اسینتوباکتر، پنومونی مرتبط با ونتیلاتور و عفونتهای جریان خون است.
- علاوه بر این اسینتوباکتر در انسان میتواند روی پوست، زخمها و مجاری تنفسی و گوارشی، کلنی تشکیل دهد.
پنومونی اکتسابی در بیمارستان
- پنومونی اسینتوباکتر عمدتاً در بیماران بخش مراقبتهای ویژه (ICU) که به ونتیلاتور مکانیکی نیاز دارند، رخ میدهد و معمولاً با ظهور دیرهنگام مشخص میشود.
- سایر تظاهرات بالینی پنومونی اسینتوباکتر مشابه مواردی است که برای پنومونی اکتسابی بیمارستانی به طور کلی گزارش شده است مانند تنگی نفس، سرفه خلطدار، تب، درد قفسه سینه، انبساط نامتقارن قفسه سینه، کاهش رزونانس (Resonance)، اگوفونی (Egophony) و غیره.
پنومونی اکتسابی از جامعه
- پنومونی اسینتوباکتر اکتسابی از جامعه معمولاً توسط یک بیماری شدید با شروع ناگهانی و پیشرفت سریع به نارسایی تنفسی و بیثباتی همودینامیک (Hemodynamic) مشخص میشود.
- شوک سپتیک در حدود یک سوم بیماران ایجاد میشود.
عفونت جریان خون
- اسینتوباکتر 5 تا 2.4 درصد از عفونتهای خونی بیمارستانی را تشکیل میدهد.
- فاکتورهای ریسک ابتلا به عفونت جریان خون آسینتوباکتر شامل بخش مراقبتهای ویژه، ونتیلاتور مکانیکی، جراحی قبلی، استفاده قبلی از آنتیبیوتیکهای طیف وسیع، سرکوب سیستم ایمنی، تروما، سوختگی، بدخیمی، کاتترهای (Catheter) ورید مرکزی، روشهای تهاجمی و اقامت طولانی مدت در بیمارستان میباشد.
- تب ممکن است تنها تظاهر باکتریمی باشد. شوک سپتیک در یک سوم بیماران مبتلا به باکتریمی اسینتوباکتر ایجاد میشود.
اندوکاردیت (Endocarditis)
- گونههای اسینتوباکتر یک علت نادر اندوکاردیت عفونی در قلب طبیعی و پیوندی هستند.
- آسینتوباکتراندوکاردیت (Acinetobacterendocarditis) به طور معمول با یک حمله سریع و با یک دوره پرفشار مشخص میشود.
- مرگ و میر در شرایط اندوکاردیت دریچه قلب طبیعی بیشتر از اندوکاردیت دریچه قلب پیوندی است. این امر احتمالاً به دلیل پایین بودن احتمال عفونت توسط این باکتری است که منجر به تاخیر در درمان در چنین مواردی میشود.
مننژیت (Meningitis)
- اسینتوباکتر یک علت نادر مننژیت بیمارستانی است.
- فاکتورهای ریسک شامل پروسههای جراحی مغز و اعصاب، نشت مایع مغزی نخاعی (Cerebrospinal fluid (CSF))، درمان قبلی با آنتیبیوتیک و خونریزی داخل جمجمه است.
- میزان مرگ و میر بین 20 تا 30 درصد است. نقایص عصبی در بیمارانی که زنده میمانند میتواند شدید باشد.
- اکثر بیماران مبتلا به اسینتوباکترمننژیت (Acinetobactermeningitis) با تب، علائم مننژی و/یا تشنج مراجعه میکنند.
- مایع مغزی نخاعی (CSF) معمولاً پلئوسیتوز (Pleocytosis) را با غلبه بر نوتروفیل (Neutrophilic)، غلظت پروتئین بالا و نسبت CSF به سرم گلوکز پایین، نشان میدهد. سایر تظاهرات بالینی عفونتهای سیستم عصبی مرکزی اسینتوباکتر به طور کلی مشابه موارد گزارش شده برای مننژیت است.
عفونت پوست، بافت نرم و استخوان
- اسینتوباکتر ممکن است زخمهای جراحی و تروماتیک (Traumatic) را آلوده کند و منجر به عفونت شدید بافت نرم شود که میتواند تا استئومیلیت (Osteomyelitis) نیز پیش برود.
- اسینتوباکتر به ندرت با عفونتهای پوستی اکتسابی از بیمارستان یا جامعه مانند سلولیت (Cellulitis) و فولیکولیت(Folliculitis) و همچنین آبسههای پوستی و فاسئیت (Fasciitis) نکروز کننده، مرتبط بوده است.
- عفونتهای زخم تروماتیک ناشی از مقاومت داروئی چند گانه کمپلکس اسینتوباکتر، پس از جراحات به وجود آمده در هنگام جنگ به طور فزایندهای شناخته شده است. به نظر میرسد آلودگی محیطی بیمارستانهای صحرایی نقش مهمی در این عفونتها داشته باشد.
- بیشتر عفونتهای اسینتوباکتر پوست با یک شکاف پوستی شروع میشود. سلولیت بهعنوان یک پینه ادمایی (edema) کاملاً مشخص همراه با اریتما (Erythema) شروع میشود که اغلب ظاهری به رنگ نارنجی دارد. سپس به جراحتی شبیه کاغذ سنباده تبدیل میشود که با وزیکولهای متعدد مشخص میشود و ممکن است بعداً به تاولهای هموراژیک (Hemorrhagic) تبدیل شود.
عفونت مجاری ادراری
- دستگاه ادراری میتواند به آسانی با اسینتوباکتر کلونیزه شود، به ویژه در محل سوندهای ادراری جایگیرنده (Indwelling urinary catheter).
سایر عفونتها
- اسینتوباکتر میتواند باعث کلونیزاسیون یا عفونت چشم شود. ایجاد کلنی توسط باکتری در کسانی که از لنز استفاده میکنند، مشاهده شده است. عفونت چشمی میتواند شامل زخم قرنیه، اندوفتالمیت (Endophthalmitis)، سلولیت (Cellulitis) اطراف چشم و عفونت پس از ترومای نافذ (Penetrating trauma) باشد.
- اسینتوباکتر میتواند باعث سینوزیت بیمارستانی در بیماران بستری در بخش مراقبتهای ویژه شود. تهویه مکانیکی هوا مهمترین عامل مستعد کننده جهت ابتلا به سینوزیت اسینتوباکتر است که با ایجاد پنومونی مرتبط است، زیرا سینوسهای عفونی به عنوان مخزنی جهت پخش عفونت به دستگاه تنفسی تحتانی عمل میکنند.
- آسینتوباکترپریتونیت (Acinetobacterperitonitis) در بیماران تحت دیالیز صفاقی (peritoneal dialysis) نیز یافت شده است. شایع ترین تظاهرات درد شکم و دیالیز کدر است.
تشخیص آزمایشگاهی اسینتوباکتر بومانی
- تشخیص عفونت اسینتوباکتر با کشت اسینتوباکتر با یک نمونه از شخص بیمار (به عنوان مثال، خلط، خون، مایع مغزی نخاعی) در کنار سایر یافتههای بالینی که نشان دهنده عفونت در آن محل است، انجام میشود.
- از آنجایی که کلونیزاسیون اسینتوباکتر رایج و درمان مشکل است و به طور بالقوه با سمیت قابل توجهی همراه است، افتراق بین کلونیزاسیون و عفونت، جهت ارائه درمانی که مخصوص عفونتهای واقعی است، مهم میباشد.
- به عنوان مثال، اسینتوباکتر ایزوله شده از خلط یک بیمار تحت ونتیلاتور، در غیاب تب، لکوسیتوز (Leukocytosis)، افزایش ترشحات تنفسی، نیاز به حمایت تنفسی اضافی، یا یک ناهنجاری جدید در تصویربرداری قفسه سینه، بیشتر نشان دهنده کلونیزاسیون است تا عفونت.
- برای موارد پنومونی، کشتهای کمی یا نیمهکمی بر روی نمونههای خلط نیز ممکن است در تشخیص عفونت و کلونیزاسیون مفید باشند.
نمونهها و مجموعه نمونه
- اسینتوباکتر بومانی از خون، خلط، پوست، مایع جنب و ادرار، معمولاً در عفونتهای مرتبط با وسایلی که روی بیمار نصب میشوند، ایزوله شده است.
خون
- خون را به روش آسپتیک (Aseptic) جمعآوری کنید.
- درپوش لاستیکی بطری کشت خون را با پد الکلی تمیز کنید.
- خون را در بطریهای کشت خون تلقیح کنید.
- تاریخ، نام بیمار و شماره بیمارستان را روی بطریهای کشت خون برچسب بزنید و نمونهها را به آزمایشگاه ارسال کنید.
- بطریهای تلقیح شده را در دمای 37 درجه سانتیگراد یا در دمای اتاق نگهداری کنید.
خلط
- یک ظرف دهانه گشاد استریل با درپوش پیچی به بیمار بدهید.
- از بیمار بخواهید 2 تا 3 بار نفس عمیق بکشد و محکم سرفه کند.
- در ظرف را باز کرده و از بیمار بخواهید خلطش را داخل بطری بریزد. از ریختن ترشحات بزاق یا بینی خودداری کنید.
- برای پردازش بیشتر در ظرف را ببندید.
شستشوی برونکوآلوئولار (Bronchoalveolar Lavage (BAL)) و شستشوی برونشی
- نمونههای برونش را با تزریق حجمهای مختلف محلول نمکی از طریق برونکوسکوپ (Bronchoscope) جمعآوری کرده و به 3 تا 4 قسمت تقسیم کنید.
- مواد مکیده شده را در ظرف دهانه گشاد 40 میلیلیتری یکبار مصرف استریل یا بطریهای استریل بریزید.
- شستشوی برونشها را با مکش مقادیر کم نمک تزریق شده از راههای هوایی بزرگ مجاری تنفسی جمعآوری کنید.
- نمونهها را در ظروف استریل یکبار مصرف 40 میلیلیتری دهانه گشاد یا اگر نمونه در ICU گرفته شده، در بطریهای استریل 100 میلیلیتری نگهداری کنید.
رنگآمیزی گرم (Gram’s staining) را انجام دهید.
گونههای اسینتوباکتر گرم منفی و به شکل کوکوباسیل ظاهر میشوند.
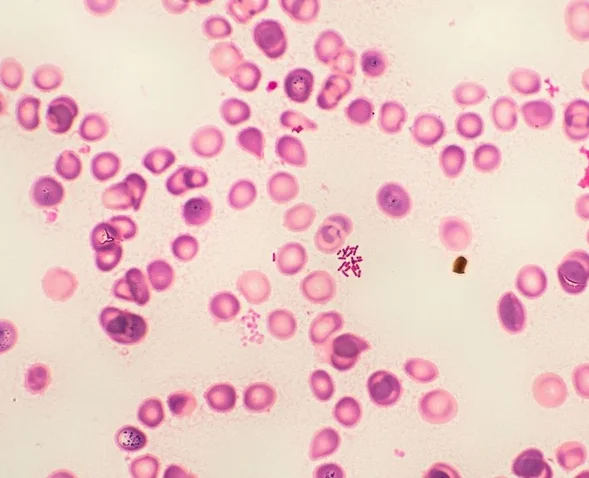
شناسایی اولیه گونههای اسینتوباکتر با روش کشت و تکثیر کشتهای نمونه
- از لولههای جمعآوری شده که کوکوباسیلهای گرم منفی را در رنگآمیزی گرم نشان دادهاند، نمونه برداری کنید.
- نمونهها را با یک لوپ تلقیح یکبار مصرف استریل در نوترینت آگار، مککانکی آگار یا پلیتهای بلاد آگار به صورت رگهای کشت دهید.
- پلیتهای تلقیح شده را در دمای 37 درجه سانتیگراد در شرایط هوازی انکوبه کنید.
- مورفولوژی کلنی بر روی پلیتهای نوترینت آگار، بلاد آگار و مککانکی آگار باید مشاهده و مستند شود.
- در نوترینت آگار، کلنیهای غیر موکوییدی (Mucoid)، مات و دایرهای شکل مشاهده میشود.
- در بلاد آگار، کلنیهای غیر همولیتیک (Hemolytic)، مات، دایرهای و خاکستری رنگ مشاهده خواهد شد.
- در مککانکی آگار، کلنیهای غیر تخمیرکننده لاکتوز، مات و دایرهای مشاهده خواهد شد.
- واکنشهای بیوشیمیایی را برای شناسایی اولیه بررسی کنید.
- تست اکسیداز سیتوکروم (Cytochrome oxidase): منفی
- محیط تحرک مانیتول (Mannitol): غیر تخمیرکننده مانیتول و غیرمتحرک
- آگار قند آهن سهگانه (Triple sugar iron agar): ته لوله و سطح شیبدار قلیایی، بدون تولید H2S یا گاز
- تست ایندول: منفی برای ایندول
- تست استفاده از سیترات: سیترات مثبت
- تست اورهآز: منفی
- مواد بیوشیمیایی را برای شناسایی گونهها اضافه کنید.
- محیط اکسیداتیو تخمیر: استفاده اکسیداتیو از گلوکز
- تست آرژنین دکربوکسیلاز (Arginine decarboxylase): مثبت
- تست کاهش نیترات: منفی
- نتایج را بر اساس کنترلهای مثبت و منفی تفسیر کنید.
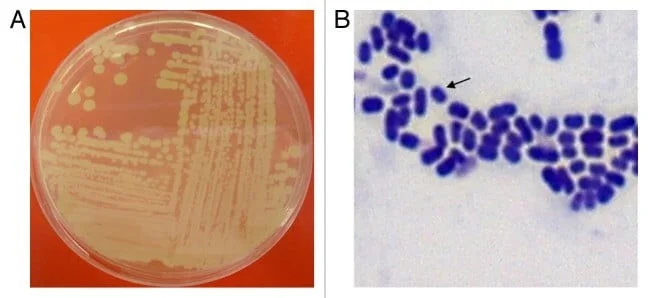
B: رنگآمیزی گرم سلولهای در مرحله تکثیر لگاریتمی (Log-phase) اسینتوباکتر بومانی کشت شده در براث Luria-Bertani؛ فلش یک سلول اسینتوباکتر بومانی را نشان میدهد.
درمان عفونت اسینتوباکتر بومانی
- اگرچه کارباپنمها (Carbapenem) آنتیبیوتیکهای مؤثری برای درمان عفونتهای اسینتوباکتر بومانی هستند، اما میزان ایزولههای اسینتوباکتر بومانی مقاوم به کارباپنم به تدریج در حال افزایش است.
- ایمیپنم (Imipenem) یا سفتازیدیم (Ceftazidime) ترکیب شده با آمینوگلیکوزیدها (Aminoglycosides) برای عفونتهای جدی استفاده میشوند.
- فقط چند گزینه موثر آنتیبیوتیکی برای درمان عفونتهای اسینتوباکتر بومانی MDR موجود است. برای مبارزه با اسینتوباکتر بومانی MDR یا pandrug-resistant (PDR) که به تمام آنتیبیوتیکهای موجود مقاوم هستند، درمانهای ترکیبی از جمله کولیستین (Colistin)/ ایمیپنم، کولیستین/ مروپنم (Meropenem)، کولیستین/ ریفامپیسین (Rifampicin)، کولیستین/ تیژسیکلین (Tigecycline)، کولیستین/ سولباکتام (Sulbactam)، کولیستین/ تئیکو (Teicoplanin) و ایمیپنم/ سولباکتام (Sulbactam) به طور گسترده مورد مطالعه قرار گرفتهاند.
پیشگیری از عفونت اسینتوباکتر بومانی
- اسینتوباکتر میتواند روی پوست زندگی کند و ممکن است برای چند روز در محیط زنده بماند، که پیشگیری از اسینتوباکتر بومانی را به یک موضوع حساس تبدیل کرده است.
- توجه دقیق به روشهای کنترل عفونت، مانند بهداشت دست و تمیز کردن محیط، میتواند خطر انتقال را کاهش دهد.
- در صورتی که پاتوژن MDR باشد، بیماران ایزوله میشوند.
بهداشت دست
بهداشت دست اساسیترین، مؤثرترین و مقرون به صرفهترین استراتژی برای کاهش عفونت متقاطع (Cross-infection) و جلوگیری از گسترش باکتریهای مقاوم است.
احتیاط در تماس با بیماران
- وقتی یک سویه XDR-GNB شناسایی شد، آزمایشگاه میکروبیولوژی باید به روشی به موقع و مطمئن پزشکان را مطلع کند.
- پزشکان ممکن است اقدامات احتیاطی تماسی مانند تخصیص اتاق یک نفره یا جداسازی جزئی با حداقل 1 متر فاصله بین تختها و کاهش استفاده از دستگاههای مشترک را برای بیماران مبتلا به XDR-GNB انجام دهند.
- فشارسنج، گوشی پزشکی، دماسنج، پمپ اینفیوژن و سایر وسایل مربوطه باید به طور اختصاصی برای بیماران مبتلا به عفونت XDR-GNB تهیه شود.
غربالگری فعال
در بخش ICU و سایر بخشهای دارای سویههای بسیار مسری XDR-GNB، بیماران باید از طریق بررسی نمونههای سوابهای پریآنال (Perianal) و مقعدی از نظر CRE و با بررسی ترشح زخم و ناحیه نازوفارنکس (Nasopharyngeal) برای غیر تخمیرکنندههای XDR، غربالگری شوند تا باکتریهای مقاوم بهسرعت از طریق روشهای معمول یا تشخیص سریع شناسایی شوند. بیماران باید به طور مناسب ایزوله شوند.
ضدعفونی سطوح محیطی

- سطوح اشیایی که پرسنل مراقبتهای بهداشتی و بیماران در محیط بیمارستان به طور مکرر با آنها تماس دارند، باید به طور منظم و کامل ضد عفونی شوند.
- برچسبگذاری فلورسانس یا سیستم نظارت بهداشتی ATP میتواند برای نظارت بر اثربخشی فرایند ضدعفونی کردن، استفاده شود تا اطمینان حاصل شود که به طور موثر مانع انتقال سویههای مقاوم میشود.
کلنیزدایی
در بیمارانی که XDR-GNB در بدن آنها کلنی تشکیل داده است، ممکن است شستشوی کل بدن با کلرهگزیدین (Chlorhexidine) و با اسفنج برای کاهش عفونتهای جریان خون مربوط به کاتتر مفید باشد.
همچنین بخوانید:
- باسیلوس سرئوس: زیستگاه، ساختار، درمان و پیشگیری
- باکتری های کلیفرم (Coliform): ویژگیها، نمونهها و روش شناسایی
- کریپتوکوکوس نئوفرمانس: زیستگاه، مورفولوژی، اپیدمیولوژی و درمان
- باسیلوس سوبتیلیس (Bacillus subtilis): یک مرور کلی و کاربردها
مترجم: صادق حسینیکیا





سلام. جنتامایسین و کوتریماکسازول به انسیتو باکتر بومانی مقاوم هستند? یا نه ؟
در حالی که هر دو آنتیبیوتیک ممکن است در برخی موارد علیه Acinetobacter baumannii مؤثر باشند، مقاومت زیادی در این باکتریها وجود دارد. بنابراین، انتخاب دارو برای درمان عفونتهای ناشی از این باکتری باید بر اساس آزمایشهای دقیق حساسیت به آنتیبیوتیکها صورت گیرد. در صورت مواجهه با عفونت Acinetobacter baumannii، مشورت با متخصص عفونی برای تعیین بهترین رویکرد درمانی ضروری است.
امروز پس از ماها کشت خون این باکتری را نشون داده.افراد در تماس با مادرم چه نکاتی را باید رعایت کنیم.تا امروز که بی خبر بودیم امکان سرایت به موجود داره.باید قرنطینه شود.فعلا بیمارستان هستیم