تکنیک ها
کشت ویروس: تکنیک ها، اصول و اهداف
مقدمهای بر کشت ویروس
ویروسها انگلهای داخل سلولی هستند و برای بقای خود به میزبان وابسته هستند. آنها را نمیتوان در محیطهای کشت غیر زنده یا در ظروف آگار به تنهایی پرورش داد، ویروسها به سلولهای زنده برای پشتیبانی از تکثیر خود نیاز دارند.
اهدف اصلی کشت ویروس عبارت است از:
- جداسازی و شناسایی ویروسها در نمونههای بالینی.
- تحقیق در مورد ساختار ویروسی، تکثیر، ژنتیک و اثرات آن روی سلول میزبان.
- آمادهسازی ویروسها برای تولید واکسن
کشت ویروسها را تحت عناوین زیر میتوان مورد بحث قرار داد:
- تلقیح حیوانات
- تلقیح به تخم جنین شده
- کشت سلولی
تلقیح حیوانات
- ویروسهایی را که نمیتوان در تخمهای جنین شده و یا به وسیله کشت بافت رشد داد، میتوان در حیوانات آزمایشگاهی مانند موش، خوکچه هندی، همستر، خرگوش و پستانداران کشت نمود.
- حیوانات انتخاب شده باید سالم و عاری از هرگونه بیماری واگیردار باشند.
- موشهای شیرخوار (کمتر از 48 ساعت سن) بیشتر مورد استفاده قرار میگیرند.
- موشهای شیرخوار به ویروسهای توگاویروس (Togavirus) و کوکساکی (Coxsackie) حساس هستند که از راههای داخل مغزی و داخل بینی تلقیح میشوند.
- ویروسها را میتوان از طریق داخل صفاقی و زیر جلدی نیز تلقیح کرد.
- پس از تلقیح، ویروس در میزبان تکثیر شده و بیماری ایجاد میکند. حیوانات جهت بررسی علائم بیماری و مرگ زیر نظر گرفته میشوند.
- سپس ویروس از بافت این حیوانات جدا و پالایش میشود.
- برای اولین بار تلقیح زنده بر روی داوطلبان انسانی برای مطالعه ویروس تب زرد استفاده شد.
مزایای کشت ویروس به روش تلقیح حیوانات
- تشخیص، بیماریزایی و علائم بالینی ویروس مشخص میشود.
- تولید آنتی بادی قابل شناسایی است.
- در جداسازی اولیه ویروسهای خاص کمک میکند.
- موشها مدل قابل اعتمادی برای مطالعه تکثیر ویروس ارائه میدهند.
- برای مطالعه پاسخهای سیستم ایمنی، اپیدمیولوژی (Epidemiology) و انکوژن (Oncogenesis) استفاده میشود.
معایب کشت ویروس به روش تلقیح حیوانات
- گرانی و مشکلات نگهداری از حیوانات.
- مشکل در انتخاب حیوانات مناسب برای یک ویروس خاص
- برخی از ویروسهای انسانی نمیتوانند در حیوانات رشد کنند، یا میتوانند رشد کنند اما باعث بیماری نمیشوند.
- موشها مدلهایی برای تولید واکسن ارائه نمیدهند.
- تلقیح حیوانات منجر به ایجاد نسلی از ویروسهای جهش یافته میشود.
- مسائل مربوط به سیستمهای رفاه حیوانات.
تلقیح به تخم جنین شده
- Goodpasture در سال 1931 برای اولین بار از تخم مرغ جنین شده برای کشت ویروس استفاده کرد.
- فرایند کشت ویروسها در تخمهای جنینی بستگی به نوع تخمی دارد که استفاده میشود.
- ویروسها به جنین جوجه 12-7 روزه تلقیح میشوند.
- باید تخمها را برای تلقیح جهت کشت آماده کرد. ابتدا سطح پوسته را با ید ضد عفونی میکنند و با یک مته کوچک استریل آن را سوراخ میکنند.
- پس از تلقیح، سوراخ تخم با ژلاتین یا پارافین بسته شده و در دمای 36 درجه سانتیگراد به مدت 2-3 روز انکوبه میشود.
- پس از انکوباسیون، تخم شکسته شده و ویروس از بافت تخم جدا میشود.
- رشد و تکثیر ویروس در جنین تخمک با مرگ جنین، آسیب سلولی جنین، یا با تشکیل جوشها یا جراحتهای معمولی روی غشای تخم مشخص میشود.
- ویروسها را میتوان در قسمتهای مختلف تخم مانند غشای کوریوآلانتوئیک (Chorioallantoic membrane (CAM))، حفره آلانتوئیس (Allantoic cavity)، کیسه آمنیوتیک (Amniotic sac) و کیسه زرده (yolk sac) کشت کرد.
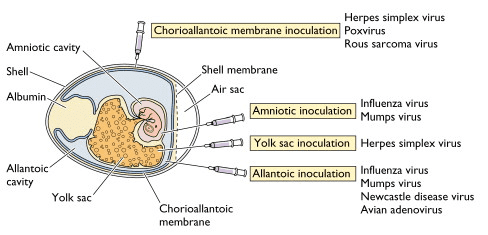
- غشای کوریوآلانتوئیک:
- تلقیح در این قسمت، عمدتاً برای رشد ویروس آبله است.
- پس از انکوباسیون، جراحات قابل مشاهدهای به نام پوک (Pock) دیده میشود که نقاط سفید و خاکستری در قسمت شفاف CAM هستند.
- ویروس هرپس سیمپلکس (Herpes simplex) نیز در CAM رشد میکند.
- یک ویروس باعث ایجاد یک پوک میشود.
- تلقیح در CAM برای مطالعه بر روی پلاکها (Plaque) نیز مناسب است.
- حفره آلانتوئیس:
- تلقیح در این قسمت عمدتاً برای تولید واکسن ویروس آنفلوانزا، تب زرد و هاری انجام میشود.
- اکثر ویروسهای پرندگان را میتوان با استفاده از تلقیح در این قسمت کشت کرد.
- کیسه آمنیوتیک:
- تلقیح در این قسمت عمدتاً برای جداسازی اولیه ویروس آنفولانزا و ویروس اوریون انجام میشود.
- در این روش، رشد و تکثیر ویروس در جنین تخم با آزمایش هماگلوتیناسیون (haemagglutination) قابل تشخیص است.
- تلقیح کیسه زرده:
- تلقیح در این قسمت سادهترین روش برای رشد و تکثیر ویروس است.
- برای کشت برخی ویروسها و برخی باکتریها (کلامیدیا (Chlamydia) و ریکتزیا(Rickettsiae)) تلقیح در این قسمت انجام میشود.
- مکانیسمهای درگیری سیستم ایمنی در کشت اکثر ویروسهای پرندگان با تلقیح در این قسمت قابل تشخیص است.
مزایای تلقیح در تخم جنین شده
- روشی پرکاربرد برای رشد و جداسازی ویروس میباشد.
- بستری ایدهآل برای رشد و تکثیر ویروس است.
- قابلیت جداسازی و کشت بسیاری از ویروسهای پرندگان و تعداد کمی از پستانداران در این روش وجود دارد.
- مقرون به صرفه بوده و نگهداری آن بسیار آسانتر است.
- نیروی کار کمتری نیاز است.
- تخمهای جنین شده به راحتی در دسترس هستند.
- استریل بوده و طیف وسیعی از بافتها و مایعات وجود دارد.
- تخم جنین شده عاری از باکتریهای آلوده کننده و بسیاری از ویروسهای پنهان میباشد.
- عوامل دفاعی اختصاصی و غیر اختصاصی در تخمهای جنینی دخیل نیستند.
- تلقیح در تخم جنین شده به طور گسترده برای رشد ویروس جهت تولید برخی واکسنها استفاده میشود.
معایب تلقیح در تخم جنین شده
- محل تلقیح برای ویروسهای مختلف، متفاوت است. یعنی هر ویروسی به مکانهای متفاوتی برای رشد و تکثیر خود نیاز دارد.
کشت سلولی (کشت بافت)
سه نوع کشت بافت وجود دارد. کشت اندام، کشت ریزنمونه و کشت سلولی.
کشتهای اندام عمدتاً برای انگلهای مربوط به اندامهای خاص انجام میشود. برای مثال کشت حلقه نای برای جداسازی ویروس کرونا انجام میشود.
کشت ریزنمونه به ندرت انجام میشود.
کشت سلولی بیشتر برای شناسایی و تکثیر ویروسها استفاده میشود.
- کشت سلولی فرآیندی است که طی آن سلولها تحت شرایط کنترل شده، رشد میکنند.
- سلولها در شرایط آزمایشگاهی روی شیشه یا یک سطح پلاستیکی در یک محیط رشد مناسب کشت میشوند.
- در ابتدا یک محیط رشد که معمولاً محلول نمک متعادل حاوی 13 اسید آمینه، قند، پروتئین، نمک، سرم گوساله (Calf serum)، بافر، آنتیبیوتیک و فنول رد (Phenol red) میباشد، تهیه شده و بافت یا سلول میزبان در آن تلقیح میشود.
- در انکوباسیون، تقسیم سلولی انجام و روی سطح شیشه پخش میشود تا یک تک لایه سلولی یکنواخت (Confluent monolayer) تشکیل شود.
انواع کشت سلولی
- کشت سلولی اولیه:
- این سلولها، سلولهای طبیعی هستند که از سلولهای حیوانی یا انسانی به دست میآیند.
- این سلولها فقط برای مدت محدودی قادر به رشد هستند و نمیتوان آنها را در محیط کشت سریالی حفظ کرد.
- از این سلولها برای جداسازی اولیه ویروسها و تولید واکسن استفاده میشود.
برای مثال میتوان به کشت سلول کلیه میمون یا کشت سلول آمنیون انسانی اشاره کرد.
- کشت سلولی دیپلوئید یا Diploid (خطوط سلولی نیمه پیوسته):
- این سلولها دیپلوئید هستند و تعداد کروموزومهای مشابه سلولهای والد را دارند.
- این سلولها را میتوان تا 50 بار به وسیله انتقال سریالی قبل از اینکه سویه سلولی از بین برود، زیر کشت داد.
- از این سلولها برای جداسازی برخی از ویروسهای سختپسند (Fastidious) و تولید واکسنهای ویروسی استفاده میشود.
- برای نمونه میتوان به سویه ریه جنینی انسان و سویه سلولی جنینی میمون Rhesus اشاره کرد.
- کشت هتروپلوئید یا Heteroploid (خطوط سلولی پیوسته):
- این سلولها از سلولهای سرطانی مشتق شدهاند.
- از آنجا که آنها را میتوان به طور نامحدود به صورت سریالی کشت کرد، به عنوان ردههای سلولی پیوسته نامگذاری میشوند.
- آنها را میتوان با زیرکشتهای سریالی یا با نگهداری در انجماد عمیق در دمای 70- درجه سانتی گراد حفظ کرد.
- به دلیل مشتق شدن از سلولهای سرطانی برای تولید واکسن مفید نیستند.
- نمونهها: HeLa (سرطان سلولی دهانه رحم انسانی)، HEP-2 (Humman Epithelioma مربوط به رده سلولی حنجره)، ردههای سلولی کلیه Vero (میمون Vervet)، BHK-21 (رده سلولی کلیه بچه همستر).
نمونههای خطوط سلولی حساس
- هرپس سیمپلکس (Herpes Simplex) Vero Hep-2، دیپلوئید انسانی ( HEK و HEL)، آمنیون انسانی
- دیپلوئید انسانی ویروس واریسلا زوستر (VZV) (HEL, HEK)
- فیبروبلاستهای دیپلوئید انسانی سیتومگالوویروس(CMV)
- آدنوویروس (Adenovirus) Hep2، HEK
- فلج اطفال MK، BGM، LLC-MK2، دیپلوئید انسانی، Vero، Hep-2
- رادویوسارکوم (Rhadomyosarcoma)
- کوکساکی (Coxsackie) B MK، BGM، LLC-MK2، vero، hep-2
- اکو (Echo ) MK، BGM، LLC-MK2، دیپلوئید انسانی، Rd
- آنفولانزای A MK، LLC-MK2، MDCK
- آنفلوانزای B MK، LLC-MK2، MDCK
- پاراآنفلوآنزا (Parainfluenza) MK، LLC-MK2
- اوریون (Mumps) MK، LLC-MK2، HEK، Vero
- سین سی شیال تنفسی (RSV) Hep-2، Vero
- راینوویروس (Rhinovirus) دیپلوئید انسانی (HEK, HEL)
- سرخک MK، HEK
- سرخجه Vero، RK13
مزایای کشت سلولی
- سهولت نسبی، طیف گسترده، ارزانتر و میزان حساسیت
مضرات کشت سلولی
- این فرآیند به تکنسینهای آموزش دیده با تجربه و به صورت تمام وقت نیاز دارد.
- آزمایشگاههای دولتی و آزمایشگاههای بیمارستانی، ویروسها را در کارهای بالینی جداسازی و شناسایی نمیکنند.
- بافت یا سرم برای تجزیه و تحلیل جهت شناسایی ویروس باید به آزمایشگاههای مرکزی فرستاده شود.
کشت ویروسهای گیاهی و باکتریوفاژها (bacteriophage)
کشت ویروسهای گیاهی
روشهایی برای کشت ویروسهای گیاهی وجود دارد که میتوان به کشت بافت گیاهی، کشت سلولهای جدا شده یا کشت پروتوپلاستها (Protoplast) و … اشاره کرد. ویروسها را میتوان در کل قسمتهای گیاه کشت داد.
برگها به صورت مکانیکی به وسیله مالش آن با ترکیبی از ویروسها و یک ساینده تلقیح میشوند. هنگامی که دیواره سلولی توسط ساینده شکسته میشود، ویروسها مستقیماً در تماس با غشای پلاسما قرار میگیرند و سلولهای میزبان در معرض را آلوده میکنند. یک ضایعه نکروز موضعی اغلب به دلیل مرگ سریع سلولها در ناحیه عفونی ایجاد میشود. برخی از ویروسهای گیاهی تنها در صورتی قابل انتقال هستند که قسمت آلوده به گیاه سالم پیوند زده شود.
کشت باکتریوفاژها
باکتریوفاژها در کشتهای براث یا آگار (Broth or Agar) مربوط به سلولهای باکتریایی جوان و فعال در حال رشد، کشت میشوند.
مطالب مرتبط با کشت ویروس:
کشت سلولی چیست؟ | کشت سلول و کاربردهای آن
مترجم: فاطمه فریادرس




درود وقتتون بخیر،من میخوام شرایط رشد و تکثیر و phمحیطی برای ویروس واریسلا زوستر رو بدونم،ممنون میشم راهنماییم کنید،برای ارائه ام احتیاج دارم
شرایط رشد و تکثیر ویروس واریسلا زوستر
1. سلولهای میزبان
سلولهای فیبروبلاست انسانی: VZV معمولاً در کشتهای سلولی فیبروبلاست انسانی تکثیر مییابد.
سلولهای Vero: سلولهای مشتق شده از کلیه میمون سبز آفریقایی که برای کشت ویروسهای مختلف از جمله VZV استفاده میشوند.
2. دمای کشت
دمای مناسب: ویروس VZV به دمای 37 درجه سانتیگراد (دمای بدن انسان) برای رشد و تکثیر نیاز دارد.
3. محیط کشت
محیط کشت سلولی: برای کشت سلولهای میزبان، معمولاً از محیطهای کشت استاندارد مانند DMEM (Dulbecco’s Modified Eagle Medium) یا RPMI 1640 استفاده میشود که با سرم جنین گاوی (Fetal Bovine Serum یا FBS) غنی شده است.
آنتیبیوتیکها: برای جلوگیری از آلودگیهای باکتریایی، معمولاً به محیط کشت آنتیبیوتیکها (مانند پنیسیلین و استرپتومایسین) اضافه میشود.
pH محیطی مناسب
pH مطلوب: محیط کشت باید دارای pH حدود 7.2 تا 7.4 باشد، که با شرایط فیزیولوژیکی بدن انسان مطابقت دارد. pH محیط کشت معمولاً با استفاده از بافرهایی مانند بیکربنات سدیم تنظیم میشود.
نکات کلیدی برای کشت ویروس واریسلا زوستر
انکوباسیون در CO2: سلولهای کشت شده باید در انکوباتور CO2 (معمولاً با 5% CO2) قرار داده شوند تا pH محیط کشت ثابت بماند.
مانیتورینگ سلولی: سلولهای کشت شده باید به طور منظم برای بررسی تکثیر ویروس و تشخیص اثرات سیتوپاتیک (Cytopathic Effects یا CPE) مانند تغییرات مورفولوژیکی سلولها، تحت مانیتورینگ قرار گیرند.
تعداد پاساژها: برای حفظ ویروس و جلوگیری از موتاسیونهای غیرضروری، تعداد پاساژهای سلولی باید محدود باشد.