اطلاعات عمومی,کشت سلول,ویدیو های آموزشی,ویکی ژن
کاربردهای کشت سلولی در تحقیقات و تشخیص
مقدمهای بر کاربردهای کشت سلولی در تحقیقات و تشخیص
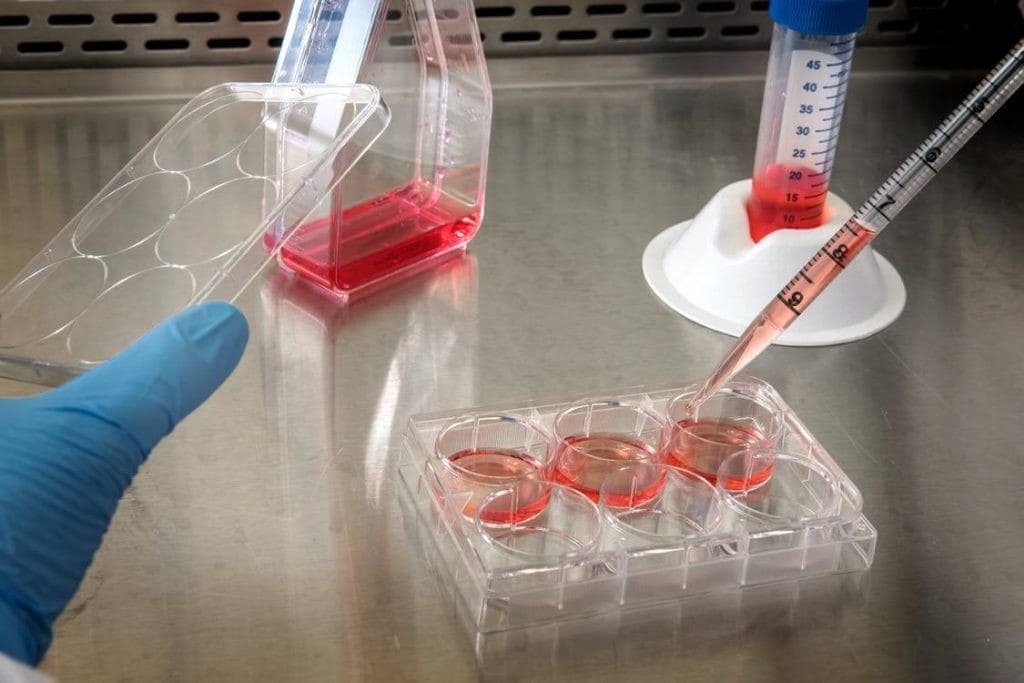
کشت سلولی- فرایند رشد سلولها در شرایط کنترلشده خارج از محیط طبیعیشان- به یکی از ارکان اصلی زیستشناسی نوین، زیستفناوری و پزشکی تبدیل شده است. از زمان نخستین کشت موفق سلولهای انسانی (سلولهای HeLa) در دهه ۱۹۵۰، استفاده از کشت سلولی بهطور چشمگیری گسترش یافته است.
امروزه، تکنیکهای کشت سلولی نهتنها در تحقیقات پایه بلکه در روشهای تشخیصی، توسعه دارو، مطالعات سرطان، تولید واکسن و پزشکی فردمحور نقش کلیدی ایفا میکنند.
این مقاله به بررسی کاربردهای گسترده کشت سلولی در حوزههای پژوهشی و تشخیصی میپردازد و همچنین روشها، انواع کشتها و چشماندازهای آینده این حوزه را مرور میکند.
کشت سلولی چیست؟
کشت سلولی به نگهداری و تکثیر سلولها در شرایط آزمایشگاهی (درون شیشهای یا in vitro) اطلاق میشود؛ سلولها میتوانند از منابع زیر کشت داده شوند:
- بافتهای اولیه (مانند پوست، کبد یا تومور)
- ردههای سلولی پایدار (مانند HeLa، HEK293، CHO)
- سلولهای بنیادی (بنیادی جنینی یا بالغ)
برای رشد مناسب، سلولها در محیطی حاوی مواد مغذی قرار میگیرند و شرایطی از جمله دمای مناسب (معمولاً ۳۷ درجه سانتیگراد)، pH در محدوده حدودی 7.2 تا 7.4 و میزان CO₂ (معمولاً 5%) برای آنها فراهم میشود.

انواع کشت سلولی
-
کشت سلولهای اولیه:
- مستقیماً از بافتها استخراج میشوند؛
- بهخوبی فیزیولوژی درونبدنی (in vivo) را تقلید میکنند؛
- عمر محدودی دارند (تعداد تقسیمهای محدود).
-
ردههای سلولی پایدار (مداوم):
- سلولهای تغییریافته یا سرطانی؛
- توانایی تقسیم نامحدود؛
- بهطور گسترده در آزمایشهای بلندمدت استفاده میشوند.
-
کشت سهبعدی و ارگانوئیدها:
- ساختار و عملکرد بافت را بهتر از کشتهای دوبعدی تقلید میکنند.
- در مهندسی بافت، پژوهشهای سرطان و تست های دارویی کاربرد دارند.
-
کشت سلولهای بنیادی:
- شامل سلولهای پرتوان یا چندتوان؛
- توانایی تمایز به انواع مختلف سلول را دارند؛
- برای پزشکی بازساختی و مدلسازی بیماریها استفاده میشوند.
ملزومات و تجهیزات پایه برای کشت سلولی
- هود لامینار (کابین ایمنی زیستی): برای کار استریل و جلوگیری از آلودگی؛
- انکوباتور CO₂: برای حفظ دما، رطوبت و تعادل گازها (معمولاً ۳۷ درجه و 5% CO₂)؛
- میکروسکوپ: جهت مشاهده شکل ظاهری و وضعیت سلولها؛
- ظروف کشت: مانند فلاسک، پلیت و پتری دیش؛
- محیط کشت: مانند DMEM، RPMI، MEM همراه با مکملهای تغذیهای؛
- تریپسینEDTA/: برای جدا کردن سلولهای چسبیده به سطح؛
- پیپت، سانتریفیوژ و تجهیزات انجماد: برای جابجایی، جداسازی و نگهداری سلولها در دمای پایین (Cryopreservation)
کاربردهای کشت سلولی در پژوهش
-
زیستشناسی سرطان
کشت سلولی به پژوهشگران این امکان را میدهد که رفتار سلولهای سرطانی را بررسی کنند، داروهای ضدسرطان را آزمایش کنند و مکانیسمهای پیشرفت تومور، متاستاز و مقاومت دارویی را بشناسند. برای مثال، ردههای سلولی سرطان پستان انسانی مانند MCF-7 یا مدلهای سهگانه منفی* مانند MDA-MB-231 برای مطالعه انواع مختلف تومورها استفاده میشوند.
* مدلهای سهگانه منفی به مدلهایی از سرطان سینه گفته میشود که سلولهای سرطانی آنها فاقد سه نوع گیرنده مهم هستند: گیرنده استروژن (ER)، گیرنده پروژسترون (PR) و HER2 این نوع سرطان به درمانهای هورمونی و هدفمند مقاوم است و برای مطالعه آن از مدلهای خاص مانند MDA-MB-231 استفاده میشود.
-
توسعه و غربالگری داروها
شرکتهای داروسازی از سلولهای کشتشده به منظور:
- بررسی اثربخشی و سمیت دارو در محیط in vitro پیش از آزمایشهای حیوانی یا انسانی؛
- انجام غربالگریهای گسترده با استفاده از سیستمهای رباتیک؛
- ارزیابی رابطه دوز-پاسخ و مکانیسم عملکرد داروها؛
سلولهایی مانند HEK293 (کلیه)،CHO (تخمدان همستر چینی) و HepG2 (کبد) بهطور گسترده در این حوزهها استفاده میشوند.
-
پژوهشهای مولکولی و ژنتیکی
کشت سلولی پایهای به منظور موارد زیر صورت می گیرد:
- مطالعه بیان ژن، ترنسفکشن و ویرایش ژن با CRISPR؛
- تولید پروتئینهای نوترکیب (مانند انسولین یا آنتیبادیها)؛
- بررسی مسیرهای پیامرسانی و تنظیم رونویسی؛
- سلولها میتوانند بهصورت ژنتیکی دستکاری شوند و با تکنیکهایی مانند RT-PCR، وسترن بلات، تستهای گزارشگر و میکروسکوپ تحلیل شوند.
-
سلولهای بنیادی و پزشکی بازساختی
سلولهای بنیادی جنینی و القایی (iPSCs) برای:
- درک مراحل اولیه رشد؛
- مدلسازی بیماریهای ژنتیکی در محیط آزمایشگاهی؛
- تولید سلولهای بافت های خاص مانند نورونها، سلولهای قلبی و کبدی؛
- فراهم کردن زیرساخت درمانهای سلولی در بیماریهایی مانند پارکینسون، دیابت و آسیب نخاعی کشت داده میشوند.
-
ایمونولوژی و پژوهشهای واکسن
سلولهای ایمنی (مانند ماکروفاژها، لنفوسیتها) برای:
- مطالعه پاسخهای سایتوکاینی، سیگنالدهی ایمنی و تعاملات میزبان-پاتوژن؛
- بررسی فعالسازی و عملکرد سلولهای ایمنی؛
- پشتیبانی از تولید واکسنها از جمله واکسنهای ویروسهایی مانند فلج اطفال، آنفلوآنزا و کووید-۱۹ (با استفاده از ردههایVero یا MDCK) کشت داده میشوند.
-
سمشناسی و مطالعات زیستمحیطی
سیستمهای کشت سلولی جایگزینی اخلاقی و مقرونبهصرفه برای تست های حیوانی هستند. در این مطالعات، سلولها در معرض سموم یا ترکیبات شیمیایی قرار میگیرند و عواملی مانند زندهمانی سلولی، آپوپتوز، تولید گونههای فعال اکسیژن (ROS) و آسیب DNA مورد ارزیابی قرار میگیرند.
کاربردهای کشت سلولی در تشخیص بالینی
-
سیتوژنتیک و تحلیل کروموزومی
لنفوسیتهای خون محیطی یا سلولهای مغز استخوان برای موارد زیر کشت داده میشوند:
- بررسی کاریوتایپ برای شناسایی ناهنجاریهای کروموزومی (مانند تریزومی ۲۱، سندرم ترنر)؛
- تشخیص جابجاییهای ساختاری (مانند ترنسلوکیشنها در لوسمی)؛
- پشتیبانی از تشخیصهای پیش از تولد از طریق کشت مایع آمنیوتیک.
-
ویروسشناسی و جداسازی ویروس
ردههای سلولی مانند Vero، HeLa و MDCK برای کشت و شناسایی ویروسها به کار میروند. این فرایند برای موارد زیر ضروری است:
- تشخیص عفونتهای ویروسی (مانند هرپس، سایتومگالوویروس، آنفلوآنزا)؛
- مشاهده اثرات سیتوپاتیک (CPE) زیر میکروسکوپ؛
- تعیین بار ویروسی از طریق تستهایی مانند plaque assay یا روش TCID₅₀
-
تشخیصهای میکروبی و آزمایشهای ضدمیکروبی
- کشت سلولی برای بررسی تأثیر سموم باکتریایی یا قارچی استفاده میشود؛
- مدلهای همکشت برای شبیهسازی تعامل میزبان-میکروب بهکار میروند؛
- برخی آزمایشگاههای تشخیص از سلولهای اپیتلیالی کشتشده برای بررسی سمیت آنتیبیوتیکها استفاده میکنند.
-
آزمایشهای حساسیتزایی و آلرژی
سلولهای ایمنی مشتقشده از بیمار میتوانند کشت داده شوند و در معرض آلرژنها یا داروها قرار گیرند تا:
- واکنشهای حساسیت دیررس (DTH) بررسی شوند؛
- واکنشپذیری سلولهای T در بیماریهای خودایمنی یا واکنشهای ناخواسته دارویی تحلیل شود.
-
پزشکی فردمحور و آزمایش حساسیت دارویی
در حوزه سرطان سلولهای توموری استخراجشده از بیمار میتوانند در مدلهای PDX یا کشتهای سهبعدی نگهداری شوند تا انواع مختلف داروهای شیمیدرمانی روی آنها آزموده شوند و مؤثرترین درمان پیشبینی گردد؛ این امر گامی مهم در مسیر پزشکی دقیق (precision medicine) بهشمار میآید.
مزایای کشت سلولی
- فراهمکردن محیطی کنترلشده برای انجام آزمایشها؛
- قابلیت تکرارپذیری نتایج در آزمایشگاهها و مطالعات مختلف؛
- کاهش نیاز به استفاده از حیوانات (جایگزینی آزمایشهای in vitro)؛
- دسترسی آسان برای دستکاریهای ژنتیکی؛
- امکان مشاهده فرایندهای سلولی بهصورت زنده و در لحظه؛
- مقیاسپذیری بالا برای کاربردهای صنعتی و بالینی.

محدودیتها و چالشهای کشت سلولی
- خطر آلودگی (قارچی، باکتریایی، مایکوپلاسما)؛
- از دست رفتن فنوتیپ یا رانش ژنتیکی در کشتهای بلندمدت؛
- تقلید ناقص محیط واقعی بدن در مدلهای دوبعدی؛
- نیاز به مهارت فنی و هزینه برای حفظ شرایط استریل؛
- دغدغههای اخلاقی در مورد استفاده از سلولهای بنیادی جنینی.
برای غلبه بر این چالشها و شبیهسازی دقیقتر شرایط فیزیولوژیک روشهای پیشرفتهای مانند همکشت (co-culture)، داربستهای سهبعدی (3D scaffolds) و سیستمهای « ارگان روی تراشه (organ-on-a-chip)» در حال توسعه هستند.
چشماندازهای آینده
با پیشرفت فناوری کشت سلولی بهسوی روشهایی پیشرفتهتر، خودکارتر و شخصیسازیشدهتر حرکت میکند. حوزههای نوظهور شامل موارد زیر هستند:
- استفاده از هوش مصنوعی برای پایش و پیشبینی شرایط کشت؛
- مدلهای ارگانوئیدی برای بهبود فرایند کشف دارو؛
- پرینت زیستی بافتها برای کاربرد در پیوندهای بافتی؛
- حسگرهای مبتنی بر سلول برای تشخیصهای لحظهای و دقیقتر.
نتیجهگیری
کشت سلولی ابزاری ضروری در علوم زیستی است که بینشهای بیسابقهای در مورد عملکرد سلولی، مکانیسمهای بیماری و واکنشهای درمانی فراهم میآورد. از تحلیل مسیرهای مولکولی در آزمایشگاهها تا تشخیص ناهنجاریهای کروموزومی یا کشت ویروسها در بیمارستانها، کاربردهای آن متنوع و در حال گسترش است.
با حرکت به سمت آیندهای که توسط پزشکی فردمحور، درمانهای بازساختی و زیستشناسی مصنوعی شکل میگیرد، نقش کشت سلولی اهمیت بیشتری پیدا خواهد کرد که آن را نه تنها به یک تکنیک، بلکه به یک پلتفرم اساسی برای زیستشناسی مدرن و نوآوریهای بالینی تبدیل میکند.
همچنین بخوانید: