دستهبندی نشده
کاربرد های ایمونوانفورماتیک
مقدمهای بر کاربرد های ایمونوانفورماتیک
امروزه چالش های زیادی در زمینه ی رشته های علوم پایه و بالینی به منظور ارائه ی استراتژی های هدفمندتر برای مبارزه و شناسایی بیماری های خطرناک عفونی و غیر عفونی پدیدار شده است. چنین استراتژی هایی می توانند به طراحی های مدرن واکسن ها، کیت ها، آنتی بادی ها، ادجوانت ها یا مواد بیولوژیکی و شیمیایی فعال منجر شوند.
واکسن ها غالبا با یک تزریق غیرفعال یا تضعیف شده ی ایزوله توسعه می یابند. اگرچه چنین واکسن هایی در بیشتر جنبه ها موفق بوده اند اما برای برخی ارگانیسم ها و شرایط با شکست مواجه شده اند و مناسب نمی باشند. واکسن های تولید شده به روش های فوق تنوع ژنتیکی و فنوتیپی و همچنین پلی مورفیسم پاتوژن ها و میزبان مثل ژن های پیچیده ی MHC را در نظر نمی گیرند.
این واکسن ها محدودیت هایی همچون ایجاد ایمنی ناکافی در برابر طیف گسترده ای از ویروس هایی دارند که بیش از حد متغیر هستند. از جمله ی این ویروس ها می توان به آنفولانزا، ویروس نقص ایمنی انسان (HIV)، ویروس هپاتیت C (HCV) و ویروس عفونی برونشیت (IBV) اشاره نمود. برخی دیگر از موجودات که با همین مشکل مواجه هستند شامل مالاریا که ناشی از پلاسمودیوم است و همچنین عامل بیماری سل می باشد.
علاوه بر این، دانش ضعیف از پاسخ های ایمنی محافظتی و فعل انفعالات درگیر در ماندگاری در برابر آنتی ژن های واکسن، از جمله دیگر محدویت های واکسن های سنتی می باشند. علاوه بر این، عوامل مختلفی مانند جهانی شدن، مهاجرت های گسترده و رشد سریع جمعیت منجر به ظهور و ظهور مجدد عوامل عفونی قدیمی و جدید در حیوانات و انسان می شود.
در نتیجه، توسعه ی تولید واکسن های نوین به عنوان یک ضرورت فوری محسوب می شود. در دهه ی گذشته، ایمونوانفورماتیک مترقی ترین حوزه در زمینه ی پیشگیری، کنترل، تشخیص و درمان بیماری ها در علوم پزشکی و دامپزشکی بوده است.

ایمونوانفورماتیک، طبقه بندی داده های بیولوژیکی، تجزیه و تحلیل کمی و کیفی همراه با بهبود طراحی دارو و واکسن بر اساس اطلاعات بیولوژیکی از مولکول های ماکرو و میکرو مانند DNA، RNA و پروتئین می باشد.
علاوه بر نکات فوق الذکر، بیوانفورماتیک بیشتر در مورد رویکردهای محاسباتی، به ویژه ایمونوانفورماتیک، واکسن شناسی محاسباتی و شیمی انفورماتیک می باشد. زیست شناسی محاسباتی ما را قادر به پیش بینی امکان بهبود خواص مختلف از محصولات بیولوژیکی موجود، توسعه نسل های جدید واکسن، کشف داروهای جدید، کیت های تشخیصی، آنتی بادی ها و ادجوانت ها و همچنین ارزیابی آلرژن ها و ترکیبات سمی با کمترین هزینه و بیشترین راندمان می نماید.
بررسی سرطان و بیماری های خودایمنی، مدل سازی فعل و انفعالات و مکانیسم های عملکرد بدن در حالات سلامتی و بیماری و همچنین آبشارهای سلولی پیچیده از جمله کاربردهای ایمونوانفورماتیک می باشد. برای محققین تمامی رشته های علمی به ویژه دامپزشکی و علوم پزشکی آشنایی با کاربردهای ایمونوانفورماتیک و استفاده از ابزارهای ایمونوانفورماتیکی به بهترین شکل ممکن، حائز اهمیت می باشد.
اهداف بسیاری از موسسات تحقیقاتی تولید واکسن ها، کیت ها، آنتی بادی ها، ادجوانت ها، محصولات سرولوژیکی و بیولوژیک و همچنین تشخیص ارگانیسم های عفونی حیوانات و انسان می باشد.
همچنین بایستی اشاره نمود که هزینه های علم ایمونوانفورماتیک، زمان مورد نیاز، عوارض جانبی و مشکلات عملی، مانند کشت ارگانیسم های بسیار خطرناک یا کم رشد، کمتر می باشد. در این زمینه بیشترین شاخه های مرتبط علم ایمونوانفورماتیک که موضوعات مرتبط با تحقیقات واکسن را پوشش می دهند عبارتند از ایمونوانفورماتیک، کموانفورماتیک و بیوانفورماتیک عمومی. (به عنوان مثال کار با توالی، پایگاه های داده یا طراحی پرایمر و پروب).
به تازگی، دانشمندان علاقه زیادی به تولید داروهای طراحی شده، تولید نسل های جدید واکسن ها، کیت ها و محصولات بیولوژیکی و روش های نوین درمانی دارند. برای رسیدن به این اهداف ایمونوانفورماتیک و کموانفورماتیک به عنوان دو شاخه اصلی بیوانفورماتیک استفاده می شود. سایر رشته های بیوانفورماتیک ممکن است زیرشاخه های این دو شاخه اصلی باشند.
برخی از زیرشاخه های ایمونوانفورماتیک و کموانفورماتیک شامل بیوانفورماتیک ساختاری، آنالیز داده های NGS، آنالیز داده های RNA-seq، آنالیز داده های microarray، آنالیزهای فیلوژنتیک و ژنتیک جمعیت، سیستم بیولوژی یا زیست شناسی سامانه ای و طراحی پیشرفته و مهندسی پروتئین، پپتید و اسیدنوکلئیک، می باشد.
در این مطلب سعی داریم با جزئیات بر روی کاربردهای ایمونوانفورماتیک که شامل تشخیص و درمان سرطان، همراه با ایده ادغام زیست شناسی سامانه ای یا سیستم بیولوژی با ایمونوانفورماتیک است، تمرکز نماییم.
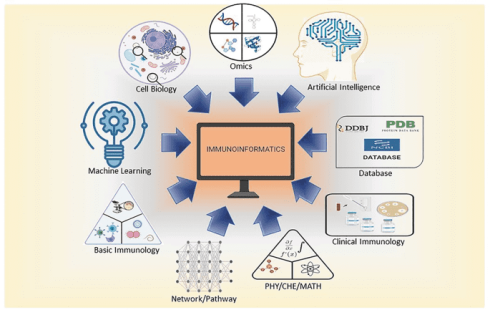
ایمونوانفورماتیک برای تشخیص و درمان سرطان
ارائه آنتی ژن نقش اساسی در پاسخ ایمنی و در نتیجه در روش های ایمنی درمانی مانند واکسیناسیون ضد تومور ایفا میکند. نیاز به غربالگری سریع آنتی ژن ها و طراحی انواع خاصی از ساختارهای بیانی برای ایمونوتراپی سرطان وجود دارد. پاسخهای ایمنی مناسب به سرطان احتمالا محدود به ایمنی یک سرطان خاص، از جمله مجموعه آنتیژنهایی است که پاسخهای ایمنی موفق را هدایت میکنند.
با این حال، یافتن مجموعه ای از آنتی ژن هایی که بین تومورهای مختلف متفاوت است، هنوز دشوار است. واکسیناسیون ضد تومور از فرآیندهای in vivo بهره میبرد و بر خلاف گسترش مصنوعی سلولهای T، از قدرت کامل سیستم ایمنی استفاده میکند. تغییرات در تشخیص و پیشگیری سرطان توسط ایمونوانفورماتیک پشتیبانی می شود.
به عنوان مثال، شبکه انفورماتیک زیست پزشکی سرطان (caBIG) شبکه ای از ۵۰۰ فرد و ۵۰ موسسه را به هم متصل می کند که داده ها و تجزیه و تحلیل ابزارها را برای سرعت بخشیدن به توسعه رویکردهای نوآورانه برای پیشگیری و درمان سرطان به اشتراک می گذارند. شماره پایگاه داده سال 2005 پژوهشگاه اسیدهای نوکلئیک ۱۴پایگاه داده مولکولی مرتبط با سرطان را فهرست می کند که ۹ ابزار، پایگاه داده ی ایمونوانفورماتیک عمدتا بر ژن های مرتبط با سرطان و بیان ژن تمرکز دارند.
فهرستی از آنتی ژن های تومور نیز موجود است. این لیست شامل آنتی ژن هایی است که اپی توپ های سلول T را تعریف کرده اند. آنتی ژن های مرتبط با تومور (TAA) نقش حیاتی در تشخیص و درمان سرطان های انسانی، مانند آنتی ژن اختصاصی پروستات (PSA) در تشخیص سرطان پروستات ایفا کرده اند. با وجود این، فرآیند شناسایی TAA اغلب توسط روشهای پیچیده آزمایشگاهی مختل شده است.
برای تسریع روند کشف آنتی ژن تومور، و بهبود تشخیص و درمان سرطان انسانی، یک پایگاه داده عمومی در دسترس آنتی ژن مرتبط با تومور انسانی (HPtaa) (http://www.hptaa.org) ایجاد شده است. زیست شناسی سامانه ها یا سیستم بیولوژی شناسایی تعداد کمی از آنتی ژن های بیان شده توسط سلول های سرطانی که اهداف مناسبی برای پاسخ های ایمنی در برابر سرطان هستند، را مورد هدف قرار داده است.
واکسن ضد تومور
پیشبینیهای قابل اعتماد پپتیدهای اپی توپ سلول T ایمنیزا برای طراحی منطقی واکسن بسیار مهم هستند و یک مشکل کلیدی در ایمونوانفورماتیک را نشان میدهند. رویکردهای محاسباتی برای تسهیل فرآیند تشخیص اپی توپ و نشان دادن کاربردهای بالقوه برای درمان ایمونوتراپی سرطان ایجاد شده است.
طراحی واکسن مبتنی بر اپی توپ، از این الگوریتم های ایمونوانفورماتیک برای شناسایی اهداف بالقوه واکسن ها علیه سرطان استفاده می کند. توسعه واکسن های DNA مبتنی بر اپی توپ و اثرات ضد توموری آنها در تحقیقات پیش بالینی علیه لنفوم سلول B توصیف شده است. بیشتر رویکردهای ایمونوتراپی بر روی القای سلولهای CD8+ T ضد توموری کار میکنند که فعالیت سیتولیتیک را به سمت سلولهای توموری بیانکننده Ags خاص تومور یا مرتبط با تومور نشان میدهند.
اما استراتژیهای ایمنسازی که صرفا بر ایمنی سلولهای T CD8+ تمرکز میکنند ممکن است ناکافی باشند زیرا قادر به ایجاد ایمنی محافظتی طولانیمدت نخواهند بود. نشان داده شده است که پپتیدهای پیش بینی شده برای اتصال به MHC می توانند پاسخ لنفوسیت های T سیتوتوکسیک (CTL) کشنده تومور را ایجاد کنند.
مشخص شده است که CTLها نقش کلیدی در تولید اثرات درمانی ضد تومور دارند. سلول های CD4+ T برای تولید و حفظ پاسخ CTL ها از طریق ارائه سیتوکین ها یا از طریق مسیر اصلی،حیاتی هستند. اپی توپ های کلاس II متصل به MHC سلول های CD4+ T را فعال می کنند و پاسخ موثر CTL را حفظ می کنند که نقش مهمی در پاسخ ضد توموری ایفا می کنند. سلول های CD4+ T وضعیت عملکردی هر دو پاسخ ایمنی ذاتی و اکتسابی را تعیین می کنند. بنابراین، گنجاندن اپی توپ های مناسب سلول CD4 + T ممکن است برای اثربخشی واکسن ضروری باشد.
ایمونوگلوبولین (IgM) که توسط لنفوم سلول B بیان می شود یک مارکر کلونال و یک آنتی ژن اختصاصی تومور است. بنابراین، می توان از آن به عنوان یک هدف ایمنی استفاده کرد. اپی توپ های ایمونوژنیک خاص شناسایی شده از این آنتی ژن های تومور را می توان به عنوان واکسن برای فعال کردن پاسخ ایمنی در برابر سلول های تومور استفاده کرد.
ایمونوانفورماتیک و سیستم بیولوژی برای پزشکی شخصی
ایده ادغام ایمونوانفورماتیک با رویکردهای زیستشناسی سامانه ای یا سیستم بیولوژی برای درک بهتر بیماریهای مرتبط با ایمنی در سطوح مختلف سیستم است. این ادغام می تواند مسیر چندین مطالعه ترجمه ای را برای اقدامات بالینی بهتر باز کند. ارتباط بین یک بیماری و تغییرات ژنتیکی یکی از مهمترین جنبه ها در فارماکوژنومیک و توسعه پزشکی شخصی است.
اطلاعات در مورد فراوانی آللی مولکول های ایمنی در جمعیت انسانی مهم است زیرا زیرگروه های مختلف بیماران را می توان با واکسن ها یا پاسخ های دارویی مختلف شناسایی کرد. به عنوان مثال، یک SNP (S427T) در ژن ایمنی ذاتی اینترفرون فاکتور تنظیم کننده 3 (IRF3) با افزایش خطر تداوم ویروس پاپیلومای انسانی (HPV) و سرطان دهانه رحم مرتبط است. پایگاه های داده تغییرات ژنومی مانند HapMap (http://snp.cshl.org/) و http://www.ncbi.nlm.nih.gov/ SNP/) dbSNP ) اطلاعاتی را در مورد داده های ژنوتیپ فردی ارائه می دهند.
پایگاه داده فرکانس آللی را می توان برای جستجوی مناطق چند شکلی از جمعیت های مختلف در زمینه سازگاری بافتی و ایمونوژنتیک (http://www.allelefrequencies.net/) استفاده کرد که شامل اطلاعات پلی مورفیسم در HLA، سیتوکین ها و گیرنده های شبه ایمونوگلوبولین سلول کشنده (KIR) است. بنابراین، گسترهای از توسعه واکسنها و داروهای بهینهسازی شده برای پیشگیری و درمان شخصی از طریق ادغام زیستشناسی سامانه ای (سیستم بیولوژی) و ایمونوانفورماتیک وجود دارد.