مقدمهای بر مدلسازی فیبروز ریوی و آسیب حاد ریوی در جوندگان
ریهها اندامهای بسیار عروقی و ظریفی هستند که وظیفه تبادل گاز و اکسیژنرسانی سیستمیک را بر عهده دارند.
بافت ریه در صورت آسیبدیدگی – چه در اثر عفونت، سموم، واکنشهای خودایمنی یا آسیب مکانیکی – میتواند یک پاسخ التهابی نامنظم ایجاد کند که منجر به آسیب حاد ریه (ALI) یا فیبروز ریوی پیشرونده (PF) میشود.
این دو بیماری دو انتهای مخالف یک طیف را نشان میدهند: ALI معمولاً ناگهانی و التهابی است، در حالی که PF آهسته و فیبروتیک و اغلب برگشتناپذیر است.
ALI با تخریب سد آلوئولی-مویرگی، نفوذ نوتروفیل، ادم غنی از پروتئین و کاهش انطباق ریه مشخص میشود.
اگر آسیب پایدار بماند یا به طور نامناسب برطرف شود، ممکن است به بازسازی فیبروتیک تبدیل شود ، که مشخصه فیبروز ریوی ایدیوپاتیک (IPF) و عوارض پس از ARDS است.برای درک مبانی مولکولی و سلولی این بیماریها و آزمایش مداخلات ضد فیبروتیک یا ضد التهابی، مدلهای جوندگان به ابزارهای ضروری تبدیل شدهاند.
در آزمایشگاه دانش بنیان ژنیران، مدلهای ALI و PF را در موشهای سوری و موشهای صحرایی، به همراه تست های کامل بافتشناسی و و مولکولی به متقاضی ارائه میدهیم.
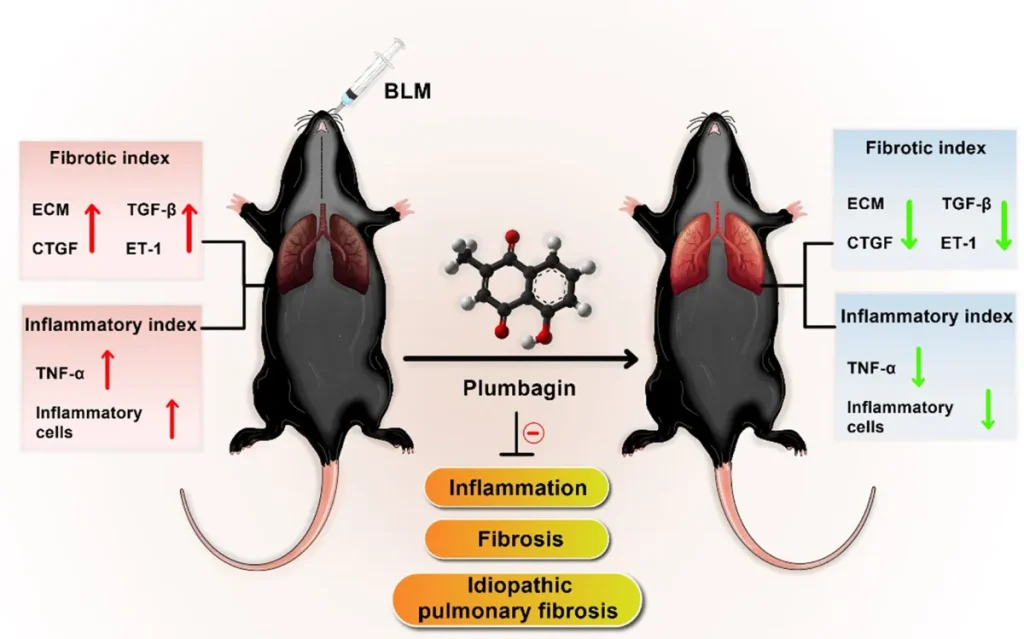
فیبروز ریوی ناشی از بلئومایسین
بلئومایسین، یک آنتیبیوتیک ضد تومور، پرکاربردترین عامل برای القای فیبروز ریوی در جوندگان است.
این بیماری باعث شکستگی رشتههای DNA، آسیب اکسیداتیو و آسیب اپیتلیال میشود و در نهایت یک پاسخ فیبروتیک مشابه آنچه در فیبروز ریوی ایدیوپاتیک انسانی (IPF) دیده میشود، ایجاد میکند.
مکانیسم اثر: بلئومایسین وقتی به صورت داخل نای یا داخل بینی تجویز شود، باعث آسیب حاد به اپیتلیوم آلوئولار میشود.
این امر منجر به موجی از نفوذ سلولهای التهابی ) عمدتاً نوتروفیلها و ماکروفاژها ( و به دنبال آن فعال شدن فیبروبلاستها و رسوب بیش از حد ماتریکس خارج سلولی (ECM)، از جمله کلاژن نوع I و III میشود.
طی ۲ تا ۴ هفته، این امر به فیبروز بینابینی، ضخیم شدن آلوئولها و از دست رفتن انطباق ریه تبدیل میشود.
عملکرد بلئومایسین بسیار موضعی و حساس به زمان است. در ابتدا، یک فاز التهابی (روزهای ۱ تا ۷) غالب است و به دنبال آن یک فاز فیبروتیک (روزهای ۷ تا ۲۸) وجود دارد که بسته به هدف تحقیق میتواند تعدیل یا از نظر درمانی هدفمند شود.
مزایاو محدودیت ها:
مزایا:
- ضایعات فیبروتیک قابل تکرار.
- ویژگیهای کلیدی IPF را تقلید میکند.
- امکان ارزیابی درمانهای ضد فیبروتیک و ضد التهابی را فراهم میکند.
محدودیتها
- فیبروز ایجاد شده در جوندگان بعد از مدتی به طور طبیعی ممکن است بهبود یابد ، در صورتی که این بیماری در انسان اصولا پیشرونده و مزمن است.
- تغییرپذیری وابسته به گونه و دوز، برخی نژاد ها ممکن است نسبت به فیبروز مقاوم باشند.
آسیب حاد ریوی ناشی از LPS
لیپوپلیساکارید (LPS)، یکی از اجزای دیواره سلولی باکتریهای گرم منفی، معمولاً برای شبیه سازی آسیب ریوی ناشی از عفونت حاد ریه (ALI) یا سپسیس استفاده میشود.
این بیماری از طریق گیرنده Toll-like 4 (TLR4) یک پاسخ ایمنی ذاتی قوی را تحریک میکند که منجر به طوفانهای سیتوکین، هجوم نوتروفیلها و اختلال در عملکرد سد دفاعی میشود.
مکانیسم: جوندگان پس از تجویز داخل نای یا سیستمیک (داخل صفاقی یا داخل وریدی) LPS، دچار التهاب گسترده ریوی میشوند.
نوتروفیلها به فضاهای آلوئولی مهاجرت میکنند و گونههای فعال اکسیژن (ROS)، پروتئازها و سیتوکینهایی مانند TNF-α، IL-1β و IL-6 تولید میکنند. سد آلوئولی-مویرگی نفوذپذیر میشود و منجر به ادم ریوی، نشت پروتئین و اختلال در تبادل گاز میشود که از نشانههای ALI/ARDS هستند.
این مدل برای مطالعه التهاب حاد، تنظیم سیتوکین، سازو کار نوتروفیل و درمانهای ضد التهابی بسیار مناسب است.
مزایاو محدودیت ها
مزایا:
- شروع اثر سریع و تکرارپذیری بالا
- شبیهسازی فاز حاد ARDS باکتریایی
- قابل تنظیم از طریق دوز و روش مصرف
محدودیتها:
- بدون فیبروز یا تغییر شکل مزمن مگر در صورت مواجهه طولانی مدت
- ایمونولوژیک اما بدون آسیب مکانیکی
- حساس به نژاد و سن حیوان
ALI ناشی از آسپیراسیون اسید
این مدل برای شبیهسازی پنومونیت آسپیراسیون، یکی از علل اصلی ARDS در محیطهای بالینی مانند عوارض بیهوشی، رفلاکس معده یا سکته مغزی، طراحی شده است.
تزریق اسید هیدروکلریک (HCl) به داخل نای باعث آسیب شیمیایی به اپیتلیوم آلوئولار میشود و منجر به یک آسیب حاد ریوی التهابی غیرعفونی میشود.
مکانیسم:
اسید باعث نکروز مستقیم اپیتلیال، تخریب دیوارههای آلوئولی و تراوش پروتئین به داخل فضاهای هوایی میشود.
این امر منجر به خونریزی، غیرفعال شدن سورفکتانت، نفوذ نوتروفیلها و هیپوکسمی میشود. آسیب ظرف ۲۴ ساعت به اوج خود میرسد و بسته به پاسخ ایمنی حیوان ممکن است برطرف شود یا ادامه یابد.
این مدل برای بررسی بازسازی اپیتلیال، شکست حاد سد دفاعی و درمانهای هدفمند با سورفکتانت مفید است.
مزایا و محدودیت ها
مزایا:
- این مدل ها همانند حالتی هستند که در انسان در اثر آسپیراسیون (ورود محتوایات معده یا مایعات به ریه)، بیماری به وجود می آید.
- ساده و مقرون به صرفه
- مناسب برای مطالعه در زمان های مختلف از زمان القا بیماری
محدودیتها:
بدون فیبروز مزمن
نیاز به کنترل دقیق حجم اسید و pH
در صورت دوز نامناسب میتواند باعث مرگ و میر شود.
مدلهای اسید اولئیک و تهویه مکانیکی
تجویز اسید اولئیک (OA) یا تهویه مکانیکی با حجم جاری بالا به ترتیب برای مدلسازی ALI مرتبط با آمبولی چربی یا آسیب ریوی ناشی از ونتیلاتور (VILI) استفاده میشوند. این مدلها به مطالعه آسیبهای ریوی اکتسابی از بیمارستان و نقش استرس بیوفیزیکی کمک میکنند.
مکانیسم:
اسید اولئیک باعث آسیب اندوتلیال میشود و منجر به نشت مویرگی، خونریزی و ادم ریوی میگردد. اتساع بیش از حد مکانیکی آلوئولها در طول تهویه نامناسب به طور مشابه یکپارچگی سد را مختل کرده و باعث التهاب و ادم میشود. هر دو مدل باعث فعال شدن نوتروفیلها، آزادسازی سیتوکین و فروپاشی آلوئولها میشوند.
این موارد برای بررسی استراتژیهای تهویه حفاظتی، تثبیتکنندههای سد دفاعی و درمانهای هدفمند عروقی مرتبط هستند.
مزایا و محدودیت ها
مزایا:
- شبیهسازی آسیبهای ریوی مرتبط با بخش مراقبتهای ویژه(ICU)
- منعکسکننده مسیرهای استرس مکانیکی و اندوتلیال
- مفید برای آزمایش پروتکلهای تهویه و درمانهای نجات
محدودیتها
- نیاز به تجهیزات تخصصی (ونتیلاتور)
- بازه زمانی کوتاه و تنوع بالای بین فردی
- کمتر برای فیبروز استفاده میشود.
همچنین بخوانید:
- خدمات القا انواع بیماری و ایجاد حیوان مدل
- دوره کارآموزی کار با حیوانات آزمایشگاهی
- خرید انواع رت و موش آزمایشگاهی