اطلاعات عمومی,ویکی ژن
مبانی سیستم بیولوژی، اومیکس و مدلسازی در زیستشناسی
درباره مبانی سیستم بیولوژی
چه شد که علم در زیستشناسی به فکر مدلسازی و ایجاد حوزهای به نام سیستم بیولوژی افتاد؟
در اصل مدلسازی در علوم مهندسی کاربرد بسیاری دارد و به این حوزه قدرت بالایی در تحلیل رفتار سیستمهای ماشینی داده است. همینطور در علوم دیگری مانند فیزیک، دانشمندان سعی کردهاند که پدیدهها را در قالب روابط ریاضی بیان کنند تا بتوانند آبوهوا، حرکت اجرام آسمانی، تغییرات زمین و مواردی از این دست را مطالعه کنند. سیستم یا سامانه بخشی از محیط است که برای مطالعه آن را از یک سیستم کلیتر جدا میکنیم یا به اصطلاح برای آن مرز تعیین میکنیم. برای درک یک سیستم به دنبال این هستیم که اجزا رو بشناسیم و ارتباط بین آنها را پیدا کنیم. سیستمها انواع مختلفی دارند:
- سامانه ساده مثل حرکت یک آونگ ساده است که معادلات ساده فیزیکی برای تحلیل رفتار آونگ نوشته میشود. باید در نظر داشته باشیم که این سامانه خیلی ساده شده و از واقعیت فاصله زیادی دارد.
- سامانه دشوار یا بغرنج از قبلی به سمت پیچیدگی حرکت کرده است. زمانی که دوتا آونگ در فضا داشته باشیم باز هم میتوانیم با معادلات رفتار سیستم را توضیح دهیم، ولی معادلات به سادگی مرحله قبل نیستند.
- سامانه آشوبناک، سامانهای است که خطا در محاسبات به صورت نمایی بالا میرود. به شدت به شرایط سیستم در حالت اولیه محاسبات وابسته است. معادلات پیچیده بوده و با اینکه میتواند سرشت سیستم را توضیح دهد، اما نمیتواند دقیقا مسیر را پیشبینی کند. به همین دلیل است که پیشبینیهای هواشناسی تا یک زمانی قابل اتکا هستند.
- سامانه پیچیده تعداد زیادی از اجزا دارند که با یکدیگر برهمکنش دارند و یک کل جدید را ایجاد میکنند. این سامانهها دارای هوش جمعی هستند و کل جدیدی را با تکیه بر مفاهیم پدیدارگی میسازند. اینجاست که با شناخت اجزای سیستم به درک درستی از آن نمیرسیم و باید به کل نگاه کنیم.
در حدود 70 سال پیش، زیستشناسان مولکولی بر این باور بودند که اگر ما عملکرد مولکولهایی را که سلولها را تشکیل میدهند، بدانیم و درک کنیم، میتوانیم بفهمیم سلولها چطور کار میکنند یا اصلاً همین عملکردها چه فرایندی را طی میکنند و چه تأثیری بر سلول میگذارند.
بااینحال، این تصور تنها بهصورت تئوریک صادق بود، البته در عمل نیز در موارد معدودی صادق است. این موضوع به این دلیل است که تعداد زیاد مولکولهای حاضر در سلول، درک بسیاری از عملکردها را به طور همزمان بسیار دشوار میکند.
با پیشرفت فناوری در سالهای بعدی، یعنی 20 تا 25 سال قبل، امکان اندازهگیری همزمان بیشتر این مولکولها ممکن شد.
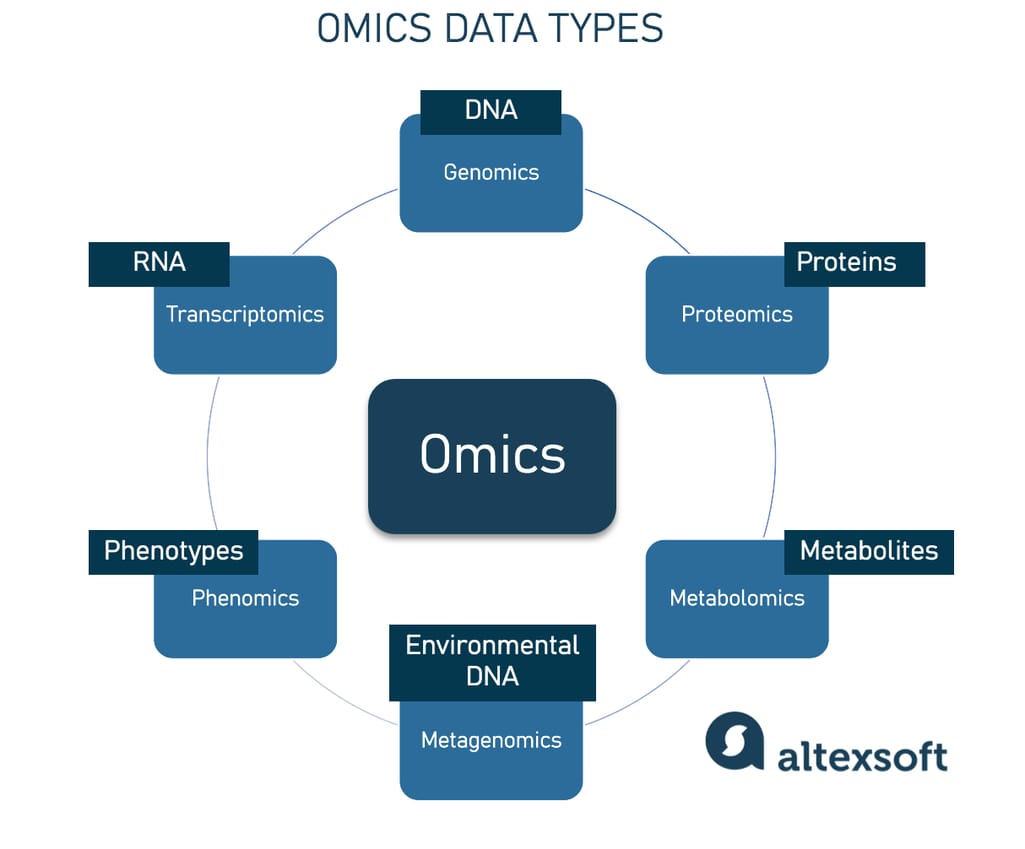
این دستگاهها، دستگاههای توالییابی با توان بالا بودند که میتوانستند در مدتزمان کوتاهتری حجم بیشتری از دادهها را توالییابی کنند. تولید دادهها به کمک تکنولوژیهای High throughput یا توان بالا، در حوزه اومیکس (Omics) قرار میگیرد. این دادهها در مراحل بعدی توسط تحلیلها و مدلسازی مبتنی بر سیستم بیولوژی مورد بررسی قرار میگیرند.
در نتیجه این افزایش قدرت در تولید داده، ما شاهد تجمع دادههای زیستی هستیم. این دادهها مجموعههایی هستند که شامل اطلاعات سلولها و ارگانیسمهای مختلف در شرایط خاص است. واکنشهای شیمیایی بین بسیاری از این اجزا در حال حاضر شناخته شده و این دانش باعث ایجاد شبکههای واکنش بیوشیمیایی بازسازی شده (reconstructed biochemical reaction networks) در مقیاس ژنومی میشود که زیربنای عملکردهای مختلف سلولی است. پس، در این زمان است که آشنایی با سیستم بیولوژی رخ میدهد و زیستشناسی سیستمهای مولکولی وارد کار میشود.
زیستشناسی سیستمها لزوماً بر خود اجزاء متمرکز نیست، بلکه بر ماهیت پیوندهایی که آنها را به هم متصل میکند و بر روی حالتهای عملکردی شبکههای بیوشیمیایی که از مجموعه همه این پیوندها حاصل میشوند، متمرکز است.
این حالتهای (states) عملکردی که در شبکهها وجود دارد، با حالتهای فیزیولوژیکی (physiological) یا هموستاتیک (homeostatic) قابلمشاهده در سلول مطابقت دارد. پس، تکمیل رابطه بین تمام اجزای شیمیایی یک سلول به همراه پایههای ژنتیکی مربوط به آنها، در کنار عملکردهای فیزیولوژیکی سلولها قرار گرفته تا نویدبخش ظهور زیستشناسی سامانهها بوده و کاربردهای سیستم بیولوژی را گستردهتر کند.
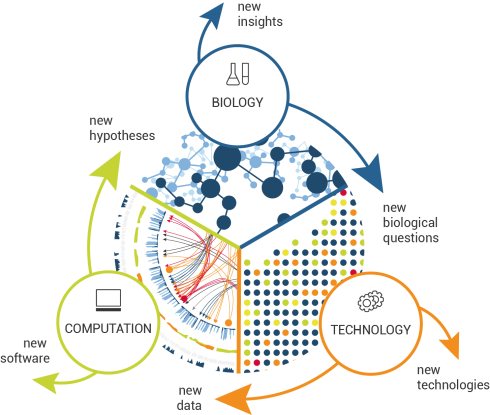
مبانی سیستم بیولوژی
در قدم اول برای آشنایی با سیستم بیولوژی باید ارتباط بین ژنوتیپ و فنوتیپ را بشناسیم. گرگور مندل از طریق آزمایشهای خود کشف کرد که اطلاعات بستهبندی شده در ماده ژنتیک، از نسلی به نسل دیگر منتقل میشود تا شکل و عملکرد موجودات در نسل بعدی را تعیین کند. این بستههای اطلاعاتی امروزه ژن نامیده میشوند و مجموعهای از تمام ژنها و نسخه خاصی از آنها که در ژنوم یک ارگانیسم وجود دارد، ژنوتیپ آن نامیده میشود.
در قدم بعدی، شکل و عملکرد یک موجود زنده بهعنوان فنوتیپ آن شناخته میشود که چگونگی ارتباط فنوتیپ با ژنوتیپ یک رابطه مهم در دانش زیستشناسی است. برای صفات تک ژنی، رابطه ژنوتیپ – فنوتیپ بهراحتی قابلدرک است؛ یک ژن یک فنوتیپ میدهد.
بااینحال، بیشتر صفات فنوتیپی شامل عملکردهای هماهنگ محصولات ژنی متعدد است که درک رابطه ژنوتیپ و فنوتیپ را برای ما دشوار میکند. چراکه در وهله اول باید همه ژنها و محصولات ژنی را بشناسیم و در وهله دوم، درکی از پیامدهای تعاملات پیچیده آنها داشته باشیم. مورد اول با استفاده از دادههای اومیکس و دومی با استفاده از تحلیل سیستمهای بیوشیمیایی بررسی میشود که از کاربردهای سیستم بیولوژی است.
پرداختن به این موارد در طی سالهای گذشته سبب شده رویکرد از پایینبهبالا (bottom-up approach) در زیستشناسی سامانهها ایجاد شود. با انتشار اولین توالی ژنوم کامل در اواسط دهه 1990، در اصل، شناسایی تمام محصولات ژنی که یک ارگانیسم را تشکیل میدهند ممکن شد. همچنین، بازسازی شبکههای متابولیکی در مقیاس ژنومی را برای ارگانیسم هدف به روشی دقیق از نظر بیوشیمیایی ممکن نمود. چنین بازسازیهای شبکه متابولیکی را میتوان به یک قالب ریاضی تبدیل کرد که روابط ژنوتیپ – فنوتیپ را قابل بررسی میکند.
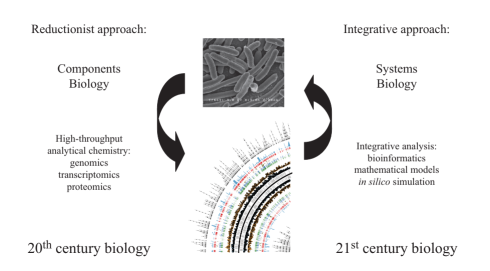
ریاضیات و مدلهای محاسباتی وابسته به آن، درک دانشپایه بیوشیمیایی، ژنتیکی و ژنومی در سلول را برای ما ممکن میکند. این اطلاعات درک رابطه بین اجزا را برای ما ممکنتر میکند تا بتوانیم دید درستی از آنچه درون یک سیستم رخ میدهد داشته باشیم. پس میتوان شاخههای سیستم بیولوژی را در علوم مختلفی پیدا کرد، چراکه همگی این علوم، اعم از ریاضیات، فیزیک و شیمی، در این حوزه بینرشتهای کنار هم قرار داده شدهاند تا بتوانیم به سؤالات زیستی پیچیده پاسخ دهیم.
سیستم بیولوژی، در اصل به دنبال مدلسازی رفتار یک سیستم زیستی است و برای اینکار از روشهای مختلفی مانند تحلیل گراف در مطالعات شبکههای زیستی، آنالیز شار برای ساخت میکروارگانیسمهای صنعتی، معادلات دیفرانسیل PDE و ODE برای بررسی رفتار دینامیکی ملکولها یا سلولها و حتی مدلسازی تصادفی و غیره استفاده میکند.
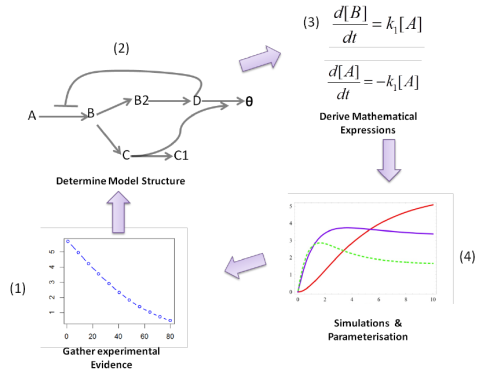
اولین توالی ژنوم کامل در اواسط دهه 1990 به دست آمد و تقریباً در همان زمان، توالیهای پروفایل بیان mRNA و فناوریهای پروتئومی نیز به ما این توانایی را دادند که تعیین کنیم یک سلول چه زمانی از چه ژنهای خاصی استفاده میکند. این فناوریها به ما اجازه میدهند تا به یک نمای در مقیاس ژنومی دستیابیم. در آغاز قرن بیست و یکم، این فرایند با سرعتی سریع در حال گسترش بود و باعث تغییر پارادایم اساسی در زیستشناسی شد.
ظهور فناوریهای توالییابی با توان بالا، زیستشناسان را مجبور کرد که سلولها را بهعنوان سیستمها ببینند، نه اینکه توجه خود را بر اجزای سلولی منفرد متمرکز کنند. نهتنها این فناوریها دیدگاه سیستمی را تحمیل کردند، بلکه مطالعه سلولها بهعنوان سیستم نیز امکانپذیر شد.
حالا با لیستی که از اجزای سلولی و خواص آنها داریم چه باید کنیم؟ این لیستها، به همان اندازه که حاوی اطلاعات هستند، اما فقط اطلاعات پایهای در مورد مولکولهایی سازنده سلولها، خصوصیات شیمیایی آنها و زمانی که مورداستفاده قرار میگیرند را ارائه میکند. حالا برای تحلیل یکپارچهای آنها باید بر بیوانفورماتیک و روشهای تحلیل سیستمها تکیه کنیم؛ بنابراین، در آغاز قرن، زیستشناسی مولکولی بر ویژگیهای سیستمی عملکردهای سلولی و بافتی متمرکز شد. در نظر داشته باشید که اینها خواصی هستند که از کل ناشی میشوند و نمایانگر خصوصیات بیولوژیکی هستند. به نوبه خود، علم در مقیاس ژنوم ظهور و شروع به رشد کرد.
سیستم بیولوژی به دلیل آنکه یک حوزه میانرشتهای محسوب میشود، از علوم مختلف میتوان به آن وارد شد؛ چیزی که باعث ایجاد نگرشهای مختلف در آن شده است که هرکدام کاربردهای سیستم بیولوژی را گسترش دادهاند. نمیتوان علوم مختلف را در این حوزه از هم جدا کرد، چراکه همگی آنها در تعامل با یکدیگر به دنبال حل سؤالات زیستی هستند. از طراحی مدلها و روشهای محاسباتی گرفته تا تحلیل سیستمهای زیستی همگی در حوزه سیستم بیولوژی بوده و کاربردهای مشترکی را دنبال میکنند.
سیستم بیولوژی میتواند در بررسی رشد و نمو جمعیتهای میکروبی و سلولی، تأثیراتی که بر رویهم میگذارند و مواردی ازایندست کاربرد داشته باشد. با داشتن اطلاعاتی درمورد سیستمهای زیستی پیچیده، میتوانیم به دستورزی سلولها به کمک روشهای مهندسی متابولیک و سینتتیک بیولوژی نیز رو بیاوریم که کاربردهایی در حوزه مهندسی شیمی و بیوتکنولوژی دارد.
در زیر به تعدادی از کاربردهای سیستم بیولوژی در زیستپزشکی اشاره شده است:
-
تعیین ماژولهای بیماری
ماژولها در شبکههای بیولوژیکی زیرشبکههایی هستند که در داخل شبکه کلی به هم پیوستهاند و بر روی عملکرد یکدیگر اثر میگذارند. ماژولهای عملکردی زیرشبکههایی هستند که پیوندهای آنها پیامدهای عملکردی را منعکس میکنند و اغلب شامل یک مسیر قابلتعریف هستند.
در حقیقت ماژولها به ما کمک میکنند که شبکه عظیم بیماری را به اجزای کوچکتر تقسیم کنیم و روی بخشی که تاثیر بیشتری بر روی بیماری داشته است تمرکز کنیم. نباید اشتباه کنیم که این تقلیلگرایی با سیستم بیولوژی منافات دارد. به کمک دیدگاه سیستمیک ما تمام تلاش خود را برای جلوگیری از سوگیری انجام میدهیم و سعی میکنیم دیتای زیادی را به دست آوریم. سپس وقتی شبکهای از بیماریها ساختیم، آن را تحلیل میکنیم. این تحلیل بخشهایی از سیستم را به ما نشان میدهد که تاثیر بیشتری بر روی بیماری داشته است. اینجاست که بر روی آن بخش مورد نظر متمرکز میشویم و تحلیل خود را ادامه میدهیم.
درحالیکه اگر از سیستم بیولوژی استفاده نمیکردیم، ممکن بود بخش مهمتری از سیستم را که تاثیر بیشتری بر روی بیماری داشته نبینیم و با بررسی اجزایی بااهمیت کمتر به تحقیقات خود ادامه داده باشیم.
-
ساختن شبکه بیماریها
همینطور که در بخش قبل نیز توضیح داده شد، به کمک سیستم بیولوژی، میتوانیم شبکه یک بیماری را تحلیل کنیم. همچنین میتوانیم یک شبکه جامع از چندین بیماری داشته باشیم. در حقیقت این شبکه به ما کمک میکند که ارتباط بیماریها با یکدیگر را متوجه شویم. یعنی ممکن است چندین بیماری بر روی یک ملکول یا مسیر خاص تاثیر بگذارند. همین امر مکانیسم بیماریها را برای ما آشکارتر کرده و تاثیرات هرکدام را بر دیگری روشن میکند.
-
شناسایی ژنهای جدید درگیر در بیماریها
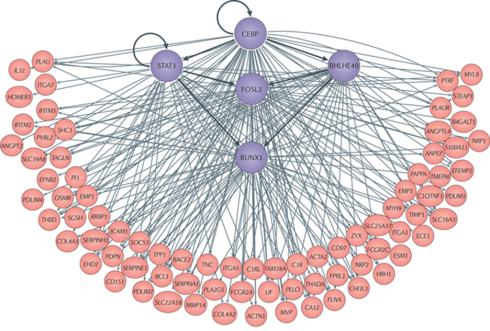
یکی از مهمترین تحلیلهایی که بر روی شبکه بیماری انجام میگیرد، شناسایی ژنهای جدید درگیر در بیماری است. گاهی اوقات در مطالعات، بدون اینکه به تحلیل شبکه بپردازیم، تغییرات چند ژن را بررسی میکنیم و از این طریق چند ژنی که بیانشان تغییر کرده است را به عنوان ژنهای درگیر در بیماری معرفی میکنیم. با این حال، میتوانیم قدم مهم دیگری را برداریم و این ژنها را در یک شبکه رسم کنیم.
شبکه به ما میگوید که این ژنها، به خصوص آنهایی که تغییرات قابل توجهی داشتهاند، با ژن اصلی دیگری در ارتباط هستند که آن تغییرات این اجزا را کنترل میکند. اما چون این ژن اصلی، تفاوت بیانی قابل توجهی نداشته از روند تحلیل بیماری حذف شده است. پس اینجا سیستم بیولوژی به کمک ما میآید تا این ژنهایی که چراغ خاموش بر روی بیماری تاثیر میگذارند را پیدا کنیم و در قدم بعدی به دنبال طراحی دارو برای آن باشیم.
-
ارتباط بین بیماریها و drug re-purposing
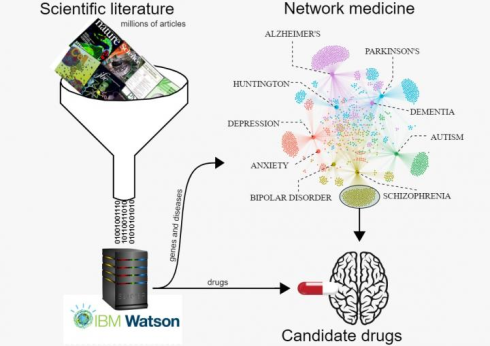
با ساختن شبکهای از بیماریها، ما قدرت این را پیدا میکنیم که تاثیر داروها بر روی بیماری را نیز بررسی کنیم. ساخت دارو یک مسیر دشوار است. سالها زمان و میلیونها دلار هزینه باید صرف شود که یک دارو تایید شود و بعد روانه بازار شود. بااینحال، ما میتوانیم داروهای قدیمی را برای بیماریهای جدید استفاده کنیم. با این کار، دیگر نیازی به بررسی ایمنی دارو نیست و با هزینهای بسیار اندک میتوانید بازار جدیدی برای دارو پیدا کنید.
شبکه بیماریها در سیستم بیولوژی، این امکان را میدهد که ارتباط بیماریها و داروها را رسم کنیم و با روشهای تحلیل گراف داروها را برای بیماریهای دیگری پیشنهاد بدهیم. به این روش، بازکاربرد دارویی (ریپوزیشنینگ دارویی) گفته میشود که در داروسازی کاربرد دارد.
-
شناسایی تارگتهای جدید برای دارو
علاوه بر روش قبلی، یعنی ریپوزیشنینگ دارویی، به کمک شناسایی ژنها یا پروتئینهای دخیل در مسیر بیماری، میتوانیم تارگتهای جدید دارویی برای طراحی دارو پیدا کنیم. با تحلیل شبکه در سیستم بیولوژی، بیوملکولهای مهمی یافت میشوند که بر روی بیماری تاثیرات مهمی میگذارند. پس با کنترل آنها میتوانیم به بهبود بیماران کمک کنیم.

-
بررسی ارتباط بین میزبان و پاتوژن
رسم شبکه، میتواند بین ملکولهای مختلف در میزبانهای مختلف باشد. رسم این شبکه بین میزبان و پاتوژن در سیستم بیولوژی، امکان بررسی مکانیسم اثر پاتوژن بر روی میزبان را میدهد. مثلا با رسم شبکه پروتئینی ارتباط پروتئینهای کرونا و پروتئینهای انسانی، میتوانیم پروتئینهای درگیر را شناسایی کنیم و به کمک این روش، مکانیسم بیماری را شناسایی کرده و به دنبال پیشنهاد دارو برای درمان باشیم.

-
مطالعات میکروبیوم
میکروبیوم از سلولهای مختلفی تشکیل شده است که از آنها میتوان به باکتریها، ویروسها، آغازیها و قارچها اشاره کرد. پس میتوان گفت که همگی در یک سیستم زیستی حضور دارند. تغییرات در جمعیت هرکدام از این اجزا سبب تغییر در فراوانی جزء دیگری در این سیستم میشود. همانطور که میدانیم، تغییر در فراوانی اجزای میکروبیوم ممکن است بر روی ایجاد یک بیماری مانند سرطانهای مختلف یا بیماریهای عصبی تاثیر بگذارد. پس به کمک سیستم بیولوژی، میتوانیم دینامیک تغییرات این سیستم را تحلیل کنیم و با ارائه راهکار درمانی از پیشرفت بیماریها جلوگیری کنیم.
دوره کارآموزی طراحی و مدلسازی سلولی: سیستم بیولوژی
منبع:
Systems Biology Constraint-based Reconstruction and Analysis BERNHARD O. PALSSON
Network Medicine: Complex Systems in Human Disease and Therapeutics Joseph Loscalzo, Albert-László Barabási, Edwin K. Silverman (eds.)
Sitpor.org