مقدمهای بر فلوسایتومتری تصویربرداری برای نظارت بر تعامل ویروس-میزبان
در این مطالعه ، محققان مؤسسه علوم Weizmann در اسرائیل پروتکل فلوسایتومتری تصویربرداری (IFC) را برای ارائه روشی با کارایی بالا، کمی و بسیار قوی برای مطالعه عفونت ویروسی و تعامل ویروس-میزبان ایجاد و بهینه کردند. محققان توانستند به طور همزمان فرآیندهای سلولی متنوعی از جمله تکثیر ویروسی، تبادل و جابجایی، ادغام مراکز تکثیر، تجمعات ویروسی و تغییرات مورفولوژی را نظارت کنند.
به دست آوردن تصویر کامل از عفونت ویروسی چالش برانگیز است
ناهمگونی ویروسها و میزبانهای آنها به این معنی است که بهترین راه برای دستیابی به تصویر کاملی از عفونت ویروسی، مطالعه جمعیتهای زیادی از سلولهای آلوده است. اما اطلاعات مربوط به تنوع در سلولهای آلوده هنگام انجام اندازهگیری وشمارش تودههای سلولی از بین میرود.
از زمان کشف Mimi virus غول پیکر، اکثر آنچه در مورد چرخه عفونت آن وجود دارد با استفاده از روش های میکروسکوپی پیچیده به دست آمده است. اگرچه اینها اطلاعات ساختاری بسیار دقیقی را ارائه میدهند، اما به دلیل میدان دید کوچکشان محدود میشوند، زیرا تنها اجازه میدهند تعداد کمی از سلولها در یک لحظه تصویربرداری شوند.
مینسکی و تیمش میخواستند روشهای موجود را با توسعه روشی با توان عملیاتی بالا تکمیل کنند که پیشرفت عفونت را کمیسازی میکند و پنجرههای زمانی دقیقی را برای مراحل مختلف در چرخه تکثیر فراهم میکند.استفاده از فلوسایتومتری تصویربرداری برای مطالعه عفونت Mimi virus در آمیب
به منظور بررسی رخدادها در سلولهای آلوده، مینسکی و تیمش از فلوسیتومتری تصویربرداری(IFC) برای نظارت بر تغییرات سلولهای آکانتاموبا پلیفاژا(Acanthamoeba polyphaga) (آمیب) که به Mimi virus غولپیکر آلوده شده بودند، استفاده کردند. اگرچه تمرکز تیم بر روی این ویروس بوده است، اما آنها می گویند که پلت فرم IFC میتواند برای مطالعه چرخه عفونت سایر ویروسها نیز مورد استفاده قرار گیرد. برای مطالعه عفونت ویروسی با استفاده از IFC، محققان ابتدا نیاز به توسعه روشهایی داشتند که ویژگی های مورفولوژیکی سلولهای آمیب چسبنده را قبل از جدا شدن و تجزیه و تحلیل در حالت تعلیق حفظ کند.
آنها همچنین نیاز به شناسایی پارامترهای IFC داشتند که بهترین اطلاعات را در مورد رخدادهای مهم چرخه عفونت نشان میدهد. پس از بهینه سازی پروتکل، تیم توانست پنجره های زمانی را برای فرآیندهای سلولی مختلف به دست آورد و از IFC برای ارزیابی اثرات اختلالاتی مانند استرس اکسیداتیو و اختلالات اسکلت سلولی بر عفونت استفاده کند. با تراز کردن فرآیندها در یک جدول زمانی، محققان توانستند آنها را در سه فاز زمانی اصلی جمع کنند که عبارتند از 0-4 ساعت PI، 4-6 ساعت PI و 6 ساعت لیز سلولی.
این مطالعه نشان داد که استرس اکسیداتیو خفیف مراحل مختلف تکثیر ویروس را کند میکند، اگرچه فرآیندهای عفونت در نهایت در دامنه های مشابه اتفاق میافتد. این تیم در مجله Cytometry مینویسد: “در این مطالعه، ما نشان دادیم که IFC می تواند برای بررسی تغییرات زمانی و دامنه تکثیر در بین جمعیتهای سلولی آلوده برای بررسی رخدادهای کلیدی در تغیر مکانیزم سلولی و تکثیر ویروس استفاده شود.”
نقش اسکلت سلولی در عفونت
با استفاده از فلوسایتومتری تصویربرداری برای بررسی جنبههای خاص برهمکنشهای ویروس-سلول، تیم تحقیقاتی بعد از آن پرسیدند که آیا تغییرات اسکلت سلولی ممکن است به عفونت کمک کند یا خیر. هنگامی که محققان میکروتوبولها و ریز رشتههای اکتین را زیر نظر گرفتند، متوجه شدند که هر دو با جمع شدن سلولها و بیحرکت شدن سلولها در مرحله دوم عفونت در 4 تا 6 ساعت ، دچار دگرگونیهای ساختاری بزرگی میشوند.
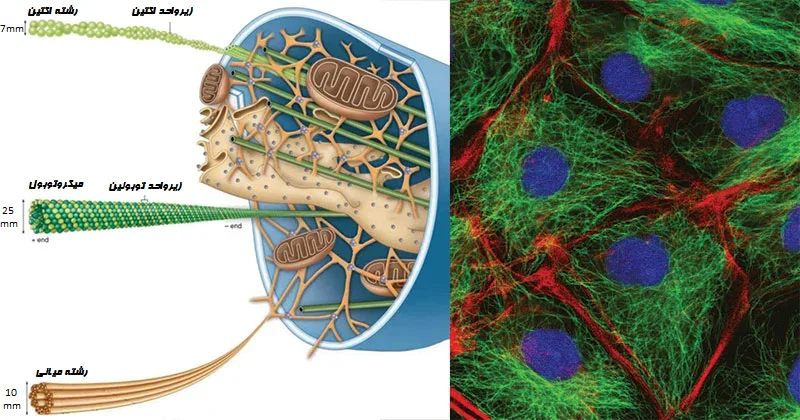
آنها پیشنهاد میکنند که انتقال میکروتوبولها به محیط سلول ممکن است فضایی را برای کارخانه ویروسی ) بخش های درون سلولی سلول میزبان که حاوی اندامک های تکثیر ویروسی و عناصر لازم برای مونتاژ و بلوغ ذرات ویروسی عفونی جدید است.(ایجاد کند تا بالغ شود و در مرکز سلول گسترش یابد و همچنین امکان تولید انبوه ویریونها را فراهم کند.
مینسکی و همکارانش میگویند: « چنین بازآرایی میکروتوبولی ممکن است نتیجه تغییرات در شبکه اکتین به دلیل عفونت ویروسی باشد، و بنابراین میکروتوبولها ممکن است مستقیم یا فعال در عفونت Mimivirus دخیل نباشند. برای یافتن اینکه آیا میکروفیلامنتهای اکتین برای عفونت لازمهستند یا خیر، محققان با استفاده از latrunculin-B رشته ها را مختل کردند. آنها سپس نقصهایی را در ادغام مراکز تکثیر با یک کارخانه ویروسی بالغ(VF) و تولید ویریونهای جدید مشاهده کردند.
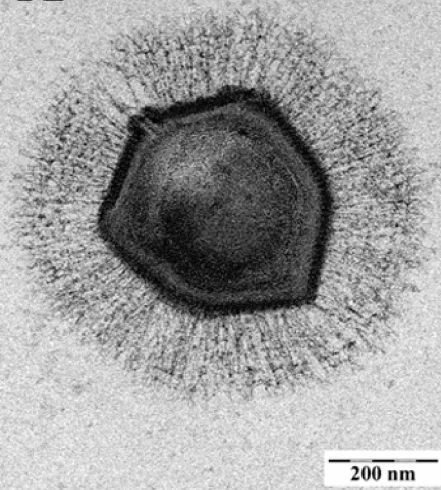
اگرچه دانشمندان به طور خاص بر روی نقش اسکلت سلولی میزبان در عفونت Mimivirus تمرکز کردند، آنها میگویند که این روش می تواند برای بسیاری از عوامل ویروسی یا سلولی دیگر که به طور بالقوه بر پیشرفت Mimivirus تأثیر می گذارد، اعمال شود.
تحقیقات آینده
اکنون تحقیقات بیشتری برای بررسی نحوه استفاده Mimivirus از اسکلت سلولی Acanthamoeba و روشن کردن مسائل اساسی دیگر چرخه عفونت ویروسی مورد نیاز است. در نهایت، آنها پیشنهاد میکنند که پلت فرم فلوسایتومتری تصویربرداری برای مطالعه چرخههای عفونت سایر ویروسها، بهویژه سایر ویروسهای غول پیکر تشکیلدهنده VF که اخیراً کشف شدهاند، برای تجزیه و تحلیل و کمی کردن تعاملات ویروس-میزبان و کشف پیشرفت عفونت در اختلالات مختلف استفاده شود.
تیم نتیجه گیری میکند: “از طریق این گزارش، ما نشان میدهیم که IFC یک رویکرد کمی با توان عملیاتی بالا و بسیار قوی برای مطالعه چرخه های عفونت ویروسی و تعامل ویروس-میزبان ارائه میدهد.”
همچنین بخوانید:
- اسکلت سلولی (Cytoskeleton): تعریف، ساختار، کارکردها و شکل آن
- فلوسایتومتری در سنجش عملکرد پلاکت در نوزادان
- فلوسایتومتری برای شناسایی اهداف واکسن برای SARS-CoV-2
- فلوسایتومتری در آنالیز سلولهای خون محیطی
- دوره مهارت آموزی فلوسایتومتری
- تشخیص آنیوپلوئیدی با فلوسایتومتری