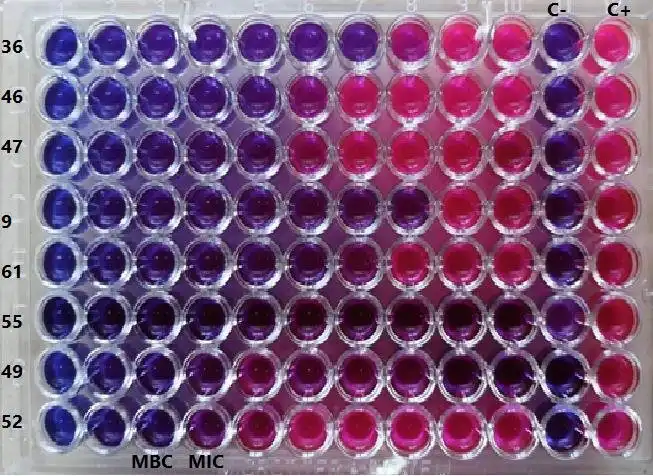
تکنیک MIC چیست؟
در علم میکروبیولوژی، غلظت مهارکنندگی حداقل که تحت عنوان تست MIC شناخته میشود، کمترین غلظت یک آنتی باکتری (مانند یک ضد قارچ، آنتی بیوتیک) میباشد که رشد قابل مشاهده یک میکروارگانیسم را بعد از یک شبانه روز انکوباسیون، مهار میکند. بعد از جداسازی کشت خالص، MIC ها را میتوان روی محیطهای کشت جامد یا آگار و یا محیط های کشت مایع رقیق شده، تشخیص داد.
مراحل انجام تست MIC
مراحل انجام تست MIC به اینگونه میباشد که کشت خالص میکروارگانیسم در محیط کشت مولر-هینتون یا سایر کشت های مناسب تهیه میشود. کشت مورد نظر بایستی استاندارد شود که از طریق تکنیکهای میکروبیولوژی استاندارد انجام میشود که در نهایت غلظت کشت مورد نظر به یک میلیون سلول در میلی لیتر برسد.
مسلما هر چقدر کشت میکروبی استاندارد تر باشد، نتایج تست تکرار پذیرتر میباشد. عوامل ضد میکروبی به دفعات رقیق میشوند که معمولا به صورت 1:1 انجام میشود، در مرحله ی بعدی، هم حجم عوامل ضد میکروبی رقیق شده، مایع تلقیح به هر کدام از محیط ها اضافه میشود که در نهایت غلظت میکروبی تقریبا به 500000 سلول در هر میلی لیتر میرسد.
عوامل ضد میکروبی تلقیح یافته رقیق شده، معمولا به مدت 18 ساعت در دمای مناسب انکوبه میشود. به منظور تکرار پذیر بودن نتایج آزمون بایستی دورهی انکوباسیون ثابت تر باشد. نتایج در نهایت به صورت کدورت یا رسوب میکروارگانیسم در انتهای ظرف گزارش داده میشود. آخرین لوله در سری رقت که رشدی را نشان نمیدهد، با حداقل غلظت مهاری (MIC) عامل ضد میکروبی، مطابقت دارد.
نقاط قوت و ضعف تکنیک MIC
آزمایش MIC یکسری نقاط قوت و نقات ضعفی دارد که در ابتدا به نقاط قوت آزمایش حداقل غلظت مهاری (MIC) اشاره میکنیم.
- سهولت و راحتی اجرای آزمایش MIC منجر به تکرار پذیر بودن آزمایش میشود.
- عوامل ضد میکروبی مورد نیاز در آزمایش MIC زیاد نمیباشد که در مقیاس کوچک قابل اجرا میباشد.
- اتلاف زمان در روش MIC کم میباشد چرا که آماده سازی کمی برای آزمون MIC مورد نیاز میباشد.
از جمله نقاط ضعف روش MIC میتوان به این مورد اشاره کرد تلقیح طولانی مدت باعث میشود که MIC بالاتر برود و مسلما غلظت پایین تلقیح باعث پایین آمدن MIC میشود. بنابراین میتوان نتیجه گرفت که تغییرات جزئی در پارامترهای تست MIC تاثیرات عمدهای بر MIC دارد.
تاریخچه تست MIC
پس از کشف و تجاری سازی آنتی بیوتیک ها، میکروبیولوژیست، فارماکولوژیست و پزشک، الکساندر فلمینگ، تکنیک رقیق سازی براث را با استفاده از کدورت براث برای ارزیابی توسعه داد. این معمولاً نقطه تصور حداقل غلظت های بازدارنده است. بعداً در دهه 1980، مؤسسه استانداردهای بالینی و آزمایشگاهی روشها و استانداردهای تعیین MIC و استفاده بالینی را ادغام کرد.
پس از کشف آنتیباکتریها، پاتوژنهای جدید و تکامل آنها، پروتکلهای CLSI نیز به طور مداوم به روز میشوند تا این تغییر را منعکس کنند. پروتکلها و پارامترهای تعیین شده توسط CLSI به عنوان «استاندارد طلایی» در ایالات متحده در نظر گرفته میشوند و توسط مقامات نظارتی، مانند FDA، برای ارزیابی استفاده میشوند.
کاربرد بالینی
امروزه از MIC در تست حساسیت ضد میکروبی استفاده میشود. MIC با ارائه تفسیر حساسیت در کنار هر آنتی بیوتیک گزارش میشود. تفاسیر مختلف حساسیت عبارتند از:
- S (حساس)
- I (متوسط)
- R (مقاوم)
این تفاسیر توسط موسسه استانداردهای بالینی و آزمایشگاهی (CLSI) ایجاد و اجرا شده است. در کلینیکها، بیشتر اوقات، پاتوژنهای دقیق را نمیتوان به راحتی با علائم بیمار تعیین کرد.
سپس، حتی اگر عامل بیماری زا مشخص شود، سروتیپهای مختلف پاتوژن، مانند استافیلوکوکوس اورئوس، سطوح متفاوتی از مقاومت به ضد میکروبی ها دارند. به این ترتیب، تجویز داروهای ضد میکروبی صحیح دشوار است. MIC در چنین مواردی با رشد پاتوژن ایزوله از بیمار در پلیت یا براث تعیین میشود که بعداً در سنجش استفاده میشود.
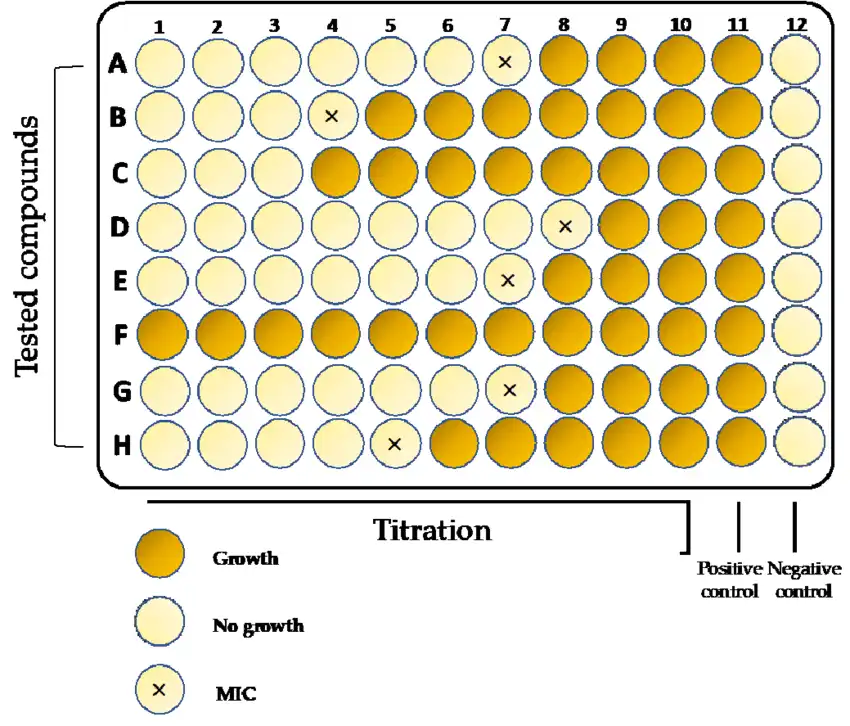
بنابراین، دانش MIC اطلاعات ارزشمندی را برای تهیه نسخه در اختیار پزشک قرار میدهد. استفاده دقیق و صحیح از داروهای ضد میکروبی نیز در زمینه باکتریهای مقاوم به چند دارو مهم است. میکروبهایی مانند باکتریها نسبت به ضد میکروبیهایی که قبلاً به آنها حساس بودند، مقاومت پیدا کردهاند. استفاده از سطوح ناسازگار ضد میکروبی فشار انتخابی را فراهم میکند که جهت و تکامل مقاومت پاتوژن های باکتریایی را هدایت میکند. به این ترتیب، تعیین MIC به منظور انجام بهترین انتخاب در تجویز داروهای ضد میکروبی اهمیت فزایندهای دارد.
MIC به صورت بالینی بیش از MBC استفاده میشود زیرا MIC آسانتر تعیین میشود. حداقل غلظت کشنده باکتری (MBC) که حداقل غلظت ضد باکتریایی است که منجر به مرگ میکروبی میشود، با عدم توانایی در کشت مجدد باکتریها تعریف میشود.
علاوه بر این، اثربخشی دارو به طور کلی زمانی مشابه است که در هر دو غلظت MIC و MBC مصرف شود، زیرا سیستم ایمنی میزبان میتواند پاتوژن را زمانی که تکثیر باکتریها متوقف شده است، دفع کند. هنگامی که MBC بسیار بالاتر از MIC باشد، سمیت دارویی مصرف MBC دارو را برای بیمار مضر میکند. سمیت ضد میکروبی میتواند به اشکال مختلفی مانند حساسیت بیش از حد ایمنی و سمیت خارج از هدف ظاهر شود.
روش های انجام تکنیک MIC
BROTH DILUTION ASSAY
سه معرف اصلی برای اجرای این سنجش ضروری است: محیط، یک عامل ضد میکروبی و خود میکروبی که در حال آزمایش است. متداولترین محیط مورد استفاده مولر هینتون براث تنظیمشده با کاتیون است، به دلیل توانایی آن در حمایت از رشد بیشتر پاتوژنها و فقدان مهارکنندههای آن نسبت به آنتیبیوتیکهای رایج.
بسته به پاتوژن و آنتی بیوتیک مورد آزمایش، محیط را می توان تغییر داد و یا تنظیم کرد. غلظت ضد میکروبی با مخلوط کردن مواد ضد میکروبی موجود با محیط به غلظت صحیح تنظیم میشود. ضد میکروبی تنظیم شده به صورت سریالی در چندین لوله (یا چاهک) رقیق می۷شود تا یک گرادیان به دست آید.
میزان رقت را می توان بسته به نقطه شکست و نیازهای پزشک تنظیم کرد. میکروب یا عامل تلقیح باید از همان واحد تشکیل دهنده کلنی باشد و باید در غلظت مناسب باشد. این ممکن است با زمان انکوباسیون و رقیق سازی تنظیم شود. برای تأیید، کنترل مثبت در رقت صد برابری برای شمارش واحدهای تشکیل دهنده کلنی قرار میگیرد. میکروبها، لولهها (یا پلیت) را تلقیح میکنند و به مدت 16 تا 20 ساعت انکوبه میشوند. MIC به طور کلی توسط کدورت تعیین میشود.
ETEST
Etest همچنین میتواند به عنوان یک روش جایگزین برای تعیین مقادیر حداقل غلظت بازدارنده طیف گستردهای از عوامل ضد میکروبی در برابر گروههای ارگانیسمهای مختلف استفاده شود که به طور گسترده در آزمایشگاههای میکروبیولوژی در سراسر جهان استفاده میشود. Etests ساخته شده توسط bioMérieux، یک نوار واکنشگر پلاستیکی غیر متخلخل و آماده برای استفاده با گرادیان آنتی بیوتیکی از پیش تعریف شده است که محدوده غلظت پیوسته را پوشش میدهد.

تفسیر نتایج تست MIC
مطالب مرتبط با تکنیک MIC: