فهرست مطالب
نمایش
تعریف تست نین هیدرین
تست نین هیدرین یک آزمایش شیمیایی است که برای تشخیص وجود آمونیاک، آمینهای اولیه/ ثانویه یا اسیدهای آمینه انجام میشود. این تست شامل افزودن شناساگر نین هیدرین در حضور یک گروه آمینه به نمونه آزمایشی است و منجر به تشکیل رنگ آبی تیره شده که اغلب به عنوان بنفش روهمان (Ruhemann’s purple) نامیده میشود.

اهداف تست نین هیدرین
- برای تشخیص وجود آمینها و گروههای آمینه در محلول آزمایش.
- برای تعیین کمیت اسیدهای آمینه موجود در نمونه.
- برای افتراق کربوهیدراتها از اسیدهای آمینه.
اصول تست نین هیدرین
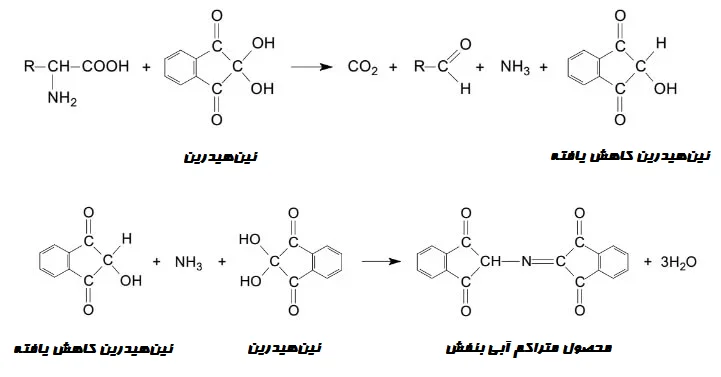
- این تست بر اساس این واقعیت است که دو مولکول نین هیدرین (2، 2- دی هیدروکسی یندان-1، 3-دیون (2, 2- dihydroxyindane-1, 3-dione)) با یک آلفا آمینو اسید آزاد واکنش داده تا یک رنگ بنفش تیره یا آبی به نام بنفش روهمان تولید کنند.
- در این واکنش نین هیدرین به عنوان یک عامل اکسیدکننده عمل میکند و باعث دآمیناسیون (Deamination) و دکربوکسیلاسیون (Decarboxylation) اسیدهای آمینه در دمای بالا میشود.
- سپس این واکنش با متراکم شدن بین مولکولهای نین هیدرین کاهش یافته، آمونیاک آزاد شده و مولکول دوم نین هیدرین دنبال میشود.
- در پایان واکنش، یک کمپلکس دیکتوهیدرین (Diketohydrin) تشکیل میشود که رنگ بنفش تیره دارد.
- در اسیدهای آمینه مانند پرولین (Proline) و هیدروکسی پرولین (Hydroxyproline)، این تست نمک ایمینیوم تولید میکند که به رنگ زرد- نارنجی است.
- به طور مشابه، پروتئینها با یک گروه آمین آزاد مانند آسپاراژین (Asparagine)، با شناساگر نین هیدرین واکنش داده و محصول قهوهای رنگی را ایجاد میکنند.
- سختی کمپلکس تشکیل شده متناسب با غلظت اسیدهای آمینه در محلول است.
- شدت رنگ به نوبه خود به نوع اسید آمینه موجود بستگی دارد.
واکنش
نیازمندیها
شناساگرها
- شناساگر نین هیدرین:35 گرم نین هیدرین را در 100 میلیلیتر اتانول حل کنید (ممکن است به جای اتانول از ایزوپروپانول (Isopropanol) یا مخلوط 1:1 استون/ بوتانول (Acetone /Butanol) استفاده شود).
- حلال رقیقکننده (برای آزمایش کمی): حجم مساوی از آب و n-پروپانول را با هم مخلوط کنید.
- محلول استاندارد (محلول پروتئین 1٪)
- محلول نمونه
وسایل مورد نیاز
- لولههای آزمایش
- پایه لوله آزمایش
- پیپت (Pipette)
تجهیزات
- بنماری (Water bath)
- اسپکتروفتومتر (Spectrophotometer)
روش تست نین هیدرین
برای تحلیل کیفی
- 1 میلیلیتر محلول پروتئین استاندارد را در یک لوله آزمایش و 1 میلیلیتر از نمونه تستی را در یک لوله آزمایش خشک دیگر بریزید.
- چند قطره شناساگر نین هیدرین را به هر دو لوله آزمایش اضافه کنید.
- لولههای آزمایش را به مدت 5 دقیقه در بنماری قرار داده و سپس اجازه دهید تا دمای اتاق خنک شود.
- شکلگیری رنگ را بررسی و نتیجه را یادداشت کنید.
برای آنالیز کمی
- حجمهای مختلف (10 میکرولیتر، 20 میکرولیتر و غیره) از محلول پروتئین استاندارد ذخیره شده داخل یک سری لولههای آزمایشی با پیپت بریزید و حجم هر کدام را با آب مقطر به 1 میلیلیتر برسانید.
- برای ساخت یک منحنی استاندارد، لولهای را با برچسب 1 که فقط حاوی 1 میلیلیتر آب مقطر است، لیبل بزنید و بقیه لولهها را با برچسب 2 تا 9 برچسب بزنید. لولههای 10 تا 15 برای نمونههای نامعلوم هستند.
- 1 میلیلیتر از شناساگر نین هیدرین و 5 میلیلیتر حلال رقیق کننده را به هر لوله اضافه کرده و با هم زدن خوب مخلوط کنید.
- لولهها را خنک کنید.
- روی لولهها را با درپوش بپوشانید و در دمای 90 درجه سانتیگراد به مدت 17 دقیقه انکوبه کنید یا در بنماری به مدت 20 دقیقه بجوشانید.
- لولهها را تا دمای اتاق خنک کرده و چگالی نوری محلولها را در طول موج 570 نانومتر (440 نانومتر برای پرولین و هیدروکسی پرولین) در مقایسه با لوله با لیبل 1 اندازهگیری کنید.
- یک منحنی استاندارد از ظرفیت جذب نور در مقابل غلظت اسید آمینه تهیه کنید.
- مقدار اسید آمینه را در نمونه نامعلوم با رسم منحنی استاندارد A570 در محور Y و غلظت اسید آمینه در محور X تعیین کنید.
نتیجه و تفسیر تست نین هیدرین

- وجود یک کمپلکس بنفش رنگ در لوله نشان دهنده یک نتیجه مثبت بوده و حاکی از وجود اسید آمینه در نمونه است.
- عدم وجود کمپلکس در لوله نشان دهنده یک نتیجه منفی است و بر فقدان اسیدهای آمینه در نمونه دلالت دارد.
- با استفاده از نمودار، میتوان غلظت نمونههای نامعلوم را تعیین کرد.
موارد استفاده از تست نین هیدرین
- از تست نین هیدرین برای تشخیص وجود اسیدهای آمینه در نمونههای نامعلوم استفاده میشود.
- این تست همچنین در سنتز پپتید (Peptide) به روش فاز جامد (Solid-phase) برای بررسی و تایید آنالیز اسید آمینه پروتئین استفاده میشود.
- از آنجایی که تست نین هیدرین بسیار حساس است، معمولا برای تشخیص اثر انگشت استفاده میشود. این امکان وجود دارد زیرا آمینهای پایانی رسوبات لیزین (Lysine) در پپتیدها و پروتئینهایی که در اثر انگشت جاری میشوند، با نین هیدرین واکنش نشان میدهند.
محدودیتهای تست نین هیدرین
- نین هیدرین نه تنها با گروههای α-آمینو واکنش میدهد، بلکه با نیتروژن موجود در آمونیاک و سایر آمینهای آزاد نیز واکنش میدهد.
- تست نین هیدرین برای تشخیص پروتئینها با وزن مولکولی بالا موثر نیست زیرا موانع فضایی (مربوط به نحوه استقرار اجزاء اتمها در فضا)، نین هیدرین را در رسیدن به گروههای α-آمینه محدود میکند.
همچنین بخوانید:
- تست میلون (Millon’s Test): تعریف، اصول، روش، نتیجه و موارد استفاده
- تست بیال (Bial): تعریف، اصول، روش، نتیجه و موارد استفاده
- تست تالنز (Tollen’s Test): تعریف، اصول، روش، نتایج و موارد استفاده
- تست ساکاگوچی (Sakaguchi Test): تعریف، اصول، روش، نتایج و موارد استفاده
مترجم: صادق حسینیکیا





اگر پروتئین با نین هیدرین وارد واکنش شود رنگ پخش میکند یا خیر؟ چرا ؟
بله، پروتئینها هنگامی که با نینهیدرین وارد واکنش میشوند، رنگ پخش میکنند، و این واکنش بهطور گستردهای برای تشخیص آمینواسیدها و پروتئینها استفاده میشود. نینهیدرین یک واکنشدهنده شیمیایی است که با آمینواسیدها و پپتیدها وارد واکنش شده و یک رنگ بنفش تیره یا آبی تولید میکند. این رنگ نشاندهنده وجود پروتئینها یا آمینواسیدها در نمونه است.
مکانیزم واکنش نینهیدرین با پروتئینها:
واکنش با گروههای آمینو: نینهیدرین با گروههای آمینو (−NH2) موجود در آمینواسیدهای پروتئینها وارد واکنش میشود. در این فرایند، گروه آمینو از آمینواسیدها یک پروتون از دست میدهد و یک آنیون آزاد شده تولید میکند که سپس با نینهیدرین واکنش میدهد.
تشکیل رنگدانه: در نتیجه واکنش شیمیایی بین نینهیدرین و آمینواسیدها، مادهای رنگی به نام روهمانس پورپل تولید میشود. این ماده دارای رنگ بنفش تیره است و میزان رنگ تولید شده میتواند برای سنجش مقدار آمینواسیدها در نمونه استفاده شود.
با سلام
ایا میتوان از تستنین هیدرین در تشخیص بهینه بودن یک داربست الکتروریسی شده استفده نمود بخصوصاگر از بیومتریال کلاژنی استفاده شده باشد و آیا در ژنیران انجام میشود ؟ با سپاس
در مورد استفاده از تست نین هیدرین برای ارزیابی بهینه بودن داربستهای الکتروریسی که از بیومتریالهای کلاژنی ساخته شدهاند، این تست میتواند مفید باشد به شرطی که هدف شناسایی و ارزیابی میزان و حالت کلاژن موجود در داربست باشد. استفاده از نین هیدرین میتواند به تعیین میزان کلاژن یا سایر پروتئینهای آزاد شده از داربست کمک کند، که این امر نشاندهنده کیفیت بیومتریال و فرایند تولید داربست است. از آنجا که کلاژن حاوی اسیدهای آمینه متعددی است که با نین هیدرین واکنش میدهند، حضور این اسیدهای آمینه آزاد میتواند نشاندهنده فعالیتهای بیوشیمیایی یا تخریب پروتئینی در داربست باشد.
کاربردهای عملی:
ارزیابی فرایند تولید داربست: بررسی میزان کلاژن و تجزیه آن در داربستها میتواند به ارزیابی روشهای تولید و پایداری داربستها کمک کند.
تحقیقات مواد: برای توسعه داربستهای جدید یا بهبود مواد موجود، تست نین هیدرین میتواند به ارزیابی اثر بخشی تغییرات در فرمولاسیون بیومتریالها کمک کند.
ملاحظات:
دقت دادهها: اطمینان از خلوص نمونه و شرایط آزمایش برای جلوگیری از نتایج نادرست ضروری است.
تفسیر نتایج: باید دقت کرد که نتایج به دست آمده از تست نین هیدرین باید با دادههای بیولوژیکی و مکانیکی دیگر تکمیل شوند تا تصویر کاملتری از عملکرد داربست حاصل شود.